
| A£®±äÉī | B£®±äĒ³ | C£®²»±ä | D£®ĪŽ·ØÅŠ¶Ļ |
 ĆūŹ¦µć¾¦×Ö“Ź¾ä¶ĪĘŖĻµĮŠ“š°ø
ĆūŹ¦µć¾¦×Ö“Ź¾ä¶ĪĘŖĻµĮŠ“š°ø
| Äź¼¶ | øßÖŠæĪ³Ģ | Äź¼¶ | ³õÖŠæĪ³Ģ |
| øßŅ» | øßŅ»Ćā·ŃæĪ³ĢĶĘ¼ö£” | ³õŅ» | ³õŅ»Ćā·ŃæĪ³ĢĶĘ¼ö£” |
| ø߶ž | ø߶žĆā·ŃæĪ³ĢĶĘ¼ö£” | ³õ¶ž | ³õ¶žĆā·ŃæĪ³ĢĶĘ¼ö£” |
| øßČż | øßČżĆā·ŃæĪ³ĢĶĘ¼ö£” | ³õČż | ³õČżĆā·ŃæĪ³ĢĶĘ¼ö£” |
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ²»Ļź ĢāŠĶ£ŗµ„Ń”Ģā
| A£®Ö»Ōö“óc£ØA£©Ź±£¬vŅ²Ōö“ó | B£®Ö»Ōö“óc£ØA£©Ź±£¬vÖµ²»±ä |
| C£®Ö»ÉżøßĪĀ¶ČŹ±£¬kÖµ²»±ä | D£®Ö»ÉżøßĪĀ¶ČŹ±£¬kÖµ±äŠ” |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ²»Ļź ĢāŠĶ£ŗµ„Ń”Ģā
| A£®½µµĶĢåĻµµÄĪĀ¶Č |
| B£®±£³ÖĢå»ż²»±ä£¬ĶØČėNO2£¬Ź¹ĢåĻµµÄŃ¹ĒæŌö“óŅ»±¶ |
| C£®±£³ÖĢå»ż²»±ä£¬ĶØČėN2£¬Ź¹ĢåĻµµÄŃ¹ĒæŌö“óŅ»±¶ |
| D£®±£³ÖŃ¹Ēæ²»±ä£¬ĶØČėAr£¬Ź¹ĢåĻµµÄĢå»żŌö“óŅ»±¶ |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ²»Ļź ĢāŠĶ£ŗµ„Ń”Ģā
| A£®²»±ä | B£®Ōö“ó | C£®¼õŠ” | D£®ĪŽ·ØÅŠ¶Ļ |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ²»Ļź ĢāŠĶ£ŗµ„Ń”Ģā
| A£®Ōö“óX»ņYµÄÅØ¶Č | B£®Ōö“óŃ¹Ēæ |
| C£®½µµĶĪĀ¶Č | D£®ÉżøßĪĀ¶Č |
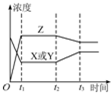
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ²»Ļź ĢāŠĶ£ŗµ„Ń”Ģā
A£®Q2£¾
| B£®Q2=
| ||||
| C£®Q2£¼Q1£¼197kJ | D£®Q2=Q1=197kJ |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ²»Ļź ĢāŠĶ£ŗµ„Ń”Ģā
| A£®H2£Øg£©+I2£Øg£©?2HI£Øg£©”÷H£¼0 |
| B£®4NH3£Øg£©+5O2£Øg£©?4NO£Øg£©+6H2O£Øg£©”÷H£¼0 |
| C£®N2£Øg£©+3H2£Øg£©?2NH3£Øg£©”÷H£¼0 |
| D£®2SO3£Øg£©?2SO2£Øg£©+O2£Øg£©”÷H£¾0 |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ²»Ļź ĢāŠĶ£ŗĢīæÕĢā
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ²»Ļź ĢāŠĶ£ŗĢīæÕĢā

²éæ““š°øŗĶ½āĪö>>
°Ł¶ČÖĀŠÅ - Į·Ļ°²įĮŠ±ķ - ŹŌĢāĮŠ±ķ
ŗž±±Ź”»„ĮŖĶųĪ„·ØŗĶ²»Į¼ŠÅĻ¢¾Ł±ØĘ½ĢØ | ĶųÉĻÓŠŗ¦ŠÅĻ¢¾Ł±Ø×ØĒų | µēŠÅÕ©Ę¾Ł±Ø×ØĒų | É꥜Ź·ŠéĪŽÖ÷ŅåÓŠŗ¦ŠÅĻ¢¾Ł±Ø×ØĒų | ÉęĘóĒÖČؾŁ±Ø×ØĒų
Ī„·ØŗĶ²»Į¼ŠÅĻ¢¾Ł±Øµē»°£ŗ027-86699610 ¾Ł±ØÓŹĻä£ŗ58377363@163.com