
依据事实,写出下列反应的热化学方程式。
(1)1molC2H4(g)与适量O2(g)反应生成CO2(g)和H2O(l),放出1411kJ热量。
(2)1molC2H5OH(l)与适量O2(g)反应生成CO2(g)和H2O(l),放出1366.8kJ热量。
(3)2molAl(s)与适量O2(g)反应生成Al2O3(s),放出1669.8kJ热量。
(1)C2H4(g)+3O2(g)=2CO2(g)+2H2O(l) △H=―1411kJ?mol-1
(2)C2H5OH(l)+3O2(g)=2CO2(g)+3H2O(l) △H=―1366.8kJ?mol-1
(3)Al(s)+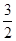 O2(g)=Al2O3(s) △H=―1669.8kJ?mol-1
O2(g)=Al2O3(s) △H=―1669.8kJ?mol-1
解析试题分析:该题考查的是热化学方程式的书写,关于热化学方程式的书写要注意以下几点:(1)△H只能写在标有反应物和生成物状态的化学方程式的右(后)边,并用“;”隔开。若为放热反应,△H为“-”;若为吸热反应,△H为“+”。△H的单位一般为KJ/mol。
(2)反应热△H与测定条件(温度、压强等)有关。书写热化学方程式时,应注明△H的测定条件(温度、压强),未指明温度和压强的反应热△H,指25℃(298K)、101KPa时的反应热△H(绝大多数反应热△H是在25℃、101KPa时测定的)。
(3)物质本身具有的能量与物质的聚集状态有关。反应物和生成物的聚集状态不同,反应热△H的数值以及符号都可能不同。因此,必须注明物质(反应物和生成物)的聚集状态(气体-g液体-l固体-s稀溶液-aq),才能完整地体现出热化学方程式的意义。热化学方程式中,不用“↑”和“↓”。
(4)热化学方程式中,各物质化学式前的化学计量数,只表示该物质的物质的量,可以是整数、分数、或小数。对相同化学反应,化学计量数不同,反应热△H也不同。如:H2(g)+1/2O2(g)=H2O(g);△H=-241.8KJ/mol2H2(g)+O2(g)=2H2O(g);△H=-483.6KJ/mol。普通化学方程式中各物质化学式前的化学计量数,既可以表示该物质的物质的量,又可以表示该物质的微粒数,还可以表示同温同压时的体积。
(5)相同条件(温度、压强),相同物质的化学反应(互逆反应,不一定是可逆反应),正向进行的反应和逆向进行的反应,其反应热△H数值相等,符号相反。如:2H2(g)+O2(g)=2H2O(l);△H=-571.6KJ/mol2H2O(l)=2H2(g)+O2(g);△H=+571.6KJ/mol
(6)反应热△H的单位KJ/mol中的“/mol”是指该化学反应整个体系(即指“每摩化学反应”),而不是指该反应中的某种物质。如2H2(g)+O2(g)=2H2O(l);△H=-571.6KJ/mol指“每摩2H2(g)+O2(g)=2H2O(l)反应”,放出571.6KJ的能量,而不是指反应中的“H2(g)、O2(g)、或H2O(l)”的物质的量。
(7)不论化学反应是否可逆,热化学方程式中的反应热△H表示反应进行到底(完全转化)时的能量变化。如:2SO2(g)+O2(g)=2SO3(g);△H=-197KJ/mol是指2molSO2(g)和1molO2(g)完全转化为2molSO3(g)时放出的能量。若在相同的温度和压强时,向某容器中加入2molSO2(g)和1molO2(g)反应达到平衡时,放出的能量为Q,因反应不能完全转化生成2molSO3(g),故Q<197KJ。
(8)反应热的大小比较,只与反应热的数值有关,与“+”“-”符号无关。“+”“-”只表示吸热或放热,都是反应热。如2H2(g)+O2(g)=2H2O(g);△H1=-aKJ/mol2H2(g)+O2(g)=2H2O(l);△H2=-bKJ/mol两反应的反应热的关系为a<b,但△H1>△H2
考点:考查热化学方程式的书写。


科目:高中化学 来源: 题型:填空题
氨气是生产化肥、硝酸等的重要原料,围绕合成氨人们进行了一系列的研究
(1)氢气既能与氮气又能与氧气发生反应,但是反应的条件却不相同。
已知:2H2 (g) + O2 (g) = 2H2O (g) ΔH =" -483.6" kJ/mol
3H2 (g) + N2 (g)  2NH3 (g) ΔH =" -92.4" kJ/mol
2NH3 (g) ΔH =" -92.4" kJ/mol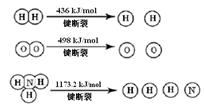
计算断裂1 mol N≡N键需要能量 kJ , 氮气分子中化学键比氧气分子中的化学键键 (填“强”或“弱”),因此氢气与二者反应的条件不同。
(2)固氮是科学家致力研究的重要课题。自然界中存在天然的大气固氮过程:N2 (g) + O2 (g) =" 2NO" (g) ΔH =" +180.8" kJ/mol ,工业合成氨则是人工固氮。
分析两种固氮反应的平衡常数,下列结论正确的是 。
| 反应 | 大气固氮 | 工业固氮 | ||||
| 温度/℃ | 27 | 2000 | 25 | 350 | 400 | 450 |
| K | 3.84×10-31 | 0.1 | 5×108 | 1.847 | 0.507 | 0.152 |
 2NH3 (g)测得甲容器中H2的转化率为40%。
2NH3 (g)测得甲容器中H2的转化率为40%。| | N2 | H2 | NH3 |
| 甲 | 1 | 3 | 0 |
| 乙 | 0.5 | 1.5 | 1 |
| 丙 | 0 | 0 | 4 |
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
随着大气污染的日趋严重,国家拟于“十二五”期间,将二氧化硫(SO2)排放量减少8%,氮氧化物(NOx)排放量减少10%。目前,消除大气污染有多种方法。
(1) 用CH4催化还原氮氧化物可以消除氮氧化物的污染。已知:
①CH4(g)+4NO2(g) ="4NO(g)" + CO2(g) +2H2O(g) ⊿H=" -574" kJ·mol-1
②CH4(g) +4NO(g) =2N2(g) + CO2(g) + 2H2O(g) ⊿H=" -1160" kJ·mol-1
③H2O(g) = H2O(l) △H=" -44.0" kJ·mol-1
写出CH4(g)与NO2(g)反应生成N2 (g)、CO2 (g)和H2O(1)的热化学方程式 。
(2)利用Fe2+、Fe3+的催化作用,常温下可将SO2转化为SO42-,从而实现对SO2的治理。已知含SO2的废气通入含Fe2+、Fe3+的溶液时,其中一个反应的离子方程式为4Fe2+ + O2+ 4H+ = 4Fe3+ + 2H2O,则另一反应的离子方程式为 。
(3)用活性炭还原法处理氮氧化物。有关反应为:C(s)+2NO(g) N2 (g)+CO2 (g) 。某研究小组向密闭的真空容器中(假设容器体积不变,固体试样体积忽略不计)加入NO和足量的活性炭,恒温(T1℃)条件下反应,反应进行到不同时间测得各物质的浓度如下:
N2 (g)+CO2 (g) 。某研究小组向密闭的真空容器中(假设容器体积不变,固体试样体积忽略不计)加入NO和足量的活性炭,恒温(T1℃)条件下反应,反应进行到不同时间测得各物质的浓度如下:
 浓度/mol·L-1 浓度/mol·L-1
| NO | N2 | CO2 | ||
| 0 | 1.00 | 0 | 0 | ||
| 10 | 0.58 | 0.21 | 0.21 | ||
| 20 | 0.40 | 0.30 | 0.30 | ||
| 30 | 0.40 | 0.30 | 0.30 | ||
| 40 | 0.32 | 0.34 | 0.17 | ||
| 50 | 0.32 | 0.34 | 0.17 |

查看答案和解析>>
科目:高中化学 来源: 题型:问答题
(14分)研究银及其化合物具有重要意义。
(l)已知:
Ag2O(s)+2HC1(g) 2AgC1(s)+H2O(1) △H1=-324.4 kJ·mo1-1
2Ag(s)+1/2O2(g) Ag2O(s) △H2=-30.6 kJ·mo1-1
H2(g)+C12(g) 2HC1(g) △H3=-184.4 kJ.·mo1-1
2H2(9)+O2(g) 2H2O(1) △H4=-571.2 l·mo1-1
写出氯气与银生成固体氯化银的热化学方程式________。
(2)美丽的银饰常用Fe(NO3)3溶液蚀刻,写出Fe3+与Ag反应的离子方程式___ _;要判定Fe(NO3)3溶液中NO3—是否在银饰蚀刻中发生反应,可取 的硝酸溶液,然后根据其是否与Ag发生反应来判定。
(3)银锌碱性电池的电解质溶液为KOH溶液,放电时,正极Ag2O2转化为Ag,负极Zn转化为Zn(OH)2,则正极反应式为 ,负极附近溶液的pH ___ (填“增大”、“不变”或“减小”)。
(4)电解法精炼银时,粗银应与直流电源的 极相连,当用AgNO3和HNO3混合溶液做电解质溶液时,发现阴极有少量红棕色气体,则产生该现象的电极反应式为____。
查看答案和解析>>
科目:高中化学 来源: 题型:问答题
硼及其化合物在耐髙温合金工业、催化剂制造、髙能燃料等方面应用广泛。
(1)氮化硼是一种耐高温材料,巳知相关反应的热化学方程式如下:
2B(s)+N2(g)= 2BN(s) ΔH="a" kJ ? mol-1
B2H6 (g)=2B(s) + 3H2 (g) ΔH =b kJ ? mol-1
N2 (g) + 3H2 (g) 2NH3 (g) ΔH ="c" kJ? mol-1
2NH3 (g) ΔH ="c" kJ? mol-1
①反应B2H6(g)+2NH3(g)=2BN(s)+6H2(g) ΔH = (用含a、b、c的代数式表示)kJ ·mol-1。
②B2H6是一种髙能燃料,写出其与Cl2反应生成两种氯化物的化学方程式: 。
(2)硼的一些化合物的独特性质日益受到人们的关注。
①最近美国化学家杰西·萨巴蒂尼发现由碳化硼制作的绿色焰火比传统焰火(硝酸钡)更安全,碳化硼中硼的质量分数为78. 6%,则碳化硼的化学式为 。
②近年来人们将LiBH4和LiNH2球磨化合可形成新的化合物Li3BN2H8和Li4BN3 H10,Li3BN2H8球磨是按物质的量之比n(LiNH2) : n(LiBH4) =" 2" : 1加热球磨形成的,反应过程中的X衍射图谱如图所示。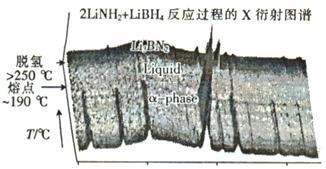
Li3BN2H8在大于250℃时分解的化学方程式为 ,Li3BN2H8与Li4BN3H10的物质的量相同时,充分分解,放出等量的H2,Li4BN3 H10分解时还会产生固体Li2NH和另一种气体,该气体是 。
(3)直接硼氢化物燃料电池的原理如图,负极的电极反应式为 。电池总反应的离子方程式为 。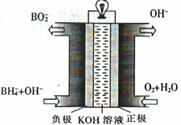
查看答案和解析>>
科目:高中化学 来源: 题型:计算题
近年来,以天然气等为原料合成甲醇的难题被一一攻克,极大地促进了甲醇化学的发展。
(1)与炭和水蒸气的反应相似,以天然气为原料也可以制得CO和H2,该反应的化学方程式为_________。
(2)合成甲醇的一种方法是以CO和H2为原料,其能量变化如图所示: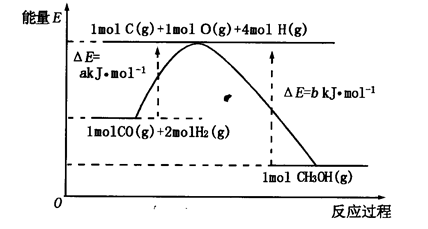
由图可知,合成甲醇的热化学方程式为________________________________________。
(3)以CO2为原料也可以合成甲醇,其反应原理为:CO2(g)+3H2(g) CH3OH(g)+H2O(g)
CH3OH(g)+H2O(g)
①在lL的密闭容器中,充入1molCO2和3molH2,在500℃下发生反应,测得CO2(g)和CH3OH(g)的浓度随时问变化如图所示:
则下列说法正确的是_________________(填字母);
| A.3min时反应达到平衡 |
| B.0~10min时用H2表示的反应速率为0.225mol·-1·min-1 |
| C.CO2的平衡转化率为25% |
D.该温度时化学平衡常数为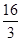 (mol/L)-2 (mol/L)-2 |
| 容器 | 容器1 | 容器2 | 容器3 |
| 反应物投入量(始态) | 1molCO2、3molH2 | 0.5molCO2、1.5molH2 | 1molCH3OH、1molH2O |
| CH3OH的平衡浓度/mol?L-1 | c1 | c2 | c3 |
| 平衡时体系压强/Pa | p1 | p2 | p3 |

查看答案和解析>>
科目:高中化学 来源: 题型:计算题
工业上采用乙苯与CO2脱氢生产重要化工原料苯乙烯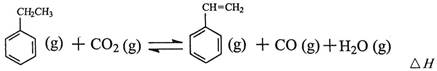
其中乙苯在CO2气氛中的反应可分两步进行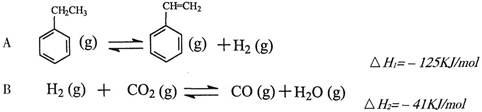
(1)上述乙苯与CO2反应的反应热△H为________________________。
(2)①乙苯与CO2反应的平衡常数表达式为:K=______________________。
②下列叙述不能说明乙苯与CO2反应已达到平衡状态的是_____________________。
a.v正(CO)=v逆(CO) b.c(CO2)=c(CO)
c.消耗1mol CO2同时生成1molH2O d.CO2的体积分数保持不变
(3)在3L密闭容器内,乙苯与CO2的反应在三种不同的条件下进行实验,乙苯、CO2的起始浓度分别为1.0mol/L和3.0mol/L,其中实验I在T1℃、0.3MPa,而实验II、III分别改变了实验其他条件;乙苯的浓度随时间的变化如图I所示。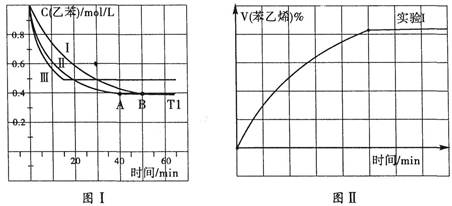
①实验I乙苯在0~50min时的反应速率为_______________。
②实验II可能改变条件的是__________________________。
③图II是实验I中苯乙烯体积分数V%随时间t的变化曲线,请在图II中补画实验Ⅲ中苯乙烯体积分数V%随时间t的变化曲线。
(4)若实验I中将乙苯的起始浓度改为1.2mol/L,其他条件不变,乙苯的转化率将(填“增大”、“减小”或“不变”),计算此时平衡常数为_____________________。
查看答案和解析>>
科目:高中化学 来源: 题型:计算题
一定条件下,通过下列反应可实现燃煤烟气中硫的回收:
2CO(g)+SO2(g)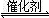 2CO2(g)+S(l) △H
2CO2(g)+S(l) △H
(1)已知2CO(g)+O2(g)= 2CO2(g) △H1=—566kJ?mol—1
S(l) +O2(g)= SO2(g) △H2=—296kJ?mol—1
则反应热ΔH= kJ?mol-1。
(2)其他条件相同、催化剂不同时,SO2的转化率随反应温度的变化如图a。260℃时 (填Fe2O3、NiO或Cr2O3)作催化剂反应速率最快。Fe2O3和NiO作催化剂均能使SO2的转化率达到最高,不考虑价格因素,选择Fe2O3的主要优点是 。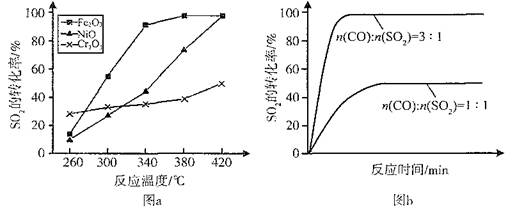
(3)科研小组在380℃、Fe2O3作催化剂时,研究了不同投料比[n(CO)∶n(SO2)]对SO2转化率的影响,结果如图b。请在答题卡坐标图中画出n(CO)∶n(SO2)="2∶1" 时,SO2转化率的预期变化曲线。
(4)工业上还可用Na2SO3溶液吸收烟气中的SO2:Na2SO3+SO2+H2O=2NaHSO3。某温度下用1.0mol?L-1 Na2SO3溶液吸收纯净的SO2,当溶液中c(SO32-)降至0.2mol?L-1时,吸收能力显著下降,应更换吸收剂。
①此时溶液中c(HSO3-)约为______mol?L-1;
②此时溶液pH=______。(已知该温度下SO32—+H+ HSO3—的平衡常数K="8.0" × 106 L?mol-1,计算时SO2、H2SO3的浓度忽略不计)
HSO3—的平衡常数K="8.0" × 106 L?mol-1,计算时SO2、H2SO3的浓度忽略不计)
查看答案和解析>>
科目:高中化学 来源: 题型:单选题
已知反应A2(g)+2B2(g) 2AB2(g)△H <0,下列说法正确的
2AB2(g)△H <0,下列说法正确的
| A.升高温度,正向反应速率增加,逆向反应速率减小 |
| B.升高温度有利于反应速率增加,从而缩短达到平衡的时间 |
| C.达到平衡后,升高温度或增大压强都有利于该反应平衡正向移动 |
| D.达到平衡后,降低温度或减小压强都有利于该反应平衡正向移动 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com