
分析 (1)盐酸为强酸,碳酸为弱酸,硅酸的酸性比碳酸更弱;
(2)先用盐酸与碳酸钠反应得到二氧化碳,二氧化碳与硅酸钠反应生成硅酸,据此可以一次性完成实验.
解答 解:(1)盐酸、碳酸、硅酸的酸性强弱顺序是:HCl>H2CO3>H2SiO3,故答案为:HCl>H2CO3>H2SiO3;
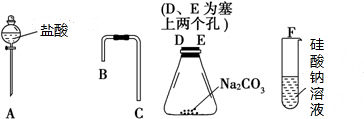
(2)盐酸、碳酸、硅酸的酸性强弱为HCl>H2CO3>H2SiO3,根据强酸制取弱酸知,盐酸和碳酸钠反应制取二氧化碳,二氧化碳和硅酸钠溶液反应制取硅酸,所以仪器的连接顺序是:A→D→E→B→C→F,
故答案为:A;D;E;B;C;F.
点评 本题考查了探究顺序强弱的实验,题目难度不大,明确实验目的为解答关键,结合强酸制取弱酸实验原理来分析解答,试题培养了学生的分析能力及化学实验能力.


科目:高中化学 来源: 题型:解答题

查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | -3 | B. | +4 | C. | +3 | D. | +2 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:解答题

| 试管编号 | ① | ② | ③ | ④ | ⑤ |
| NaNO2含量/mg•L-1 | 0 | 20 | 40 | 60 | 80 |
| 实验方案 | 实验现象 | 实验结论 |
| 取5mL 待测液,加入一定量的维生素C,振荡, 再加入1mL M溶液,加入至蒸馏水10mL,再振荡, 与④号色阶对比. | 紫红色比④色阶浅 | 维生素C 可以有效降低NaNO2的含量. |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
 某模拟“人工树叶”电化学实验装置如图所示,该装置能将H2O和CO2转化为O2和燃料(C3H8O).下列说法正确的是( )
某模拟“人工树叶”电化学实验装置如图所示,该装置能将H2O和CO2转化为O2和燃料(C3H8O).下列说法正确的是( )| A. | 该装置工作时,b极发生还原反应 | |
| B. | 每生成1molO2,有44gCO2被还原 | |
| C. | 该装置工作时,H+从a极区通过质子交换膜向b极区迁移 | |
| D. | a电极的反应为:3CO2+18H++18e-═C3H8O+5H2O |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com