
| 高温高压 |
| 催化剂 |
| A、2s | B、1s |
| C、0.67s | D、1.2s |
 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案科目:高中化学 来源: 题型:
| A、酸性氧化物一定是非金属氧化物,非金属氧化物不一定是酸性氧化物 |
| B、碱性氧化物一定是金属氧化物,金属氧化物不一定是碱性氧化物 |
| C、电离出的阳离子全部是H+的物质一定是酸 |
| D、能与酸反应的氧化物一定是碱性氧化物 |
查看答案和解析>>
科目:高中化学 来源: 题型:

查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
 实验室需用98ml 1.0mol/L 硫酸,现用浓硫酸(标签如下图)配制.实验仪器有:A.25ml量筒 B.托盘天平 C.玻璃棒 D.50ml容量瓶 E.10ml量筒 F.胶头滴管 G.50ml烧杯 H.100ml容量瓶 I.200ml容量瓶
实验室需用98ml 1.0mol/L 硫酸,现用浓硫酸(标签如下图)配制.实验仪器有:A.25ml量筒 B.托盘天平 C.玻璃棒 D.50ml容量瓶 E.10ml量筒 F.胶头滴管 G.50ml烧杯 H.100ml容量瓶 I.200ml容量瓶查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
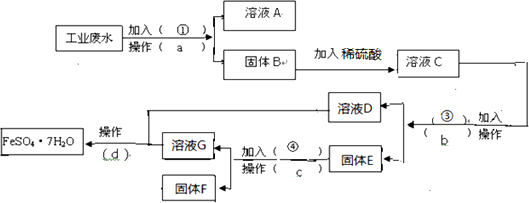
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com