
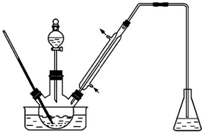
 实验室以苯甲醛为原料制备间溴苯甲醛(实验装置如图,相关物质的沸点见附表).
实验室以苯甲醛为原料制备间溴苯甲醛(实验装置如图,相关物质的沸点见附表).| 物质 | 沸点/℃ | 物质 | 沸点/℃ |
| 溴 | 58.8 | 1,2-二氯乙烷 | 83.5 |
| 苯甲醛 | 179 | 间溴苯甲醛 | 229 |
分析 苯甲醛与溴在氯化铝催化作用下在60℃时反应生成间溴苯甲醛,通式生成HBr,经冷凝回流可到间溴苯甲醛,生成的HBr用氢氧化钠溶液吸收,防止污染空气,有机相中含有Br2,加入HCl,可用碳酸氢钠除去,有机相加入无水MgSO4固体,可起到吸收水的作用,减压蒸馏,可降低沸点,避免温度过高,导致间溴苯甲醛被氧化,以此解答该题.
解答 解:(1)因溴易挥发,为使溴充分反应,应进行冷凝回流,以增大产率,反应发生取代反应,生成间溴苯甲醛的同时生成HBr,用氢氧化钠溶液吸收,防止污染空气,
故答案为:冷凝回流;NaOH;
(2)将三颈瓶中的一定配比的无水AlCl3、1,2-二氯乙烷和苯甲醛充分混合,三种物质中无水AlCl3为催化剂,1,2-二氯乙烷为溶剂,苯甲醛为反应物,
故答案为:AlCl3;
(3)将反应混合物含有溴,缓慢加入一定量的稀盐酸中,加入碳酸氢钠,可与Br2、HCl反应,
故答案为:Br2、HCl;
(4)经洗涤的有机相含有水,加入适量无水MgSO4固体,可起到除去有机相的水的作用,
故答案为:除去有机相的水;
(5)减压蒸馏,可降低沸点,避免温度过高,导致间溴苯甲醛被氧化,
故答案为:间溴苯甲醛被氧化.
点评 本题考查有机物的制备,为高考常见题型和高频考点,侧重于学生的分析能力和实验能力的考查,注意把握基本实验操作方法以及实验的原理,难度不大.


 小学学习好帮手系列答案
小学学习好帮手系列答案 小学同步三练核心密卷系列答案
小学同步三练核心密卷系列答案科目:高中化学 来源: 题型:解答题
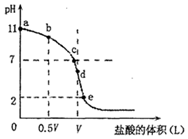 c(NH4+)+c(H+)=c(NH3•H2O)+c(OH-)
c(NH4+)+c(H+)=c(NH3•H2O)+c(OH-)查看答案和解析>>
科目:高中化学 来源: 题型:填空题
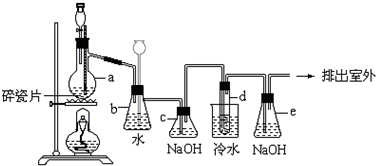
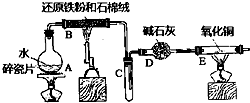 某校化学小组学生利用如图所列装置进行“铁与水反应”的实验,并进行了其他有关实验.(图中夹持及尾气处理装置均已略去)
某校化学小组学生利用如图所列装置进行“铁与水反应”的实验,并进行了其他有关实验.(图中夹持及尾气处理装置均已略去)查看答案和解析>>
科目:高中化学 来源: 题型:解答题
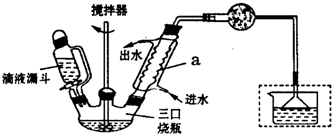
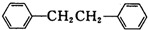 )是一种重要的有机合成中间体,实验室可用苯和1,2一二氯乙烷(ClCH2CH2Cl)为原料,在无水AlCl3催化下加热制得,其制取步骤为:
)是一种重要的有机合成中间体,实验室可用苯和1,2一二氯乙烷(ClCH2CH2Cl)为原料,在无水AlCl3催化下加热制得,其制取步骤为:
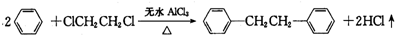
| 名称 | 相对分子质量 | 密度/(g•cm-3) | 熔点/℃ | 沸点/℃ | 溶解性 |
| 苯 | 78 | 0.88 | 5.5 | 80.1 | 难溶水,易溶乙醇 |
| 1,2-二氯化烷 | 99 | 1.27 | -35.3 | 83.5 | 难溶水,可溶苯 |
| 无水氯化铝 | 133.5 | 2.44 | 190 | 178(升华) | 遇水分解,微溶苯 |
| 联苄 | 182 | 0.98 | 52 | 284 | 难溶水,易溶苯 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 若温度不变,将容器的体积缩小到原来的一半,此时A的浓度为原来的2.1倍,则m+n<p+q | |
| B. | 若平衡时,A、B的转化率相等,说明反应开始时,A、B的物质的量之比为m:n | |
| C. | 若m+n=p+q,则往含有a mol气体的平衡体系中再加入a mol的B,达到新平衡时,气体的总物质的量等于2a | |
| D. | 若温度不变时,压强增大到原来的2倍,达到新平衡时,总体积一定比原来的$\frac{1}{2}$要小 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| t/min | 0 | 2 | 4 | 6 | 8 | 10 |
| V(O2)/mL | 0.0 | 9.9 | 17.2 | 22.4 | 26.5 | 29.9 |
| A. | 0~6min的平均反应速率:v(H2O2)≈3.3×10-2mol/(L•min) | |
| B. | 6~10min的平均反应速率:v(H2O2)<3.3×10-2mol/(L•min) | |
| C. | 反应至6min时,c(H2O2)=0.3mol/L | |
| D. | 反应至6min时,H2O2分解了50% |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 萃取操作时,应选择有机萃取剂,且萃取剂的密度必须比水大 | |
| B. | 用蒸发的方法使NaCl从溶液中析出时,玻璃棒的作用是引流 | |
| C. | 蒸馏操作时,应使温度计水银球插入蒸馏烧瓶的液面以下 | |
| D. | 分液时,分液漏斗下层液体从下口放出,上层液体从上口倒出 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
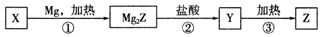
| A. | X可以和氢氟酸反应 | |
| B. | 甲烷的稳定性比Y强 | |
| C. | Z是将太阳能转换为电能的常用材料 | |
| D. | 上述①②③变化过程中,依次发生置换反应、复分解反应和分解反应 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com