
【题目】某同学在研究前18号元素时发现,可以将它们排成如图所示的“蜗牛”形状,图中每个“”代表一种元素,其中O点代表氢元素.下列说法中错误的是
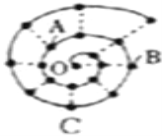
A. O与A、B、C均能形成两种化合物
B. A元素位于元素周期表ⅥA族
C. B元素是图中金属性最强的元素
D. B、C最高价氧化物的水化物可以相互反应
科目:高中化学 来源: 题型:
【题目】二氧化钛是一种重要的工业原料.
(1)实验室可通过以下方法制得:TiCI4 ![]() TiO2xH2O
TiO2xH2O ![]() TiO2TiCl4水解生成TiO2xH2O的化学方程式是;检验TiO2xH2O中Cl﹣是否被除净的方法是 .
TiO2TiCl4水解生成TiO2xH2O的化学方程式是;检验TiO2xH2O中Cl﹣是否被除净的方法是 .
(2)工业上可用含Fe2O3的钛铁矿(主要成分为FeTiO3 , 其中Ti化合价为+4价)制取,其主要流程如下: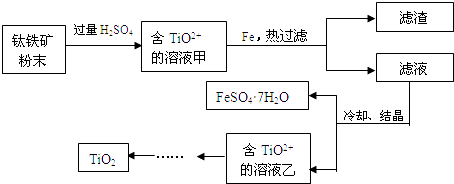
Fe2O3与硫酸反应的离子方程式是;向甲溶液中加入铁的目的是 .
(3)二氧化钛可用于制取金属钛,其步骤如下:TiO2![]() TiCl4
TiCl4![]() Ti反应②的方程式是 , 该反应需要在Ar的气氛中进行,原因是 .
Ti反应②的方程式是 , 该反应需要在Ar的气氛中进行,原因是 .
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】X、Y、Z、W各代表一种物质,若X+Y=Z+W,则X和Y的反应不可能是( )
A.盐和盐的反应B.碱性氧化物和水的反应
C.酸与碱的反应D.酸性氧化物和碱的反应
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某同学设计如图所示装置分别进行探究实验(夹持装置已略去) 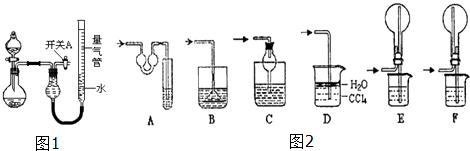
实验 | 药品 | 制取气体 | 量气管中的液体 |
① | Cu、稀HNO3 | H2O | |
② | NaOH固体、浓氨水 | NH3 | |
③ | Na2CO3固体、稀H2SO4 | CO2 | |
④ | 镁铝合金、NaOH溶液(足量) | H2 | H2O |
请回答下列问题:
(1)简述如何检查该装置的气密性: .
(2)该同学认为实验①可通过收集测量NO气体的体积,来探究Cu样品的纯度.你认为是否可行?请简述原因. .
(3)实验②中剩余的NH3需吸收处理.以下各种尾气吸收装置中,适合于吸收NH3 , 而且能防止倒吸的有
(4)实验③中,量气管中的液体最好是 .
A.H2O
B.CCl4
C.饱和Na2CO3溶液
D.饱和NaHCO3溶液
(5)本实验应对量气管多次读数,读数时应注意: ①恢复至室温,② , ③视线与凹液面最低处相平.
(6)实验④获得以下数据(所有气体体积均已换算成标准状况)
编号 | 镁铝合金质量 | 量气管第一次读数 | 量气管第二次读数 |
① | 1.0g | 10.0mL | 346.3mL |
② | 1.0g | 10.0mL | 335.0mL |
③ | 1.0g | 10.0mL | 345.7mL |
根据上述合理数据计算镁铝合金中铝的质量分数 .
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】海水中有取之不尽的化学资源,从海水中可提取多种化工原料,下图是某化工厂对海水资源综合利用的示意图:

试回答下列问题:
(1)实验室里将粗盐制成精盐的过程中,过滤的操作需用到玻璃棒,玻璃棒的作用是:____,还需要的玻璃仪器有:____。
(2)粗盐中含有Ca2+、 Mg2+、 SO42-等杂质,精制后可得NaCl饱和溶液,精制时通常在溶液中:①加入过量的BaC12溶液,②过量的NaOH溶液,③过量的Na2C03溶液,则添加试剂顺序为____(填写序号),最后在滤液加入盐酸至溶液呈中性。请写出加入盐酸后可能发生反应的离子方程式:____。
(3)海水提取食盐后的母液中有K+、Na+、Mg2+等阳离子。从离子反应的角度考虑,在母液里加入石灰乳发生反应的离子方程式:____。
(4)电解无水氯化镁制取镁的化学方程式为____。将镁蒸气冷却后即为固体镁,镁蒸气需在Ar气氛围中冷却,理由:____。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】Na、Cu、Fe、Cl、O、N是常见的6种元素.
(1)Fe位于元素周期表第周期第族;O的基态原子核外有个未成对电子.Cu的基态原子电子排布式为 .
(2)用“>”或“<”填空:
第一电离能 | 原子半径 | 稳定性 |
NO | CNa | NH3H2O |
(3)液态N2H4与液态N2O4反应生成气态水,在25℃、101kPa下,已知该反应每消耗1mol N2H4放出519.85kJ的热量,该反应的热化学反应方程式是:
(4)古老的但仍是最有用的制备N2H4的方法是NaClO溶液氧化过量的NH3 , 写出该反应的离子方程式,并标出电子转移的方向和数目 .
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】求25℃时以下溶液的pH
(1)pH=3的盐酸与pH=5的硫酸等体积混合后,pH=
(2)pH=10和pH=12的两种NaOH溶液等体积混合后,pH=
(3)pH=9的NaOH溶液稀释到原来的10倍后,pH= , 再稀释到原来的1000倍后,pH .
(4)pH=12的NaOH和pH=4的HCl等体积混合后,pH= .
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】饱和盐溶液W的电解产物发生下列系列反应.图中的每一方格表示有关的一种主要反应物或生成物(反应中加入或生成的水以及生成的其它产物已略去),其中A、B、C、D、E在常温下均为气态物质,X和K是中学常见的金属单质,氧化物Y是一种比较好的耐火材料.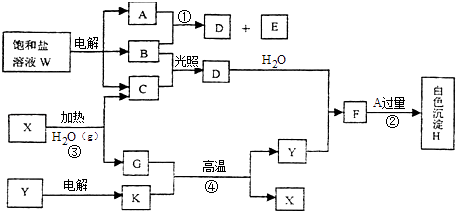
回答下列问题:
(1)X、Y的化学式是:X , Y .
(2)A的电子式是 , B的晶体类型是 .
(3)反应②的离子方程式是 .
(4)饱和盐溶液W电解的化学方程式是 .
(5)已知C的燃烧热为285.8kJ/mol.试写出C(用化学式表示)燃烧生成液态物质的热化学方程式 .
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com