

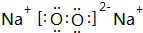
 ,
, ;
;

 暑假作业海燕出版社系列答案
暑假作业海燕出版社系列答案科目:高中化学 来源: 题型:
| A、甲醇 | B、甲醛 | C、甲酸 | D、甲苯 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| H+ |
| ①转化 |
| Fe2+ |
| ②还原 |
| OH- |
| ③沉淀 |
查看答案和解析>>
科目:高中化学 来源: 题型:
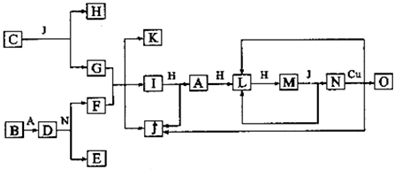
查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
A、按照系统命名法, 的名称为3,3,4-三甲基己烷 的名称为3,3,4-三甲基己烷 |
| B、乙醇、乙酸和乙酸乙酯可以用饱和Na2CO3溶液鉴别 |
| C、苯乙烯中所有原子可能共平面 |
D、1.0mol的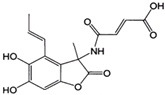 与NaOH溶液和Br2反应时,分别需要消耗NaOH 5.0mol和Br2 3.0mol 与NaOH溶液和Br2反应时,分别需要消耗NaOH 5.0mol和Br2 3.0mol |
查看答案和解析>>
科目:高中化学 来源: 题型:
| 选项 | 物质转化关系 | a | b | c | d |
| A | 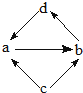 |
FeCl2 | FeCl3 | Fe | CuCl2 |
| B | NO | NO2 | N2 | HNO3 | |
| C | Na2CO3 | NaOH | Na2O2 | NaHCO3 | |
| D | Al2O3 | NaAlO2 | Al | Al(OH)3 |
| A、A | B、B | C、C | D、D |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、正极反应式为:O2+2H2O+4e-═40H - |
| B、电池工作时,电流由铝电极沿导线流向铂电极 |
| C、以网状的铂为正极,可增大与氧气的接触面积 |
| D、该电池通常只需更换铝板就可继续使用 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、离子化合物中可能含共价键 |
| B、共价化合物中一定不含离子键 |
| C、所有物质中都含有化学键 |
| D、离子化合物中不一定含金属元素 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com