
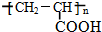 、GCH3CH(OH)CH2OH;
、GCH3CH(OH)CH2OH;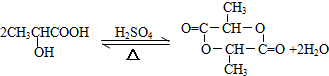 ;②F→A
;②F→A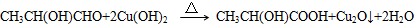 .
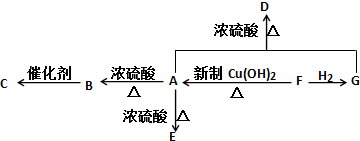
. 分析 E分子不饱和度=$\frac{6×2+2-8}{2}$=3,则E中不含苯环,F和新制氢氧化铜悬浊液发生反应生成A,则A中含有羧基、F中含有醛基,F和氢气发生加成反应生成G,则G中含有醇羟基,两分子A能生成一分子E,分子式为C6H8O4,A发生酯化反应生成E,E结构简式为 ,A结构简式为CH3CH(OH)COOH;
,A结构简式为CH3CH(OH)COOH;
A发生消去反应生成B,B发生加聚反应生成高分子化合物C,则B为CH2=CHCOOH,C为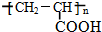 ,F发生氧化反应生成A,则F含有-CHO,故F为CH3CH(OH)CHO,F与氢气反应生成G,则G为CH3CH(OH)CH2OH,故D为
,F发生氧化反应生成A,则F含有-CHO,故F为CH3CH(OH)CHO,F与氢气反应生成G,则G为CH3CH(OH)CH2OH,故D为 ,据此分析解答.
,据此分析解答.
解答 解:E分子不饱和度=$\frac{6×2+2-8}{2}$=3,则E中不含苯环,F和新制氢氧化铜悬浊液发生反应生成A,则A中含有羧基、F中含有醛基,F和氢气发生加成反应生成G,则G中含有醇羟基,两分子A能生成一分子E,分子式为C6H8O4,A发生酯化反应生成E,E结构简式为 ,A结构简式为CH3CH(OH)COOH;
,A结构简式为CH3CH(OH)COOH;
A发生消去反应生成B,B发生加聚反应生成高分子化合物C,则B为CH2=CHCOOH,C为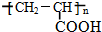 ,F发生氧化反应生成A,则F含有-CHO,故F为CH3CH(OH)CHO,F与氢气反应生成G,则G为CH3CH(OH)CH2OH,故D为
,F发生氧化反应生成A,则F含有-CHO,故F为CH3CH(OH)CHO,F与氢气反应生成G,则G为CH3CH(OH)CH2OH,故D为 ,
,
(1)通过以上分析知,A生成B是消去反应、B生成C是加聚反应、A生成E是酯化反应,
故答案为:消去反应;加聚反应;酯化反应;
(2)A、C、G的结构简式分别为CH3CH(OH)COOH、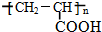 、CH3CH(OH)CH2OH,
、CH3CH(OH)CH2OH,
故答案为:CH3CH(OH)COOH;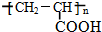 ;CH3CH(OH)CH2OH;
;CH3CH(OH)CH2OH;
H2SO4△
(3)①A→E的反应方程式为: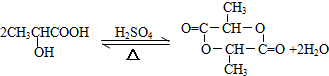 ,
,
②F→A反应方程式为: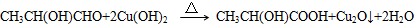 ,
,
故答案为: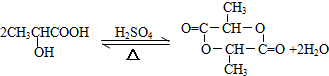 ;
;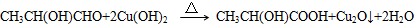 .
.
点评 本题考查有机物推断,为高频考点,侧重考查分析推断能力,正确判断C结构简式是解本题关键,再结合题给信息、反应条件进行推断,题目难度不大.


科目:高中化学 来源: 题型:选择题
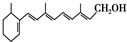 ,式中以线示键,线的交点与端点处代表碳原子,并用氢原子数补足四价,但C、H原子未标记出来,关于它的叙述正确的是( )
,式中以线示键,线的交点与端点处代表碳原子,并用氢原子数补足四价,但C、H原子未标记出来,关于它的叙述正确的是( )| A. | 维生素A的分子式为C20H30O | |
| B. | 维生素A中含有苯环 | |
| C. | 维生素A中可以使溴水褪色 | |
| D. | 1mol维生素A在催化剂作用下最多可与7molH2发生加成反应 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 2CH2=CH2+O2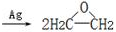 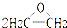 是理想的原子经济,原子利用率为100% 是理想的原子经济,原子利用率为100% | |
| B. | 含磷合成洗涤剂易被细菌分解,故不会导致水体污染 | |
| C. | CO2的大量排放能破坏臭氧层,形成“臭氧空洞” | |
| D. | pH在5.6~7.0之间的降水通常称为酸雨 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | Na+、OH-、Cl- | B. | Na+、NH4+、Cl- | C. | Cu2+、K+、Cl- | D. | K+、SO32-、ClO- |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 软脂酸 C17H33COOH | B. | 纯碱 Na2CO3•10H2O | ||
| C. | 纤维素[C6H7O2(OH)3]n | D. | 丙氨酸 CH2(NH2)CH2COOH |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
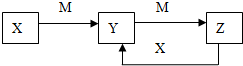 物质X、Y、Z有如图转化关系:请回答下列问题:
物质X、Y、Z有如图转化关系:请回答下列问题:查看答案和解析>>
科目:高中化学 来源: 题型:解答题
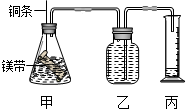
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 向饱和Na2CO3溶液中通入过量的CO2,溶液中无明显现象 | |
| B. | 检验某溶液是否含有SO${\;}_{4}^{2-}$时,应取少量该溶液,依次加入BaCl2溶液和稀盐酸 | |
| C. | 已知H+(aq)+OH-(aq)═H2O(l);△H=-57.3 kJ/mol.将4 g氢氧化钠固体放入100mL1mol/L的稀盐酸中,放出了5.73 kJ的热量 | |
| D. | 向100ml1mol/L的Ca(HCO3)2 溶液中加入等浓度等体积的NaOH溶液,溶液的碱性减弱 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | X、Y分子式中氢原子数不一定要相同,碳原子数必定不同 | |
| B. | 若X为CH4,则相对分子质量最小的Y是甲醇 | |
| C. | 若X为CH4,则相对分子质量最小的Y是乙二醇 | |
| D. | X、Y的化学式应含有相同的氢原子数,且相差n个碳原子,同时相差2n个氧原子(n为正整数) |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com