
| A. | ①②⑤ | B. | ②④ | C. | ②④⑥ | D. | ③⑤⑥ |
分析 ①无色溶液中不存在有色的铜离子;
②pH=11的溶液中存在大量氢氧根离子,四种离子之间不反应,都不与企业广告离子反应;
③加入Al能放出H2的溶液中存在大量氢离子或氢氧根离子,碳酸氢根离子、铵根离子与氢氧根离子反应,碳酸氢根离子还与氢离子反应;
④在由水电离出的c(OH-)=10-13mol•L-1的溶液中存在大量氢离子或氢氧根离子,四种离子之间不反应,都不与氢离子、氢氧根离子反应;
⑤能使红色石蕊试纸变为蓝色的溶液中存在大量氢氧根离子,碳酸氢根离子与氢氧根离子反应;
⑥酸性溶液中,Fe2+、NO3-发生氧化还原反应.
解答 解:①无色溶液中不能存在有色的Cu2+,故①错误;
②pH=11的溶液呈碱性,CO32-、Na+、AlO2-、NO3-之间不反应,都不与氢氧根离子反应,在溶液中能够大量共存,故②正确;
③加入Al能放出H2的溶液呈酸性或强碱性,HCO3-与氢离子反应,HCO3-、NH4+与氢氧根离子反应,在溶液中不能大量共存,故③错误;
④在由水电离出的c(OH-)=10-13mol•L-1的溶液呈酸性或碱性,Na+、Ba2+、Cl-、I-之间不反应,都不与氢离子、氢氧根离子反应,在溶液中能够大量共存,故④正确;
⑤能使红色石蕊试纸变为蓝色的溶液呈碱性,溶液中存在大量氢氧根离子,HCO3-与氢氧根离子反应,在溶液中不能大量共存,故⑤错误;
⑥酸性溶液中,NO3-具有强氧化性,能够氧化Fe2+,在溶液中不能大量共存,故⑥错误;
故选B.
点评 本题考查离子共存的正误判断,为高考的高频题,题目难度中等,注意明确离子不能大量共存的一般情况:能发生复分解反应的离子之间;能发生氧化还原反应的离子之间等;还应该注意题目所隐含的条件,如:溶液的酸碱性,据此来判断溶液中是否有大量的 H+或OH-;溶液的颜色,如无色时可排除 Cu2+、Fe2+、Fe3+、MnO4-等有色离子的存在;溶液的具体反应条件,如“氧化还原反应”、“加入铝粉产生氢气”等.


科目:高中化学 来源: 题型:推断题
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
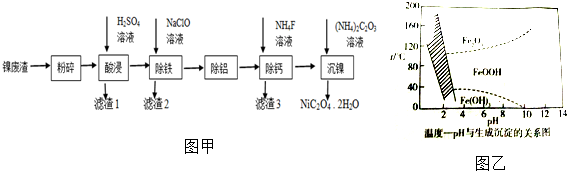
查看答案和解析>>
科目:高中化学 来源: 题型:实验题
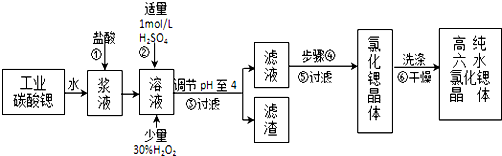
| 氢氧化物 | Fe(OH)3 | Fe(OH)2 |
| 开始沉淀的pH | 1.5 | 6.5 |
| 沉淀完全的pH | 3.7 | 9.7 |
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
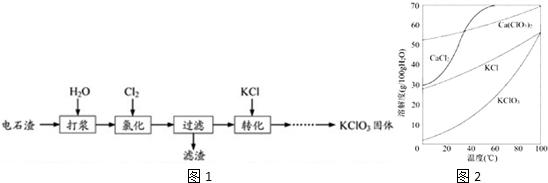
查看答案和解析>>
科目:高中化学 来源: 题型:实验题
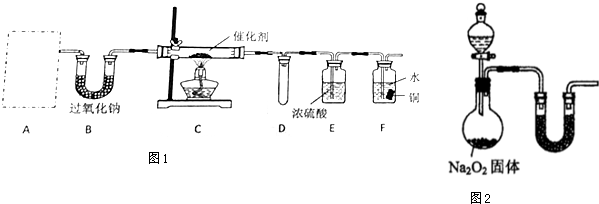
查看答案和解析>>
科目:高中化学 来源: 题型:实验题
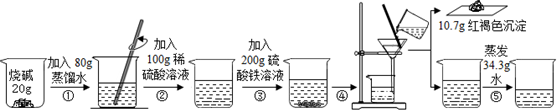
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | ①②③④ | B. | ②③④① | C. | ②①③④ | D. | ④②③① |
查看答案和解析>>
科目:高中化学 来源: 题型:多选题
| A. | 氨水稀释后,溶液中$\frac{c(N{H}_{4}^{+})}{c(N{H}_{3}•{H}_{2}O)}$的值减小 | |
| B. | 0.1 mol•L-1Na2CO3溶液加蒸馏水稀释,CO32-的水解程度增大,溶液的pH减小 | |
| C. | 电解精炼铜过程中,阳极质量的减少与阴极质量的增加一定相等 | |
| D. | 298 K时,2H2S(g)+SO2(g)═3S(s)+2H2O(l)能自发进行,则其△H<0 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com