
| 实验步骤 | 预期现象和结论 |
| | |
科目:高中化学 来源:不详 题型:实验题
 酸酸化的BaCl2溶液,只观察到有白色沉淀生成。
酸酸化的BaCl2溶液,只观察到有白色沉淀生成。 沉淀的量的关系如图所示:
沉淀的量的关系如图所示: 试问:
试问:| 物 质 | 燃烧热(kJ·mol-1) |
| H2(g) | -285.8 |
| CO(g) | -283.0 |
| CH4(g) | -890.3 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:实验题
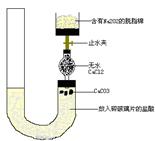
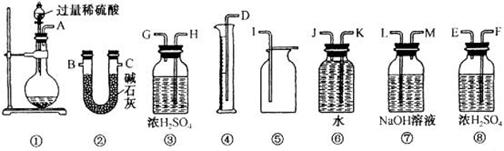
 的连接顺序 。
的连接顺序 。  。
。查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| A.用结晶法从水溶液中获得氯化铁晶体 |
| B.用纸上层析法检验氯化铁溶液中是否混有少量氯化铜 |
| C.为准确测定盐酸与NaOH溶液反应的中和热,所用酸和碱的物质的量必需相等 |
| D.用AgNO3溶液、稀硝酸鉴别亚硝酸钠和食盐 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
A.现向K2Cr2O7溶液中加入少量氢氧化钠,溶液变为黄色,证明溶液中存在着平衡:Cr2O72-+H2O 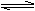 2CrO42-+2H+ 2CrO42-+2H+ |
| B.CH2=CH-CHO能使酸性高锰酸钾溶液褪色,证明该分子中一定含有碳碳双键 |
| C.用相互滴加的方法不能鉴别NaCl、AlCl3、Na2CO3、NaHSO4四种无色溶液 |
| D.SO2通入Ba(NO3)2溶液中出现白色沉淀,证明BaSO3不溶于水 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
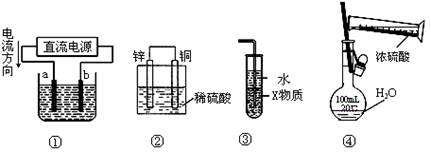
| A.若采用装置①精炼铜,则a极为纯铜,b极为粗铜,电解质溶液为CuSO4溶液 |
| B.装置②是原电池,工作时SO42-离子向铜极移动 |
| C.装置③中X若为四氯化碳,则此装置可用于吸收氨气,并防止倒吸 |
| D.装置④可用于实验室配置一定物质的量浓度的稀硫酸 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:实验题
 。
。 _____。
_____。| A.该学生在量取浓硫酸时,俯视刻度线 |
| B.称量固体NaOH时,将砝码和物品的位置颠倒(没有使用游码) |
C.溶解H2SO4操作时没有冷却至室温就立即完成后面的配制操 作。 作。 |
D.在烧杯中溶解 搅拌时,溅出少量溶液 搅拌时,溅出少量溶液 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:实验题
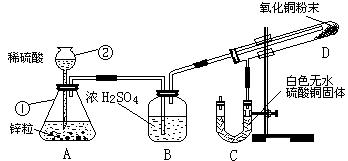
 ⑴写出编号仪器的名称:②
⑴写出编号仪器的名称:② 查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| 选项 | 实验操作 | 实验目的或结论 |
| A | 向含有少量FeCl3的MgCl2溶液中加入足量Mg(OH)2粉末,搅拦一段时间后过滤 | 除去MgCl2溶液中少量FeCl3 |
| B | 向某溶液中加入BaCl2溶液生成白色沉淀,继续加稀硝酸沉淀不消失 | 证明溶液中含SO42- |
| C | 向某溶液中加入稀盐酸,放出无色无味气体,将气体通入澄清石灰水,石灰水变浑浊 | 证明该溶液中存在CO32- |
| D | 向0.1mol·L-1FeSO4溶液中滴加少量酸性KMnO4溶液,KMnO4溶液褪色 | 证明Fe2+具有氧化性 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com