
 C�ֱ������ֲ�ͬʵ�������½��У����ǵ���ʼŨ�Ⱦ�Ϊc(A)="0.100" mol��L-1c(B)="0.200" mol��L-1 c(C)="0" mol��L-1����Ӧ��A��Ũ����ʱ��ı仯����ͼ��ʾ��
C�ֱ������ֲ�ͬʵ�������½��У����ǵ���ʼŨ�Ⱦ�Ϊc(A)="0.100" mol��L-1c(B)="0.200" mol��L-1 c(C)="0" mol��L-1����Ӧ��A��Ũ����ʱ��ı仯����ͼ��ʾ��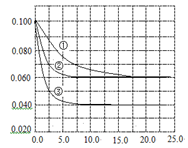
 C�ġ�H��0
C�ġ�H��0


| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ������ ���ͣ���ѡ��
 2C��g�� ��2���ӷ�Ӧ�ﵽƽ�⣬��ʱ����0.2mol C��
2C��g�� ��2���ӷ�Ӧ�ﵽƽ�⣬��ʱ����0.2mol C��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ������ ���ͣ���ѡ��
 ClF3(g)����H<0�����������У���ȷ����
ClF3(g)����H<0�����������У���ȷ����| A�����º���ʱ����ClF ת��40% ʱ�������ڵ�ѹǿΪ��ʼʱ��0.6 �� |
| B���� c(F2):c (ClF): c (ClF3) ="1:" 1: 1����Ӧһ���ﵽƽ��״̬ |
| C���ﵽƽ��������������ݻ���������Ӧ���ʼ�С���淴Ӧ��������ƽ������ |
| D��ƽ����ٽ����¶ȣ����ֺ��ݣ��ﵽ�µ�ƽ�⣬���������ƽ��Ħ���������� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ������ ���ͣ���ѡ��
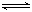 3C��g����2D��g����(bΪ
3C��g����2D��g����(bΪ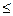 3��������) ��
3��������) ��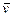 ��B���� ��
��B���� ��| t�� | 700 | 800 | 830 | 1000 | 1200 |
| K | 0.6 | 0.9 | 1.0 | 1.7 | 2.6 |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ������ ���ͣ������
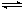 2NH3����ƽ���÷�Ӧ�ų�������Ϊ18.4 kJ����������ܵ����ʵ���Ϊ3.6 mol�������ڵ�ѹǿ��Ϊԭ����90%����֪N2��H2��ת������ͬ��
2NH3����ƽ���÷�Ӧ�ų�������Ϊ18.4 kJ����������ܵ����ʵ���Ϊ3.6 mol�������ڵ�ѹǿ��Ϊԭ����90%����֪N2��H2��ת������ͬ�� ��
�� ��ƽ����ȫ��ͬ��
��ƽ����ȫ��ͬ���鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ������ ���ͣ������
 CH3OH(g)��H2O(g) ��H����49.0kJ/mol��Ϊ̽����Ӧԭ�����ֽ�������ʵ�飺
CH3OH(g)��H2O(g) ��H����49.0kJ/mol��Ϊ̽����Ӧԭ�����ֽ�������ʵ�飺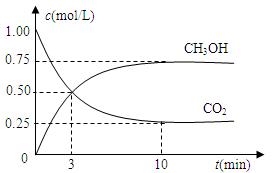
A�������¶� | B������He(g)��ʹ��ϵѹǿ���� |
| C����H2O(g)����ϵ�з��� | D���ٳ���1 mol CO2��4 mol H2 |
 mol CH3OH��1 mol H2O��Ϊ��ʹ��Ӧ�ﵽ�Ļ�ѧƽ�������һ��������ʼ�������H2�����ʵ���Ϊ ��
mol CH3OH��1 mol H2O��Ϊ��ʹ��Ӧ�ﵽ�Ļ�ѧƽ�������һ��������ʼ�������H2�����ʵ���Ϊ ���鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ������ ���ͣ���ѡ��
 2SO3���ڻ�����г���һ������18Oԭ�ӣ��ﵽƽ���Ժ�18Oԭ��
2SO3���ڻ�����г���һ������18Oԭ�ӣ��ﵽƽ���Ժ�18Oԭ��| A��ֻ������O2�С� | B��ֻ������O2��SO2�� |
C��ֻ������O2��S O3�� O3�� | D��������O2��SO2��SO3�� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ������ ���ͣ���ѡ��
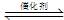 CH3OH��g����T1��T2�¶��£�CH3OH�����ʵ�������ʱ��ı仯��ϵ����ͼ��ʾ�������й�˵����ȷ����
CH3OH��g����T1��T2�¶��£�CH3OH�����ʵ�������ʱ��ı仯��ϵ����ͼ��ʾ�������й�˵����ȷ����
| A��T1>T2 |
| B��K(T1)>K(T2) |
| C��T1�¶��´ﵽƽ����ٳ���һ����CO��CO��ת�������� |
| D��T2�¶��£�0~10min��v(H2)=0.06mol��L-1��min-1 |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ������ ���ͣ������

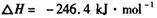
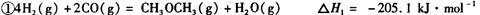
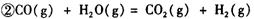
 ��__________________ ______________
��__________________ ______________ 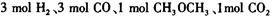 ����һ���¶Ⱥ�ѹǿ�·�����Ӧ��
����һ���¶Ⱥ�ѹǿ�·�����Ӧ��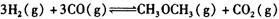 ����һ��ʱ��ﵽƽ�⣬�����ƽ��ʱ��������ܶ���ͬ��ͬѹ����ʼʱ��1.6�����ʣ��ٷ�Ӧ��ʼʱ�����淴Ӧ����
����һ��ʱ��ﵽƽ�⣬�����ƽ��ʱ��������ܶ���ͬ��ͬѹ����ʼʱ��1.6�����ʣ��ٷ�Ӧ��ʼʱ�����淴Ӧ���� �Ĵ�С��V(����____V���棩��� >������ < ����"="),�����ǣ�________________________________
�Ĵ�С��V(����____V���棩��� >������ < ����"="),�����ǣ�________________________________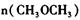 =_________________��ƽ��ʱCO��ת����= _________________��
=_________________��ƽ��ʱCO��ת����= _________________���鿴�𰸺ͽ���>>
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com