
 ,X在一定条件下能发生的反应是acd(选填字母);
,X在一定条件下能发生的反应是acd(选填字母); )能与化合物Y在一定条件发生取代反应生成X与乙酸,该反应的化学方程式是
)能与化合物Y在一定条件发生取代反应生成X与乙酸,该反应的化学方程式是 ;
; ②苯环上的一溴代物只有两种
②苯环上的一溴代物只有两种 :
: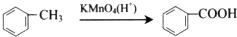
 .
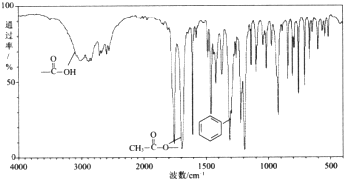
. 分析 (1)有机物X分子式为C9H8O4,结合其红外光谱图可知,X含有苯环、-OOCCH3、-COOH,核磁共振氢谱图峰面积比是1:1:1:1:1:3,故X为 ;
;
(2)邻羟基苯甲酸( )能与化合物Y在一定条件发生取代反应生成X与乙酸,则Y为乙酸酐;
)能与化合物Y在一定条件发生取代反应生成X与乙酸,则Y为乙酸酐;
(3)有关扑热息痛的信息如下:①分子中含有基团 ,②苯环上的一溴代物只有两种,③能和浓溴水反应生成白色沉淀,含有酚羟基,④能发生水解反应生成乙酸,结合①可知含有-NHCOCH3,结合②可知,-OH与-NHCOCH3处于对位;
,②苯环上的一溴代物只有两种,③能和浓溴水反应生成白色沉淀,含有酚羟基,④能发生水解反应生成乙酸,结合①可知含有-NHCOCH3,结合②可知,-OH与-NHCOCH3处于对位;
(4)邻甲基苯酚与乙酸酐反应得到W,然后在用酸性高锰酸钾溶液氧化得到X.
解答 解:(1)有机物X分子式为C9H8O4,结合其红外光谱图可知,X含有苯环、-OOCCH3、-COOH,核磁共振氢谱图峰面积比是1:1:1:1:1:3,故X为 ,可以发生加成反应、酯化反应、水解反应,不能发生消去反应,
,可以发生加成反应、酯化反应、水解反应,不能发生消去反应,
故答案为: ;acd;
;acd;
(2)邻羟基苯甲酸( )能与化合物Y在一定条件发生取代反应生成X与乙酸,则Y为乙酸酐,反应方程式为:
)能与化合物Y在一定条件发生取代反应生成X与乙酸,则Y为乙酸酐,反应方程式为: ,
,
故答案为: ;
;
(3)有关扑热息痛的信息如下:①分子中含有基团 ,②苯环上的一溴代物只有两种,③能和浓溴水反应生成白色沉淀,含有酚羟基,④能发生水解反应生成乙酸,结合①可知含有-NHCOCH3,结合②可知,-OH与-NHCOCH3处于对位,扑热息痛的结构简式是:
,②苯环上的一溴代物只有两种,③能和浓溴水反应生成白色沉淀,含有酚羟基,④能发生水解反应生成乙酸,结合①可知含有-NHCOCH3,结合②可知,-OH与-NHCOCH3处于对位,扑热息痛的结构简式是: ,
,
故答案为: ;
;
(4)邻甲基苯酚与乙酸酐反应得到W,然后在用酸性高锰酸钾溶液氧化得到X,则W的结构简式为: ,
,
故答案为: .
.
点评 本题考查有机物的推断与合成,侧重考查学生分析推理能力,难度中等.


科目:高中化学 来源: 题型:选择题
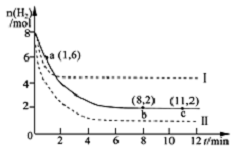 工业上可用CO2生产甲醇,反应为:CO2(g)+3H2(g)?CH3OH(g)+H2O(g).将6molCO2和8mol H2充入2L的密闭容器中,测得H2的物质的量随时间变化如图实线所示.图中虚线表示仅改变某一反应条件时,H2物质的量随时间的变化.下列说法正确的是( )
工业上可用CO2生产甲醇,反应为:CO2(g)+3H2(g)?CH3OH(g)+H2O(g).将6molCO2和8mol H2充入2L的密闭容器中,测得H2的物质的量随时间变化如图实线所示.图中虚线表示仅改变某一反应条件时,H2物质的量随时间的变化.下列说法正确的是( )| A. | 反应开始至a点时v(H2)=2mol•L-1•min-1 | |
| B. | 若曲线I对应的条件改变是升高温度,则该反应△H>0 | |
| C. | 曲线II对应的条件改变是降低压强 | |
| D. | 保持温度不变,若将平衡后的容器体积缩小至1L,重新达平衡时则2 mol•L-1<c(CH3OH)<8/3 mol•L-1 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 回收其中的石墨电极 | |
| B. | 回收利用电池外壳的金属材料 | |
| C. | 不使电池中渗露的电解液腐蚀其他物品 | |
| D. | 防止电池中汞、镉和铅等重金属离子对土壤和水源的污染 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 2s | B. | 2 min | C. | 3s | D. | 3 min |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题

查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | Na+、H+、Cu2+、NO3- | B. | Na+、Fe2+、H+、NO3- | ||
| C. | NH4+、Cl-、SO42-、OH- | D. | HCO3-、Mg2+、Na+、OH- |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com