
分析 ①光导纤维的主要成分是二氧化锆晶体,所以SiO2可以制光导纤维;
②CO2与CaCl2不反应,据此进行判断;
③冰是水,干冰是二氧化碳,都是由一种物质组成的,并且都是由不同种元素组成的纯净物;
④Cl2、Na2O2、H2O2等氧化性;SO2与品红发生化合反应褪色;
⑤盐酸是氯化氢的水溶液;
⑥MgCl2、AlCl3、FeCl3溶液,阴离子相同,阳离子不同,分别与NaOH反应的现象为:白色沉淀、生成白色沉淀后溶解、红褐色沉淀;
⑦豆浆是固溶胶、雾是气溶胶;
⑧利用丁达尔效应可以区分溶液和胶体.
解答 解:①光导纤维的主要成分是二氧化锆晶体,所以SiO2可以制光导纤维,故错误;
②CO2与CaCl2不反应,所以不会出现浑浊,故错误;
③冰是水,干冰是二氧化碳,它们在一起是属于混合物,故错误;
④Cl2、Na2O2、H2O2等氧化性;SO2与品红发生化合反应褪色,所以不一定是二氧化硫,故错误;
⑤盐酸是氯化氢的水溶液,是混合物,故错误;
⑥MgCl2、AlCl3、FeCl3溶液,阴离子相同,阳离子不同,分别与NaOH反应的现象为:白色沉淀、生成白色沉淀后溶解、红褐色沉淀,所以现象不同,故正确;
⑦豆浆是固溶胶、雾是气溶胶,都是胶体,故正确;
⑧利用丁达尔效应可以区分溶液和胶体,故正确;
故答案为:⑥⑦⑧.
点评 本题考查了常见物质的组成、性质和应用,熟悉物质的组成是解答本题的关键.


 名师指导期末冲刺卷系列答案
名师指导期末冲刺卷系列答案 开心蛙口算题卡系列答案
开心蛙口算题卡系列答案科目:高中化学 来源: 题型:解答题
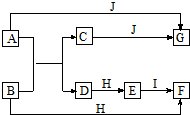
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | Al3+、K+、Cl-、AlO2- | B. | Al3+、Na+、NO3-、HCO3- | ||
| C. | NH4+、Fe2+、SO42-、NO3- | D. | Ca2+、H+、NO3-、S2O32- |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题

| A. | 用浓盐酸和MnO2反应制取Cl2 | |
| B. | 用浓硫酸与Na2SO3反应制取SO2 | |
| C. | 用H2O2溶液和MnO2反应制取O2 | |
| D. | 用NH4Cl浓溶液和Ca(OH)2浓溶液反应制取NH3 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 标准状况下,22.4L乙醇的分子数为NA | |
| B. | 1mol甲基中含有的电子数为10NA | |
| C. | 13g乙炔和苯的混合气体中含有原子总数为2NA | |
| D. | 1L 0.1mol•L-1乙酸溶液中H+数目为0.1NA |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 将Na2O与Na2O2分别加入滴有酚酞的水中,二者现象相同 | |
| B. | 在Na2O2与水的反应中,氧化产物与还原产物物质的量之比为1:4 | |
| C. | 相同物质的量的氧化钠和过氧化钠中阴离子物质的量之比为1:1 | |
| D. | 等质量的Na2O与Na2O2投入等量且足量水中充分反应后所得溶液物质的量浓度相等 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
 $\frac{\underline{\;[O]\;}}{\;}$
$\frac{\underline{\;[O]\;}}{\;}$ +
+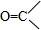
 +H2O→
+H2O→ +HCl
+HCl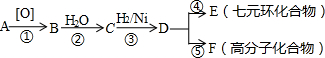
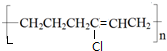 、BOHCCH2CH2CH2CH2COCl、EOHCCH2CH2CH2CH2COOH
、BOHCCH2CH2CH2CH2COCl、EOHCCH2CH2CH2CH2COOH +nH2O,缩聚反应.
+nH2O,缩聚反应.查看答案和解析>>
科目:高中化学 来源: 题型:选择题

| A. | 曲线①代表0.1 mol/L KOH溶液滴定HC1溶液的滴定曲线,曲线②代表0.1 mol/LKOH溶液滴定CH3COOH溶液的滴定曲线 | |
| B. | 在相同温度下,C点水电离的c(H+)等于A点水电离的c(H+) | |
| C. | 在A点的溶液中有:c(CH3COO-)+c(OH-)-c(H+)=0.1 mol/L | |
| D. | 在B点的溶液中有:c(K+)>c(OH-)>c(CH3COO-)>c(H+) |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com