
【题目】【2017陕西黄陵】 磷及其化合物在生产、生活中有重要的用途。回答下列问题:
(1)直链聚磷酸是由n个磷酸分子通过分子间脱水形成的,常用于制取阻燃剂聚磷酸铵。
①写出磷酸主要的电离方程式 。
②直链低聚磷酸铵的化学式可表示为(NH4)(n+2)PnOx,x= (用n表示)。
(2)在碱性条件下,次磷酸盐可用于化学镀银,完成其反应的离子方程式。
□H2PO2-+□Ag+ + □ = □PO43-+ □Ag +□
(3)由工业白磷(含少量砷、铁、镁等)制备高纯白磷(熔点44℃,沸点280℃),主要生产流程如下
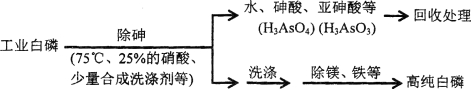
①除砷过程在75℃下进行,其合理的原因是_______(填字母)。
a.温度不宜过高,防止硝酸分解 b.适当提高温度,加快化学反应速率
c.使白磷熔化,并溶于水 d.降低白磷的毒性
②硝酸氧化除砷时被还原为NO,若氧化产物为等物质的量的亚砷酸与砷酸,则化学反应方程式为____________________________
【答案】(10分)(1)①H3PO4![]() H++ H2PO4- (2分) ②3n+1(2分)
H++ H2PO4- (2分) ②3n+1(2分)
(2)H2PO2-+ 4Ag++ 6OH- = PO43- + 4Ag + 4H2O(2分)
(3)①cd (2分) ② 8HNO3+6As+5H2O= 3H3AsO4+3H3AsO3+8NO↑(2分)
【解析】(1)①H3PO4是三元弱酸,其电离是逐步进行的,主要是第一步电离,磷酸主要的电离方程式是H3PO4![]() H++H2PO4-;②在磷酸通过分子间脱水形成直链聚磷酸中,n越大,分子中含有的羟基就越少,得到的直链聚磷酸铵的水溶性越小;(2)该反应是氧化还原反应,同时也是离子反应,根据电子守恒、电荷守恒及原子守恒,可得反应的方程式是:H2PO2-+4Ag++6OH-=PO43-+4Ag+4H2O。(3) ①除砷过程在75 ℃下进行,其合理的原因是使白磷熔化,提高反应活性;适当提高温度,增大反应速率;温度不宜过高,防止硝酸分解,所以选项是acd。②生产过程在高纯氮气保护下进行,原因是白磷非常活泼,容易与空气中的氧气发生反应;在氮气的环境中,其目的是防止白磷被空气中氧气氧化;③除砷过程中,合成洗涤剂起到乳化作用。④硝酸氧化除砷时被还原为NO,砷被氧化为砷酸,根据电子守恒、原子守恒,可得砷转化为砷酸的化学方程式:3As+5HNO3+2H2O=3H3AsO4+5NO↑;氧化相同质量的砷,当转化为亚砷酸的量越多,得到的电子就越少,则反应消耗硝酸的量越少;⑤根据图示可知,砷的脱除率从a点到b点降低,原因是硝酸浓度变大,氧化性增强,有较多的硝酸用于氧化白磷,脱砷率降低。
H++H2PO4-;②在磷酸通过分子间脱水形成直链聚磷酸中,n越大,分子中含有的羟基就越少,得到的直链聚磷酸铵的水溶性越小;(2)该反应是氧化还原反应,同时也是离子反应,根据电子守恒、电荷守恒及原子守恒,可得反应的方程式是:H2PO2-+4Ag++6OH-=PO43-+4Ag+4H2O。(3) ①除砷过程在75 ℃下进行,其合理的原因是使白磷熔化,提高反应活性;适当提高温度,增大反应速率;温度不宜过高,防止硝酸分解,所以选项是acd。②生产过程在高纯氮气保护下进行,原因是白磷非常活泼,容易与空气中的氧气发生反应;在氮气的环境中,其目的是防止白磷被空气中氧气氧化;③除砷过程中,合成洗涤剂起到乳化作用。④硝酸氧化除砷时被还原为NO,砷被氧化为砷酸,根据电子守恒、原子守恒,可得砷转化为砷酸的化学方程式:3As+5HNO3+2H2O=3H3AsO4+5NO↑;氧化相同质量的砷,当转化为亚砷酸的量越多,得到的电子就越少,则反应消耗硝酸的量越少;⑤根据图示可知,砷的脱除率从a点到b点降低,原因是硝酸浓度变大,氧化性增强,有较多的硝酸用于氧化白磷,脱砷率降低。


 阅读快车系列答案
阅读快车系列答案科目:高中化学 来源: 题型:
【题目】几种相邻主族短周期元素的相对位置如表,元素X的原子核外电子数是M的2倍,Y的氧化物具有两性。下列说法不正确的是
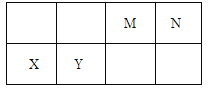
A. 元素的第一电离能X<Y
B. X位于第三周期IIA ,其单质可采用电解熔融其氯代物制备
C. 元素最高价氧化物的水化物中,酸性最强的是HNO3
D. 气体分子(MN)2的电子式为![]()
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】设阿伏加德罗常数为6.02×1023mol﹣1 . 关于1mol H2O的叙述正确的是( )
A.含有1mol H2
B.含有6.02×1023个水分子
C.质量为18 g/mol
D.在标准状况下的体积为22.4 L
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列各组中的离子,能在溶液中大量共存的是
A.Fe3+、Na+、Cl-、OH-
B.Fe3+、Cl-、K+、Ca2+
C.Cl-、Ca2+、Mg2+、CO32-
D.Ba2+、K+、CO32-、Cl-
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列物质在常温下发生水解时,对应的离子方程式正确的是( )
①Na2CO3:CO32-+2H2O![]() H2O+CO2↑+2OH-
H2O+CO2↑+2OH-
②NH4Cl:NH4++H2O![]() NH3·H2O+H+
NH3·H2O+H+
③CuSO4:Cu2++2H2O![]() Cu(OH)2+2H+
Cu(OH)2+2H+
④NaF:F-+H2O![]() HF+OH-
HF+OH-
A.①④ B.②③ C.①③ D.②④
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列现象中,是因为发生加成反应而产生的现象是( )
A. 乙烯使酸性高锰酸钾溶液褪色
B. 将苯滴入溴水中,振荡后水层接近无色
C. 乙烯使溴的四氯化碳溶液褪色
D. 甲烷与氯气混合,光照一段时间后黄绿色消失
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】硫酸锶(SrSO4)在水中的沉淀溶解平衡曲线如图所示。下列说法正确的是
A. 温度一定时,Ksp(SrSO4)随c(SO42—)的增大而减小
B. 三个不同温度中,313 K时Ksp(SrSO4)最大
C. 283 K时,图中a点对应的溶液是饱和溶液
D. 283 K下的SrSO4饱和溶液升温到363 K后变为不饱和溶液
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列图示与对应的叙述相符的是( )
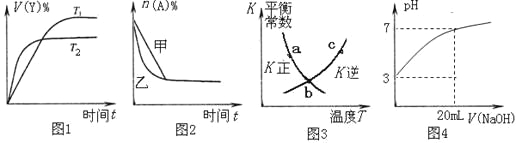
A. 图1表示可逆反应“2X(g)![]() Y(g)△H<0”温度T1<T2的情形
Y(g)△H<0”温度T1<T2的情形
B. 图2表示压强对可逆反应2A(g)+2B(g)![]() 3C(g)+D(s)的影响,乙的压强比甲的压强大
3C(g)+D(s)的影响,乙的压强比甲的压强大
C. 图3中a、b、c三点中只有b点已经达到化学平衡状态
D. 图4是向20 mL pH =3的醋酸溶液中滴加pH=11的NaOH溶液过程中pH变化曲线
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com