���㣺ת�������¶ȡ�ѹǿ�ı仯����,�Ȼ�ѧ����ʽ,��ѧƽ���Ӱ������,���������ˮ��Һ�еĵ���ƽ��
ר�⣺���ʵ����ר��
��������1����i����ͼ��֪��ѹǿһ��ʱ�����¶����ߣ�CO��ת���ʽ��ͣ��������¶�ƽ�����淴Ӧ�ƶ����ݴ��жϣ�
��ii����ѧƽ�ⳣ��K=
������CO��ת���ʣ���������ʽ�����ƽ��ʱ����ֵ����ʵ������������ƽ��ʱ����ֵ�Ũ�ȣ�����ƽ�ⳣ�����㣻
���淴Ӧ��ƽ�ⳣ��Խ��˵����Ӧ���еij̶�Խ����˵����Ӧ���ʿ���������˵���÷�Ӧ��ͨ��������һ�����Է���������˵����Ӧ�����Ȼ��Ƿ��ȣ�
��iii�����¶Ⱥ��ݻ����������£�����ƽ����ϵ�г���a mol CO��g����2a mol H
2��g������ЧΪ��ԭƽ��Ļ���������һ��ѹǿ��ƽ��������Ӧ�ƶ���
��ѧƽ�ⳣ��ֻ���¶�Ӱ�죬��Ũ���أ��¶Ȳ��䣬ƽ�ⳣ�����䣻
��iv������μӷ�Ӧ��CO�����ʵ��������ò���������ƽ��ʱ��Ӧ���������ʵ����仯������������ƽ��ʱ�ܵ����ʵ��������ú��º����£�ѹǿ֮�ȵ������ʵ���֮�Ƚ��
��2�����ݸ�˹������дĿ���Ȼ�ѧ����ʽ��
��3���ٸ��ݵ���غ��֪��c��NH
4+��+c��H
+��=c��Cl
-��+c��OH
-��������c��NH
4+����c��Cl
-������c��H
+����c��OH
-������Һ�����ԣ��ݴ˽��ѡ���жϣ�
����Һ�д���ƽ��NH
3��H
2O?NH
4++OH
-�����ݵ���غ������Һ��pHֵ������������Һ��c��OH
-��������������Ũ�ȼ���c��NH
4+�������������غ������Һ��c��NH
3��H
2O��������NH
3?H
2O�ĵ��볣������ʽ���㣮
���
�⣺��1����i����ͼ��֪��ѹǿһ��ʱ�����¶����ߣ�CO��ת���ʽ��ͣ��������¶�ƽ�����淴Ӧ�ƶ���������ӦΪ���ȷ�Ӧ��
�ʴ�Ϊ�����ȣ�
��2��100�棬ƽ��ʱCO��ת����Ϊ0.5�����Բμӷ�Ӧ��CO�����ʵ���Ϊ0.5amol��
CO��g��+2H
2��g��
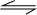
CH
3OH��g����
��ʼ��mol����a 2a 0
�仯��mol����0.5a a 0.5a
ƽ�⣨mol����0.5a a 0.5a
����ƽ��ʱ��CO��Ũ��Ϊ
=
mol/L��H
2��Ũ��Ϊ
=
mol/L��CH
3OH��Ũ��Ϊ
=
mol/L��100��ʱ�÷�Ӧ��ƽ�ⳣ��k�T
=
��
a�����淴Ӧ��ƽ�ⳣ���ܴ�˵����Ӧ���еij̶Ⱥܴ���˵���÷�Ӧ��ͨ��������һ�����Է������÷�Ӧ������Ҫ�����ſ��Խ��У���a����
b�����淴Ӧ��ƽ�ⳣ���ܴ�˵����Ӧ���еij̶Ⱥܴ���˵���������·�Ӧ���ʺܿ죬��b����
c�����淴Ӧ��ƽ�ⳣ���ܴ�˵����Ӧ���еij̶Ⱥܴ�Ӧ��ƽ��ʱ������һ�ַ�Ӧ��İٷֺ�����С����c��ȷ��
d�����淴Ӧ��ƽ�ⳣ���ܴ�˵����Ӧ���еij̶Ⱥܴ���˵���÷�Ӧ�����Ȼ��Ƿ��ȣ���d����
�ʴ�Ϊ��
��c��
��iii�����¶Ⱥ��ݻ����������£�����ƽ����ϵ�г���a mol CO��g����2a mol H
2��g������ЧΪ��ԭƽ��Ļ���������һ��ѹǿ��ƽ��������Ӧ�ƶ���CO��ת��������ѧƽ�ⳣ��ֻ���¶�Ӱ�죬��Ũ���أ��¶Ȳ��䣬ƽ�ⳣ�����䣬
�ʴ�Ϊ�������䣻
��iv���μӷ�Ӧ��CO�����ʵ���Ϊ2.5mol��90%=2.25mol����
CO��g��+2H
2��g��?CH
3OH��g�� ���ʵ������١�n
1 2
2.25mol 4.5mol
��ƽ��ʱ�ܵ����ʵ���Ϊ2.5mol+7.5mol-4.5mol=5.5mol�����º�����ѹǿ֮�ȵ������ʵ���֮�ȣ���ƽ��ʱ������ѹǿΪ��ʼʱѹǿ��
=0.55����
�ʴ�Ϊ��0.55��
��2����֪����CH
4��g��+2O
2��g���TCO
2��g��+2H
2O��l����H
1=-890.3kJ?mol
-1��H
2��g��+
O
2��g���TH
2O��l����H
2=-285.8kJ?mol
-1��
���ø�˹���ɣ����ڡ�4-�ٿɵã�CO
2��g��+4H
2��g��=CH
4��g��+2H
2O��l����H=4����-285.8kJ?mol
-1��-��-890.3kJ?mol
-1��=-252.9kJ?mol
-1��
�ʴ�Ϊ��CO
2��g��+4H
2��g��=CH
4��g��+2H
2O��l����H=-252.9kJ?mol
-1��
��5���ٸ��ݵ���غ��֪��c��NH
4+��+c��H
+��=c��Cl
-��+c��OH
-��������c��NH
4+����c��Cl
-������c��H
+����c��OH
-������Һ�����ԣ�
a������㣬��ˮʣ�࣬Ϊ�Ȼ���백ˮ�Ļ����Һ��笠�����ˮ��̶ȴ��ڰ�ˮ�ĵ���ʱ����Һ���ܳ����ԣ���a���ܣ�
b����ˮ������ǡ����ȫ��Ӧ��Ϊ�Ȼ����Һ��笠�����ˮ�⣬��Һ�����ԣ���b���ܣ�
c�������������ҺΪ�Ȼ�李�����Ļ����Һ����Һ�����ԣ���c���ܣ�
��ѡ��abc��
�ڸ��ݵ���غ���c��NH
4+��+c��H
+��=c��Cl
-��+c��OH
-��������c��NH
4+��=c��Cl
-������c��H
+��=c��OH
-������Һ�����ԣ�����Һ��c��OH
-��=10
-7mol/L����Һ��c��NH
4+��=c��Cl
-��=
��0.1mol?L
-1=0.05mol?L
-1���ʻ�Ϻ���Һ��c��NH
3��H
2O��=
��amol?L
-1-0.05mol?L
-1=��0.5a-0.05��mol/L��NH
3?H
2O�ĵ��볣��K
b=
=
��
�ʴ�Ϊ��
��
���������⿼�黯ѧƽ��ͼ��ѧƽ���йؼ��㡢��ѧƽ�ⳣ����Ӱ�컯ѧƽ������ء��Ȼ�ѧ����ʽ��д����Һ������жϡ�����ƽ�ⳣ������ȣ��Ƕ�֪ʶ���ۺ����ã���5����ע������Ũ�ȵļ��㣬Ӧ��ǿƽʱ֪ʶ�Ļ��ۣ��Ѷ��еȣ�

 �о��Ϳ���CO2��CO�Ĵ��������ǻ�����������Դ���õ�˫Ӯ�Ŀ��⣮
�о��Ϳ���CO2��CO�Ĵ��������ǻ�����������Դ���õ�˫Ӯ�Ŀ��⣮ CH3OH��g����
CH3OH��g����

 ȫ�ܲ����ĩС״Ԫϵ�д�
ȫ�ܲ����ĩС״Ԫϵ�д�




 SO2��NOx�ڻ�ѧ��ҵ������Ҫ��;��Ҳ�Ǵ�����Ⱦ����Ҫ��Դ�����������ò��أ�Ԥ�������������ǵ�ǰ��ҵ�Ϻͻ������������о�����Ҫ����֮һ��
SO2��NOx�ڻ�ѧ��ҵ������Ҫ��;��Ҳ�Ǵ�����Ⱦ����Ҫ��Դ�����������ò��أ�Ԥ�������������ǵ�ǰ��ҵ�Ϻͻ������������о�����Ҫ����֮һ��