
����Ŀ����������[Ce(OH)4]��һ����Ҫ��ϡ��������Է�̼���(��Ҫ��CeFCO3)Ϊԭ���Ʊ�Ce(OH)4��һ�ֹ����������£�
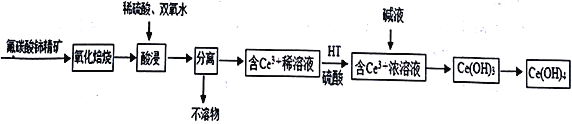
��֪����������Һ��Ce4+��ǿ�����ԡ��ش�����������
��1�� ������������ǰ�轫��ʯ�����ϸ��������Ŀ����_________________________��������CeFCO3 ��Ce �Ļ��ϼ�Ϊ________________________��
��2�������������ɵ��滯����Ϊ��������(CeO2)���������ʱ������Ӧ�����ӷ���ʽΪ__________________________________�����ʱ�����¶ȹ��ߵ�ԭ����____________________��
��3����֪�л���HT �ܽ�Ce3+��ˮ��Һ����ȡ�������ù��̿ɱ�ʾΪ��2 Ce3+ (ˮ��) +6HT (�л���)![]() 2CeT3 (�л���) +6H+ (ˮ��)
2CeT3 (�л���) +6H+ (ˮ��)
��ƽ���ƶ��ǶȽ����� ��CeT3(�л���) ����H2SO4��ýϴ��ĺ�Ce3+��ˮ��Һ��ԭ����____________________��
��4��Ce(OH)3��¶�ڿ�����ʱ�����ɫ�����ձ�ɻ�ɫ��Ce(OH)4���÷�Ӧ�Ļ�ѧ����ʽΪ________________________________��
��5����֪298 K ʱ��Ksp[Ce(OH)3]=1��10-20��Ϊ��ʹ��Һ��Ce3+������ȫ�������pHΪ______���ϡ�
���𰸡� �������������ĽӴ����������Ӧ���ʣ����ԭ�ϵ������� +3 2CeO2+H2O2+6H+===2Ce3+ +O2��+4H2O H2O2�����ֽ� ���Һ�м��� H2SO4 ʹ c(H+)����ƽ�����γ� Ce3+ˮ��Һ�����ƶ� 4Ce(OH)3 +O2+2H2O===4Ce(OH)4 9
�����������⿼�黯ѧ�������̣���1����ʯ����ɿ���������Ӵ�������ӿ췴Ӧ���ʣ����ԭ�ϵ������ʣ�CeFCO3��CO3�ԣ�2�ۣ�F�ԣ�1�ۣ����廯�ϼ۴�����Ϊ0����Ce�ԣ�3�ۣ���2����������Һ��Ce4����ǿ�����ԣ�������������ǿ����������ʱ�����ֻ�ԭ�ԣ���������������������ʱ�����ӷ���ʽΪ2CeO2��H2O2��6H��=2Ce3����O2����4H2O����Ϊ�������ⲻ�ȶ��������ֽ⣬������ʱ�¶Ȳ��ܹ��ߣ���ֹH2O2���ȷֽ⣻��3��������ȡ�Ĺ��̣��������ᣬ����c(H��)��ʹƽ�����淴Ӧ������У���4��������ϢCe�Ļ��ϼ��ɣ�3�ۡ���4�ۣ����ϼ����ߣ�Ӧ������������������Ӧ����ʽΪ��4Ce(OH)3 +O2+2H2O=4Ce(OH)4 ����5��������Ũ��С�ڻ����10��5mol��L��1��������ȫ�������ܶȻ��ı���ʽc(OH��)= 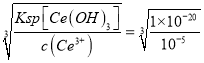 =10��5mol/l��c(H��)=Kw/c(OH��)=10��9mol��L��1����pH=9��
=10��5mol/l��c(H��)=Kw/c(OH��)=10��9mol��L��1����pH=9��


 ÿ��10���ӿ�����������������ϵ�д�
ÿ��10���ӿ�����������������ϵ�д�
| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ������0.1000 mol��L��1KMnO4������Һ�ζ�δ֪Ũ�ȵ���ɫH2C2O4��Һ����Ӧ���ӷ���ʽ�ǣ�2MnO4����5H2C2O4��6H+ = 2Mn2+��10CO2����8H2O
���������⣺
��1���õζ�ʵ������IJ���������______________��������ĸ��
A����ʽ�ζ���B����ʽ�ζ��� C����Ͳ D����ƿ E������̨F���ζ��ܼ�G���ձ�H����ֽ I��©��
��2������________(��ᡱ�)ʽ�ζ���ʢ�Ÿ��������Һ���Է���ԭ��___________________________________________��
��3���ζ��յ������Ϊ___________________________________��
��4�����ζ���ʼ�ͽ���ʱ���ζ����е�Һ����ͼ��ʾ������ʼ����Ϊ________mL���յ����Ϊ________mL��
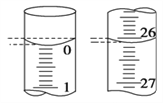
��5��ijѧ������3��ʵ��ֱ��¼�й��������±���
�ζ� ���� | ����H2C2O4��Һ�����/mL | 0.1000 mol/L KMnO4�������mL�� | ||
�ζ�ǰ�̶� | �ζ���̶� | ��Һ���/mL | ||
��һ�� | 25.00 | 0.00 | 26.11 | 26.11 |
�ڶ��� | 25.00 | 1.56 | 30.30 | 28.74 |
������ | 25.00 | 0.22 | 26.31 | 26.09 |
�����ϱ�������ʽ�����H2C2O4��Һ�����ʵ���Ũ��Ϊ_______________��
��6�����в����п���ʹ�ⶨ���ƫ�͵���___________(����ĸ)��
A����ʽ�ζ���δ�ñ�Һ��ϴ��ֱ��ע��KMnO4��Һ
B���ζ�ǰʢ�Ų�����Һ����ƿ������ˮϴ����û�и���
C����ʽ�ζ��ܼ��첿���ڵζ�ǰû�����ݣ��ζ���������
D����ȡKMnO4��Һʱ����ʼ���Ӷ������ζ�����ʱ���Ӷ���
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ������ʵ�������Ҫ�õ�������������������ͬ���ǣ� �� �ٹ��� ������ ���ܽ� ��������ƿ��ת��Һ�壮
A.�٢�
B.�٢ڢ�
C.�ڢۢ�
D.�٢�
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ�����и�����������Һ�п��Դ������棬��������������Һ��Ҳ�������������ǣ� ��
A.Na����Ba2����Cl����SO42��B.K����Na����NO3����OH��
C.H�� ��NH4����Fe3����SO42��D.H����Cl����CO32����NO3��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��̼�������ȡ�þ������ͭ�Ǽ�����Ҫ��Ԫ�أ���ش��������⣺
(1)��Ԫ�صĺ˵����Ϊ28�����̬ԭ�ӵĵ����Ų�ʽΪ____________________���ṹ����__________�ֲ�ͬ��״�ĵ����ơ�
(2)MgO���۵����CuO��������________________________________________��
(3)þԭ�ӵ�һ�����ܷ����ظ�������ԭ����_____________________________��
(4)Ni��CO���γ������![]() ���÷�����
���÷�����![]() ����
����![]() ��������Ϊ__________��
��������Ϊ__________��
(5) ![]() �����е�����ԭ���ӻ����������__________���÷��ӵĿռ乹��Ϊ__________��
�����е�����ԭ���ӻ����������__________���÷��ӵĿռ乹��Ϊ__________��
(6)ͭ�������γ���ͼ��ʾ�ľ����ṹ������ͭԭ�Ӿ��ȵط�ɢ�ھ����ڲ���a��bԭ�ӵ������������Ϊ(0��0��0)��![]() ����dԭ�ӵ��������Ϊ____________________����֪���þ�����ܶ�Ϊ
����dԭ�ӵ��������Ϊ____________________����֪���þ�����ܶ�Ϊ![]() ��
�� ![]() �ǰ����ӵ�������ֵ��������Ϊ__________cm(�г�����ʽ����)��
�ǰ����ӵ�������ֵ��������Ϊ__________cm(�г�����ʽ����)��

�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��ij������ͨ��V L CO2���ټ�������Na2O2�����������С��W L�������յ�CO2������ǣ���Ϊ��ͬ�����£�
A.��V��W��LB.2��V��W��LC.��2V��W��LD.2W L
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ�������ѳ������л���Ӧ���ܼ���ʵ�����Ʊ������ѵķ�Ӧ����Ҫʵ��װ�����£�2CH3CH2CH2CH2OH![]() ��CH3CH2CH2CH2��2O+H2O����Ӧ��Ͳ��������������±���
��CH3CH2CH2CH2��2O+H2O����Ӧ��Ͳ��������������±���
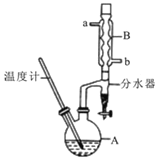

�ٽ�6 mLŨ�����37 g����������һ��˳�����ӵ�A�У����Ӽ�����ʯ��
�ڼ���A�з�ӦҺ��Ѹ��������135�棬ά�ַ�Ӧһ��ʱ�䡣
�۷����ᴿ����A��Һ����ȴ���仺������ʢ��70 mLˮ���¶ȷ�Һ©���У���ҡ���ã���Һ�ôֲ��
�ֲܴ���������40 mLˮ��20 mL NaOH��Һ��40 mLˮϴ�ӣ���Һ�����Լ3g��ˮ�Ȼ��ƿ���������һ��ʱ�����ȥ�Ȼ��ơ�
�ݽ������������Ĵֲ�����������ռ���֣��ô���������11g����ش�
��1���������Ũ�����������������˳��Ϊ��Ӧ�ȼ� ��
��2������Aǰ�����ȴ� ���a����b��������B��ͨ��ˮ��
��3������۵�Ŀ���dz���ϴȥ ����ҡ���ã��ֲ���Ӧ ����ϡ����¡����ڵ�����
��4��������У���������ʱӦ�ռ� ����ѡ����ĸ�����ҵ���֡�
A��100�� B��117�� C��135�� D��142��
��5����Ӧ�����л�۲쵽��ˮ�����ռ���Һ�����ʣ��ҷ�Ϊ�������㣬���ŷ�Ӧ�Ľ��У���ˮ����Һ��������������ʱ���ϲ�Һ�������֧���Զ�����A����ˮ�����ϲ�Һ�����Ҫ�ɷ�Ϊ ���²�Һ�����Ҫ�ɷ�Ϊ ��
��6����ʵ���У������ѵIJ���Ϊ ����ȷ��1%����
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ���Ӻ�ˮ�п��Ի�õ�ˮ��ʳ�β�����ȡþ��������ʣ�
��1����ˮ�����ķ�����Ҫ��_____________������������________________ ��
��2�����뾭����ѧ�仯���ܴӺ�ˮ�л�õ������ǣ�����ţ�_____________��
A���ȡ��塢�⡡����B���ơ�þ��������C���ռ��������D��ʳ�Ρ���ˮ
��3���Ӻ�ˮ����ȡþ��������ͼ��ʾ��
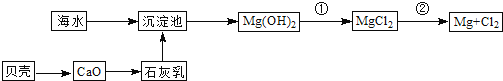
��Ӧ�ڵĻ�ѧ����ʽΪ_________________________________________________��
��4���Ӻ�ˮ����ȡ�����Ҫ��������Ũ���ĺ�ˮ��ͨ�������������������������塣���嵥�ʵ�ˮ��Һ��ͨ�������ˮ�������嵥�ʴ���ʢ��SO2��Һ������������Ŀ����_________���÷�Ӧ�Ļ�ѧ����ʽΪ________________________________��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ������������ȷ���ǣ� ��
A.1 mol H2SO4 ������Ϊ98 gmol��1
B.H2SO4��Ħ������Ϊ98 g
C.9.8 g H2SO4����NA��H2SO4����
D.6.02��1023��H2SO4���ӵ�����Ϊ98 g
�鿴�𰸺ͽ���>>
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com