
| 实验设计及操作 | 离子方程式 |
| Ⅰ.向盛有2mlCuSO4溶液的试管里加入2mlNaOH溶液,观察现象 | Cu2++2OH-═Cu(OH)2↓ |
| Ⅱ.向盛有2mL pH=1的HCl溶液的试管里慢慢滴入18mL(已足量)CH3COONH4溶液(查资料知CH3COONH4,溶液呈中性 )震荡摇匀,测得pH≈3.7 | |
| Ⅲ向盛有2mLNaHCO3溶液的试管里加入2mL H2SO4溶液,观察现象 | HCO${\;}_{3}^{-}$+H+═H2O+CO2↑ |
| Ⅳ向盛有2mL 稀Na2SO4溶液的试管里加入2mL稀KCl溶液,观察无明显现象 |  |
分析 (1)①如果二者不反应,混合后溶液中c(H+)=$\frac{0.1mol/L×0.002L}{(0.002+0.018)L}$=0.01mol/L,混合溶液pH=2,实际上溶液pH=3.7>2,说明II实验中二者反应生成弱电解质醋酸;
②实验I中生成沉淀、实验II中生成弱电解质、实验3中生成气体和弱电解质;
③通过实验对比知,只要发生复分解反应,则离子浓度一定减小;
④当生成上述三类物质时,形成新的化学键而导致体系的焓减或生成气体而导致熵增;
(2)①在水溶液里电离出的阳离子全部是氢离子的化合物是酸,根据酸的定义判断是否属于酸;
②酸性条件下,硝酸根离子具有强氧化性,能氧化硫离子生成S单质,同时生成NO;
该反应中被氧化的物质是Na2S,根据转移电子相等计算被氧化的物质物质的量;
③氯化铵和碱反应生成氨气,硝酸钠和氯化铵不反应,据此分析解答.
解答 解:(1)①如果二者不反应,混合后溶液中c(H+)=$\frac{0.1mol/L×0.002L}{(0.002+0.018)L}$=0.01mol/L,混合溶液pH=2,实际上溶液pH=3.7>2,说明II实验中二者反应生成弱电解质醋酸,离子方程式为H++CH3COO-=CH3COOH,故答案为:H++CH3COO-=CH3COOH;
②实验I中生成沉淀、实验II中生成弱电解质、实验3中生成气体和弱电解质,这三个实验都发生复分解反应,IV中不产生上述物质,所以不发生复分解反应,则复分解反应条件是生成气体、沉淀、弱电解质中的一个即可,故答案为:气体、沉淀、弱电解质;
③通过实验对比知,只要发生复分解反应,则离子浓度一定减小,所以离子反应总是向着离子浓度减小的方向进行,故答案为:离子浓度减小;
④当生成上述三类物质时,形成新的化学键而导致体系的焓减或生成气体而导致熵增,由化学反应进行的方向的焓判据和熵判据知,反应可发生,
故答案为:当生成上述三类物质时,形成新的化学键而导致体系的焓减或生成气体而导致熵增,由化学反应进行的方向的焓判据和熵判据知,反应可发生;
(2)①在水溶液里电离出的阳离子全部是氢离子的化合物是酸,氯化铵在水溶液中只电离出铵根离子和酸根离子,且氯化铵溶液呈酸性是因为水解导致的,硫酸氢钠在水溶液中电离出的阳离子还有钠离子,所以氯化铵和硫酸氢钠都是盐,
故答案为;不合理;硫酸氢钠和氯化铵都属于盐,前者电离产生的阳离子除了氢离子还有钠离子,后者是因为水解而显酸性;
②酸性条件下,硝酸根离子具有强氧化性,能氧化硫离子生成S单质,同时生成NO,离子方程式为2NO3-+3S2-+8H+=2NO↑+3S↓+4H2O;
该反应中被氧化的物质是Na2S,根据转移电子相等得被氧化的物质物质的量=$\frac{\frac{1.12L}{22.4L}×3}{2}$=0.075mol,
转移电子物质的量=$\frac{1.12L}{22.4L/mol}$×3=0.15mol,
故答案为:2NO3-+3S2-+8H+=2NO↑+3S↓+4H2O;0.075;0.15;
③氯化铵和碱反应生成氨气,硝酸钠和氯化铵不反应,则其鉴别方法为:取两张待测液少许于试管中,分别加入氯化铵溶液并加热,有刺激性气味气体产生的为NaOH,另一种为硝酸钠,
答:取两张待测液少许于试管中,分别加入氯化铵溶液并加热,有刺激性气味气体产生的为NaOH,另一种为硝酸钠.
点评 本题考查物质检验和鉴别实验方案设计、离子反应条件探究等知识点,为高频考点,明确物质性质及其性质差异性、离子反应条件是解本题关键,侧重考查学生分析、实验探究及总结归纳、实验操作及设计能力,题目难度中等.


 培优好卷单元加期末卷系列答案
培优好卷单元加期末卷系列答案科目:高中化学 来源: 题型:选择题
| A. | 该冶炼锌的反应属于置换反应 | |
| B. | 煤炭中起作用的主要成分是C | |
| C. | 冶炼Zn的反应方程式为:ZnCO3+2C$\frac{\underline{\;高温\;}}{\;}$Zn+3CO↑ | |
| D. | 倭铅是指金属锌和铅的混合物 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | AlCl3溶液中加入过量氨水:Al3++4NH3•H2O═AlO${\;}_{2}^{-}$+4NH${\;}_{4}^{+}$+2H2O | |
| B. | 在海带灰的浸出液(含有I-)中滴加H2O2得到I2:2I-+H2O2+2H+═I2+O2↑+2H2O | |
| C. | 在氢氧化钡溶液中滴加硫酸氢钾溶液至PH=7:Ba2++2OH-+2H++SO42-═BaSO4↓+2H2O | |
| D. | 用碳酸钠溶液浸泡锅炉水垢:Ca2++CO32-═CaCO3↓ |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
| 温度/℃ | 400 | 500 | 800 |
| 平衡常数K | 9.94 | 9 | 1 |
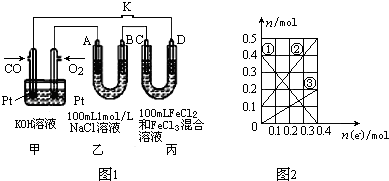
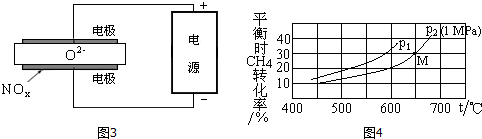
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com