
| A. | H2SeO3 | B. | H2SeO3和HSeO3- | C. | HSeO3- | D. | HSeO3-和SeO32- |
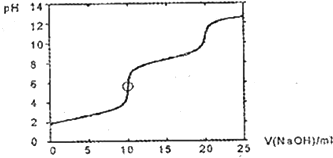
分析 0.100mol/LH2SeO3的pH=2,说明H2SeO3?HSeO3-+H+的电离程度为10%,此时HSeO3-含硒量约占溶液中硒总量的10%,曲线第一波段发生的反应为H2SeO3+NaOH=NaHSeO3+H2O,第二波段发生的反应为NaHSeO3+NaOH=Na2SeO3+H2O.
解答 解:0.100mol/LH2SeO3的pH=2,说明H2SeO3?HSeO3-+H+的电离程度为10%,此时HSeO3-含硒量约占溶液中硒总量的10%,
曲线第一波段发生的反应为H2SeO3+NaOH=NaHSeO3+H2O,导致该波段中任何一点的HSeO3-含硒量占溶液中硒总量大于10%,
第二波段发生的反应为NaHSeO3+NaOH=Na2SeO3+H2O,
故选C.
点评 本题考查了酸、碱混合时的定性判断,难度中等,明确加入强碱性溶液对弱酸的电离平衡的影响是解题的关键.


科目:高中化学 来源: 题型:选择题
| A. | 液氯能使鲜花褪色 | |
| B. | 蒸馏实验中,温度计水银球应位于蒸馏烧瓶支管口处 | |
| C. | 只用BaCl2溶液就可以鉴别SO42-和CO32- | |
| D. | 在实验室里,硅酸钠溶液存放在带磨口玻璃塞的试剂瓶中 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | ①② | B. | ②③ | C. | ①④ | D. | ③④ |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 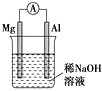 图铝片发生的电极反应式是:Al+4OH-3e-═AlO2-+2H2O | |
| B. |  图发生析氢腐蚀,离子反应方程式为:Fe+2H+═Fe2++H2↑ | |
| C. | 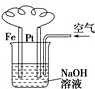 图溶液中发生了变化:4Fe(OH)2+O2+2H2O═4Fe(OH)3 | |
| D. | 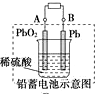 图充电时,阳极反应是:PbSO4+2H2O-2e-═=PbO2+SO42-+4H+ |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 该电池负极的电极反应为:Al-3e-═Al3+ | |
| B. | 该电池可能是一种可充电的二次电池 | |
| C. | 消耗相同质量金属时,用锂作负极产生电子的物质的量比用铝时多 | |
| D. | 电池工作时,溶液中铝离子向正极移动 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 溶液是电中性的,胶体是带电的 | |
| B. | 胶体粒子可以通过半透膜而溶液不行,故可以用半透膜来分离胶体和溶液 | |
| C. | 一束光线分别通过溶液和胶体时,后者会出现明显的光带,前者则没有 | |
| D. | 溶液中溶质粒子的运动有规律,胶体中分散质粒子的运动无规律,即布朗运动 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 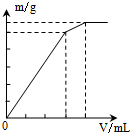 Al2(SO4)2 | B. | 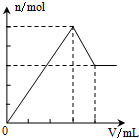 KAl(SO4)2 | C. | 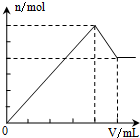 NH4Al(SO4)2 | D. | 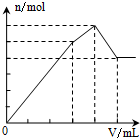 NH4Al(SO4)2 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com