
已知:①向饱和NaCl的氨气溶液中持续通入CO2气体;②向饱和Na2CO3溶液中通入足量的CO2气体。最终两种溶液中均会析出NaHCO3晶体,下列有关说法中错误的是( )
A.①中的离子反应方程式是:Na++NH3+CO2+H2O =NaHCO3↓ + NH4+
B.②中的离子反应方程式是:2Na++CO32-+H2O+CO2 = 2NaHCO3↓
C.上述变化说明相同温度下溶解度Na2CO3 > NaHCO3 > NaCl
D.向饱和CaCl2溶液中加入浓Ba(OH)2溶液,也会析出晶体
科目:高中化学 来源: 题型:
取体积相同的KI、Na2SO3、FeBr2溶液,分别通入足量氯气,当恰好完全反应时,三种溶液消耗氯气的物质的量相同,则KI、Na2SO3、FeBr2溶液的物质的量浓度之比为 ( )
A. 2∶1∶2 B. 2∶1∶3 C. 6∶3∶2 D. 3∶7∶1
查看答案和解析>>
科目:高中化学 来源: 题型:
铁是日常生活中用途最广、用量最大的金属材料。
 (1)常温下,可用铁质容器盛装浓硫酸的原因是 。
(1)常温下,可用铁质容器盛装浓硫酸的原因是 。
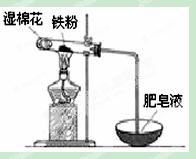
(2)某实验小组利用右图装置验证铁与水蒸气的反应。
①湿棉花的作用是 ,试管中反应的化学方程式是 。
②实验结束后,取出少量反应后的固体于试管中,加入过量盐酸,固体完全溶解,所得溶液中存在的阳离子是 (填序号)。
a.一定有Fe2+、H+和Fe3+ b.一定有Fe2+、H+,可能有Fe3+
c.一定有Fe2+、Fe3+,可能有 H+ d.一定有Fe3+、H+,可能有Fe2+
(3)另称取一定量的铁钉放入足量的浓硫酸中,加热,充分反应后收集气体。经测定气体中含有SO2、CO2和H2。
① 铁与足量的浓硫酸反应的化学方程式是 。
② 将672 mL(标准状况)收集到的气体通入足量溴水中,发生反应:
SO2 + Br2 + 2H2O = 2HBr + H2SO4,然后加入足量BaCl2溶液,经洗涤、干燥得到固体4.66 g。由此推知收集到的气体中SO2的体积分数是 。( 结果保留三位有效数字)
结果保留三位有效数字)
查看答案和解析>>
科目:高中化学 来源: 题型:
下列有关实验的现象描述正确的是 ( )
A.氢气在氯气中燃烧,火焰呈苍白色,瓶口出现大量白雾
B.磷在氯气中燃烧,发出明亮的蓝紫色火焰,产生大量白色烟雾
C.铜在氯气中燃烧,产生白烟,加水溶解后可得蓝绿色溶液
D.用洁净的铂丝沾取碳酸钾粉末在酒精灯火焰上灼烧,可观察到明亮的紫色火焰
查看答案和解析>>
科目:高中化学 来源: 题型:
工业上将Na2CO3和Na2S以1:2的物质的量之比配成溶液,再通入SO2,可制取Na2S2O3,同时放出CO2。在该反应中 ( )
A.二氧化硫体现还原性,做还原剂
B.氧化剂与还原剂的物质的量之比为1:2
C.每生成1molNa2S2O3,转移4mol电子
D.相同条件下,每吸收10m3SO2就会放出2.5m3CO2
查看答案和解析>>
科目:高中化学 来源: 题型:
A、B、C、D、E五种元素均为短周期元素,原子序数逐渐增大。A是宇宙中含量最高的元素,B可形成多种同素异形体,其中一种的硬度自然界中最大。D元素原子的最外层电子数是次外层电子数的3倍。E元素的最高价氧化物的水化物的酸性强于硫酸。
(1)写出元素C在元素周期表的位置 ,单质E的工业制备的离子方程式为________。
(2)B、C、D三种元素的最简单氢化物的稳定性从大到小的顺序是 (填化学式),
B的单质,在加热条件下能与C的最高价氧化物对应的水化物的浓溶液反应,写出对应的化学方程式 。
(3)A、B、C、D几种元素之间可以形成多种10电子微粒,写出上述10电子微粒中离子之间反应的一个离子方程式:
查看答案和解析>>
科目:高中化学 来源: 题型:
下列关于Na2O和Na2O2的叙述正确的是( )
A.Na2O与Na2O2颜色相同 B.均可与CO2、H2O反应产生氧气
C.所含氧元素的化合价均为-2 D.阴阳离子的个数比均为1:2
查看答案和解析>>
科目:高中化学 来源: 题型:
X、Y、Z、W、R属于短周期主族元素。X的原子半径是短周期主族元素中最大的,Y元素的原子最外层电子数为m,次外层电子数为n,Z元素的原子L层电子数为m+n,M层电子数为m—n,W元素与Z元素同主族,R元素原子与Y元素原子的核外电子数之比为2:1。 下列叙述错误的是:( )
A.X与Y形成的两种化合物中阴、阳离子的个数比均为1∶2
B.Y的氢化物比R的氢化物稳定,熔沸点高
C.Z、W、R最高价氧化物对应水化物的酸性强弱顺序是:R>W>Z
D.RY2、WY2通入BaCl2溶液中均有白色沉淀生成。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com