
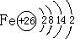 ,
,分析 (1)铁为26号元素第ⅤⅢ族,四个电子层,最外层2个电子;
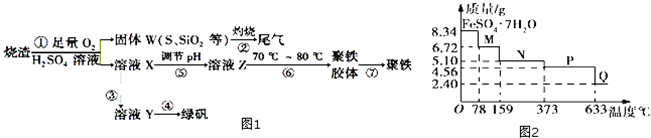
(2)根据反应物和生成物的种类结合质量守恒书写化学方程式;
(3)溶液X中含有Fe3+,要制备绿矾,应加入Fe使之还原为Fe2+;过程④是溶液中得到溶质晶体可以通过蒸发结晶得到;
(4)过程⑥目的为促进的水解,加热有利于水解的进行;
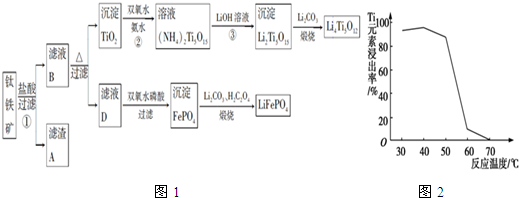
(5)8.34g FeS04•7H20样品物质的量=$\frac{8.34g}{278g/mol}$=0.03mol,其中m(H20)=0.03mol×7×18g/mol=3.78g,如晶体全部失去结晶水,固体的质量应为8.34g-3.78g=4.56g,可知在加热到373℃之前,晶体失去部分结晶水,结合质量的变化可确定在不同温度时加热后固体的化学式,加热至633℃时,固体的质量为2.40g,其中n(Fe)=n( FeS04•7H20)=0.03mol,m(Fe)=0.03mol×56g/mol=1.68g,则固体中m(O)=2.40g-1.68g=0.72g,n(O)=$\frac{0.72g}{16g/mol}$=0.045mol,则n(Fe):n(O)=0.03mol:0.045mol=2:3,则固体物质Q的化学式为Fe2O3,以此解答该题.
(6)根据n(Fe3+)=n(SO42-)计算.
解答 解:(1)铁为26号元素第ⅤⅢ族,四个电子层,最外层2个电子,原子结构示意图为: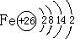 ,
,
故答案为: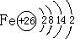 ;
;
(2)反应物为FeS、O2和H2SO4,生成物有S,根据质量守恒还应有Fe2(SO4)3和H2O,
反应的化学方程式为4FeS+3O2+6H2SO4=2Fe2(SO4)3+6H2O+4S,
故答案为:4FeS+3O2+6H2SO4=2Fe2(SO4)3+6H2O+4S;
(3)溶液X中含有Fe3+,要制备绿矾,应加入Fe使之还原为Fe2+,加入铁可生成Fe2+,并且不引入新的杂质,过程④是溶液中得到溶质晶体可以通过蒸发结晶得到,
故答案为:Fe(或铁),蒸发结晶;
(4)过程⑥目的为促进的水解,加热有利于水解的进行,促进Fe3+的水解,
故答案为:促进Fe3+的水解;
(5)8.34g FeS04•7H20样品物质的量=$\frac{8.34g}{278g/mol}$=0.03mol,其中m(H20)=0.03mol×7×18g/mol=3.78g,如晶体全部失去结晶水,固体的质量应为8.34g-3.78g=4.56g,可知在加热到373℃之前,晶体失去部分结晶水,
A.温度为78℃时,固体质量为6.72g,其中m(FeS04)=0.03mol×152g/mol=4.56g,m(H20)=6.72g-4.56g=2.16g,n(H20)=$\frac{2.16g}{18g/mol}$=0.12mol,则n(H20):n(FeS04)=0.12mol:0.03mol=4:1,则化学式为FeSO4•4H2O,故A错误;
B.温度为l59℃时,固体质量为5.10g,其中m(FeS04)=0.03mol×152g/mol=4.56g,m(H20)=5.10g-4.56g=0.54g,n(H20)=$\frac{0.54g}{18g/mol}$=0.03mol,则n(H20):n(FeS04)=0.03mol:0.03mol=1:1,则化学式为FeSO4•H2O,故B错误;
C.m(FeS04)=0.03mol×152g/mol=4.56g,则在隔绝空气条件下由N得到P的化学方程式为FeSO4•H2O$\frac{\underline{\;\;△\;\;}}{\;}$FeS04+H20,故C错误;
D.加热至633℃时,固体的质量为2.40g,其中n(Fe)=n( FeS04•7H20)=0.03mol,m(Fe)=0.03mol×56g/mol=1.68g,则固体中m(O)=2.40g-1.68g=0.72g,n(O)=$\frac{0.72g}{16g/mol}$=0.045mol,则n(Fe):n(O)=0.03mol:0.045mol=2:3,则固体物质Q的化学式为Fe2O3,故D正确.
故选D.
故答案为:D.
(6)过滤、洗涤、干燥,称量,得固体质量为3.495g,应为BaSO4沉淀,
n(BaSO4)=$\frac{3.495g}{233g/mol}$=0.015mol,
则n(Fe3+)=n(SO42-)=0.015mol,
m(Fe)=0.015mol×56g/mol=0.84g,
ω(Fe)=$\frac{0.84g}{2.7g}$×100%=31.1%,
故答案为:31.1%
点评 本题考查较为综合,涉及物质含量的测定、制备实验方案的设计等知识,题目难度较大,注意常见化学实验操作方法.


 智能训练练测考系列答案
智能训练练测考系列答案科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源:2016-2017学年江西省高二上月考一化学试卷(解析版) 题型:选择题
下列说法或表示方法正确的是
A.HI(g) 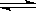 1/2H2(g)+ 1/2I2(s);△H = —26.5kJ/mol,由此可知1mol HI在密闭容器中分解后可以放出26.5kJ的能量
1/2H2(g)+ 1/2I2(s);△H = —26.5kJ/mol,由此可知1mol HI在密闭容器中分解后可以放出26.5kJ的能量
B.在稀溶液中,H+(aq)+OH-(aq)==H2O(l) ΔH=-57.3 kJ·mol-1,若将含0.5 mol H2SO4的浓硫酸与含1mol NaOH的溶液混合,放出的热量大于57.3 kJ
C.由C(石墨)==C(金刚石) ΔH=1.90 kJ·mol-1可知,金刚石比石墨稳定
D.在100 kPa时,2 g H2完全燃烧生成液态水,放出285.8 kJ热量,则H2 燃烧的热化学方程式为2H2(g)+O2(g)==2H2O(l) ΔH=-285.8 kJ·mol-1
燃烧的热化学方程式为2H2(g)+O2(g)==2H2O(l) ΔH=-285.8 kJ·mol-1
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
| 水解反应 | 平衡常数(K) |
| Fe3++3H2O?Fe(OH)3+3H+ | 7.9×10-4 |
| Fe2++2H2O?Fe(OH)2+2H+ | 3.2×10-10 |
| Cu2++2H2O?Cu(OH)2+2H+ | 3.2×10-7 |
| 实验内容 | 实验现象 |
| 甲同学的实验方案 | 溶液逐渐变成蓝绿色,pH略有上升 |
| 乙同学的实验方案 | 无明显现象,pH没有明显变化. |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题

| 沉淀物 | 开始沉淀时的pH | 完全沉淀时的pH |
| Al(OH)3 | 3.8 | 5.2 |
| Fe(OH)3 | 2.7 | 3.2 |
| Fe(OH)2 | 7.6 | 9.7 |
| Ni(OH)2 | 7.1 | 9.2 |
查看答案和解析>>
科目:高中化学 来源: 题型:多选题
| 选项 | 操作 | 现象 | 结论 |
| A | 将足量的乙烯通入到溴水中 | 溴水褪色 | 乙烯与溴水反应生成无色物质 |
| B | 往CaCl2溶液中通入足量的CO2 | 先有白色沉淀生成,后沉淀溶解 | CaCO3不溶于水,Ca(HCO3)2可溶于水 |
| C | 将铜板电路投入FeCl3溶液中 | 铜溶于FeCl3溶液 | 氧化性:Fe3+>Cu2+ |
| D | 取久置的Na2O2粉末,向其中滴加足量的盐酸 | 产生无色气体 | Na2O2已变质为Na2CO3 |
| A. | A | B. | B | C. | C | D. | D |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
 某同学用下图所示实验装置制取乙酸乙酯.回答以下问题:
某同学用下图所示实验装置制取乙酸乙酯.回答以下问题:查看答案和解析>>
科目:高中化学 来源: 题型:解答题
 实验室用乙酸和正丁醇制备乙酸正丁酯.有关物质的相关数据如下表:
实验室用乙酸和正丁醇制备乙酸正丁酯.有关物质的相关数据如下表:| 化合物 | 相对分子质量 | 密度/g•cm-3 | 沸点/℃ | 溶解度g/l00g水 |
| 正丁醇 | 74 | 0.80 | 118.0 | 9 |
| 冰醋酸 | 60 | 1.045 | 118.1 | 互溶 |
| 乙酸正丁酯 | 116 | 0.882 | 126.1 | 0.7 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com