
| ||
| ||


 阅读快车系列答案
阅读快车系列答案科目:高中化学 来源: 题型:

| A、正极被保护 |
| B、H+向Zn电极移动 |
| C、加入少量KSCN溶液,变血红色 |
| D、负极的电极反应式是:Fe-2e-=Fe2+ |
查看答案和解析>>
科目:高中化学 来源: 题型:
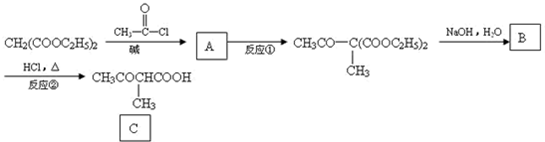
| ①D |
| 碱 |
| ②NaOH,H2O |
| ③HCl,△ |
 COOH,
COOH,查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
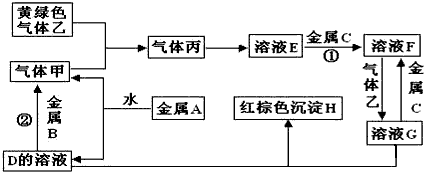
查看答案和解析>>
科目:高中化学 来源: 题型:

| 时间/浓度 | c(CO)(mol/L) | c(H2 )(mol/L) | c(CH3OH)(mol/L) |
| 起始 | 0.200 | 0.300 | 0.000 |
| 第4min | a | b | c |

查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、任何离子键在形成的过程中必定有电子的得与失 |
| B、电解质与非电解质的本质区别,是在水溶液或熔化状态下能否电离 |
| C、用氯气消毒过的自来水配制亚硫酸钠溶液,不会产生明显药品变质 |
| D、一定条件下若反应能自发进行,则其△S>0 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com