
| A��0.01mol/L CH3COOH��pH=12��NaOH��Һ��ϣ�����Ϻ�c��CH3COO-����c��Na+��������Һһ���ʼ��� |
| B�������£��������0.01mol/L HCl��pH=12�İ�ˮ��ϣ�����Һ��pH=7 |
| C��0.1mol/L��ij��Ԫ������Na2A��Һ�У�c��Na+��=2c��H2A��+2c��HA-��+2c��A2-�� |
| D����5mL 0.02mol/L��H2SO4��5mL 0.02mol/L NaOH��Һ��ֻ�ϣ�����Ϻ���Һ�����Ϊ10mL������Һ��pH=7 |
| 0.005L��0.02mol/L��2-0.02mol/L��0.005L |
| 0.01L |


 �Ķ��쳵ϵ�д�
�Ķ��쳵ϵ�д�
| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
| A��CuFeS2������ԭ������Ԫ�ر����� |
| B��SO2���������FeS�ǻ�ԭ���� |
| C��ÿ����1mol Cu2S����4mol������ |
| D��ÿת��1.2mol���ӣ���0.2mol������ |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
| A��33.6L������27g����ַ�Ӧ��ת�Ƶĵ�����һ��Ϊ3NA |
| B����0.2mol Cl2�ܽ���10L��ˮ�У�������0.2NA��HClO |
| C����CO2��O2��ɵĻ�����й���NA�����ӣ����е���ԭ����Ϊ2NA |
| D��0.012kg 13C�У���̼ԭ����ΪNA |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
| A��1.0L 1.0mo1?L-1��NaAlO2ˮ��Һ�к��е���ԭ����Ϊ2NA |
| B��12gʯīϩ������ʯī���к�����Ԫ���ĸ���Ϊ0.5NA |
| C��25��ʱpH=13��NaOH��Һ�к���OH-����ĿΪ0.1NA |
| D��1mol���ǻ���1moL������������������������Ϊ9NA |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
| A | B | C | D |
 |
 |
 |
 |
| ��֤��ѧ��ת��Ϊ���� | ��֤�¶ȶ�ƽ���ƶ���Ӱ�� | ��֤�������ⸯʴ | ��֤�ǽ���Cl��C��Si |
| A��A | B��B | C��C | D��D |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�

| ||
| T/�� | 20 | 40 | 60 | 80 |
| S��Li2CO3��/g | 1.33 | 1.17 | 1.01 | 0.85 |
| S��Li2SO4��/g | 34.2 | 32.8 | 31.9 | 30.7 |

�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
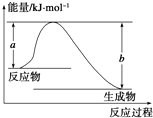 �Ͽ�1mol AB��g�������еĻ�ѧ��ʹ��ֱ�������̬Aԭ�Ӻ���̬Bԭ�������յ�������ΪA-B���ļ��ܣ��±��г���һЩ��ѧ���ļ���E��
�Ͽ�1mol AB��g�������еĻ�ѧ��ʹ��ֱ�������̬Aԭ�Ӻ���̬Bԭ�������յ�������ΪA-B���ļ��ܣ��±��г���һЩ��ѧ���ļ���E��| ��ѧ�� | H-H | Cl-Cl | O�TO | C-Cl | C-H | O-H | H-Cl |
| E/kJ?mol-1 | 436 | 247 | x | 330 | 413 | 463 | 431 |
| 1 |
| 2 |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
 S2Cl2�����������л����Ȼ����Լ���ij�о���ѧϰС������ʵ���ҳ����Լ��������ϳ�S2Cl2��
S2Cl2�����������л����Ȼ����Լ���ij�о���ѧϰС������ʵ���ҳ����Լ��������ϳ�S2Cl2���鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
| A��0.1 mol/L |
| B��0.2 mol/L |
| C��0.3 mol/L |
| D��0.4 mol/L |
�鿴�𰸺ͽ���>>
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com