
分析 (1)设R元素相对原子质量为a,根据电子转移守恒列方程计算;
(2)根据相对原子质量可以确定R元素,进而确定其质子数,计算各同位素质量数,设含12个中子的同位素的摩尔分数为x,则含14个中子的同位素的摩尔分数为(1-x-10.13%),根据元素相对原子质量列方程解答.
解答 解:(1)设R元素相对原子质量为a,根据电子转移守恒:$\frac{1.216}{a}$×2=$\frac{1.12}{22.4}$×2,解得a=24.32,
答:R元素相对原子质量为24.32;
(2)由相对原子质量可知,R为Mg元素,中子数分别为12、13和14的Mg的质量数分别为24、25、26,设含12个中子的同位素的摩尔分数为x,则含14个中子的同位素的摩尔分数为(1-x-10.13%),则:24x+25×10.13%+26×(1-x-10.13%)=24.32,解得x=78.935%,
答:含12个中子的同位素的摩尔分数为78.935%.
点评 本题考查化学方程式计算、相对原子质量,难度不大,注意掌握原子的相对原子质量、近似相对原子质量与元素相对原子质量、近似相对原子质量.


科目:高中化学 来源: 题型:选择题
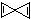 的烃X,根据分析,下列说法中不正确的是( )
的烃X,根据分析,下列说法中不正确的是( )| A. | X的分子式为C5H4 | |
| B. | 分子中氢原子的化学环境只有一种 | |
| C. | 1 mol X在一定条件下可与2 mol氢气发生反应 | |
| D. | X不能使高锰酸钾酸性溶液褪色 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | ③ | B. | ④ | C. | ②⑤ | D. | ① |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 若R(OH)n为强碱,则W(OH)m也为强碱 | |
| B. | 若HnXOm为强酸,则Y是活泼非金属元素 | |
| C. | 若Y的最低化合价为-2,则Z的最高正化合价为+6 | |
| D. | 若X的最高正化合价为+5,则五种元素都是非金属元素 |
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
 .
.查看答案和解析>>
科目:高中化学 来源: 题型:解答题

 ;
;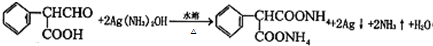 .
.查看答案和解析>>
科目:高中化学 来源: 题型:解答题
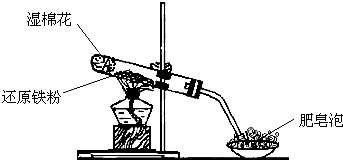
| 实验操作 | 预期的现象与结论 |
| 步骤1:取1-2mL上述溶液于试管甲中,向里面再滴入几滴KSCN溶液,振荡 | 有溶液变血红色现象,则证明有Fe3+,若无该现象,则证明不含Fe3+. |
| 步骤2:另取1-2mL上述溶液于试管乙中,向里面再滴入几滴KMnO4溶液,振荡 | 有KMnO4溶液紫色褪去现象,则证明有Fe2+,若无该现象,则证明不含Fe2+. |
| 步骤3:综合步骤1.2 | 得出结论 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题

查看答案和解析>>
科目:高中化学 来源: 题型:解答题
 ;
;  ;
;查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com