
| Fe3+ | Co2+ | Co3+ | Al3+ | |
| pH����ʼ������ | 1.9 | 7.15 | -0.23 | 3.4 |
| pH����ȫ������ | 3.2 | 9.15 | 1.09 | 4.7 |
| �¶ȷ�Χ/�� | ��������/g |
| 150��210 | 4.41 |
| 290��320 | 2.41 |
| 890��920 | 2.25 |
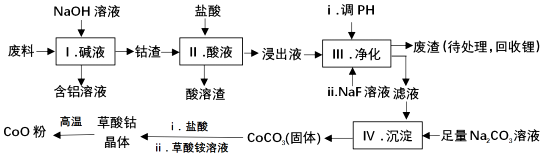
���� ���ϣ���Al��Li��Co2O3��Fe2O3�����ʣ���������������Һ�����Al�ܽ⣺2Al+2OH-+2H2O=2AlO2-+3H2�����õ�������Li��Co2O3��Fe2O3�������������ܽ��Li��Fe2O3�ܽ���������ӡ������ӣ�Co2O3����������ԭ��Ӧ������������������Ϊ������2O3+6H++2Cl-=2Co2++Cl2��+3H2O�����˵õ����ܵ���Һ����pH������NaF��Һ��������ȥ����Ӻ������ӣ�����Һ�м���̼������Һ����������Ϊ̼���ܳ�������������Ͳ������Һ�õ������ܾ��壬���·ֽ�õ������ܣ��ݴ˷�������
��� �⣺��1��������еõ�������Һ����������������Һ��Ӧ����ƫ�����ƺ���������Ӧ�Ļ�ѧ����ʽΪ��2Al+2OH-+2H2O=2AlO2-+3H2����
�ʴ�Ϊ��2Al+2OH-+2H2O=2AlO2-+3H2����
��2��I��ͨ�����˵õ������ͺ�����Һ���ʴ�Ϊ�����ˣ�
��3������������������Һ���Ȼ���Ϊ���������ԭ���غ�͵����غ������ƽ��д���ӷ���ʽ����Ԫ�ػ��ϼ۽���Ϊ+2�ۣ���Ԫ�ػ��ϼ�-1�۱仯Ϊ0�ۣ���Ӧ�����ӷ���ʽ��Co2O3+6H++2Cl-=2Co2++Cl2��+3H2O��
�ʴ�Ϊ��Co2O3+6H++2Cl-=2Co2++Cl2��+3H2O��
��4�����ݱ������ݷ����жϼ���̼���Ƶ�����ҺPH�����������Ӻ�����ӣ������ܳ��������ӣ��������Na2CO3��Һ�������ǵ�����Һ��pH��Ӧʹ��Һ��pH��ΧΪ3.2��PH��7.15��
�ʴ�Ϊ��3.2��PH��7.15��
��5��III�е���pH������NaF��Һ��������ȥ����Ӻ������ӣ������е���Ҫ�ɷ�ΪLiF��Fe��OH��3������NaF��Һ��������Һ��Li+��Ũ�ȣ����ⲽ����γ�Li2CO3�ij�����
�ʴ�Ϊ��Fe��OH��3��LiF��������Һ��Li+��Ũ�ȣ����ⲽ����γ�Li2CO3�ij�����
��6���٣�5�����ټ��㾧�����ʵ���n=$\frac{5.49g}{183g/mol}$=0.03mol��ʧȥ�ᾧˮӦΪ0.06mol�����������仯=0.06mol��18g/mol=1.08g��ͼ�����ݿ�֪��150�桫210����������仯5.49g-4.41g=1.08g��˵��210��ʧȥ�ᾧˮ�õ�CoC2O4��
�ʴ�Ϊ��CoC2O4��
��210��310���������CoC2O4�����ķ�Ӧ������������ֻ��CO2 ������Ԫ���غ�õ�����CO2���ʵ���Ϊ0.06mol������=0.06mol��44g/mol=2.64g�������������Ƽ�С=4.41g-2.41g=2g��˵��˵��������μӷ�ӦӦΪ��������Ӧ����������=2.64g-2g=0.64g��O2���ʵ���=$\frac{0.064g}{32g/mol}$=0.02mol����
n��CoC2O4����n��O2����n��CO2��=0.03��0.02��0.06=3��2��6��
����ʽ����ϵ��֮�ȵ���ת����֮�ȣ����Ը÷�Ӧ�ķ���ʽΪ��3CoC2O4+2O2$\frac{\underline{\;210��310��\;}}{\;}$Co3O4+6CO2��
�ʴ�Ϊ��3CoC2O4+2O2$\frac{\underline{\;210��310��\;}}{\;}$Co3O4+6CO2��
���� ����ͨ����ij��ҵ�����л����ܵĹ������̿����˻�ѧ����ʽ�����ӷ���ʽ��д��ȷ�������ι���ɷּ��Ⱥ�ֽ�������ɷ��ǽⱾ��ؼ�����Ŀ�Ѷ��еȣ�


 ��������һ���þ�ϵ�д�
��������һ���þ�ϵ�д� Сѧ��10����Ӧ����ϵ�д�
Сѧ��10����Ӧ����ϵ�д�
| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | ij��ɫ��Һ�п��ܴ������ڣ�H+��Cl-��MnO${\;}_{4}^{-}$ | |
| B�� | ��������ˮ����� c��OH-��=1��10-12mol•L-1����Һ���ܴ������棺K+��Na+��Cl-��HCO3- | |
| C�� | ��FeBr2��Һ��ͨ������������2Fe2++4Br-+3Cl2�T2 Fe3++2 Br2+6 Cl- | |
| D�� | ϡ�����Ba��OH��2��Һ��Ӧ��H++SO${\;}_{4}^{2-}$+Ba2++OH-�TBaSO4��+H2O |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | �Ʊ���ˮAlCl3ʱ�������SOCl2ֻ����ˮ������ | |
| B�� | ��ع��������У�SOCl2����ԭΪLi2SO3��S���� | |
| C�� | ��ع��������У����Ӿ��������Һ����﮵缫 | |
| D�� | �øõ�ص��ˮ������2mol H2������1.5molSOCl2 |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ���ѡ��
| A�� | ��������1.792L | B�� | ����AgCl����11.7g | ||
| C�� | ����ԭ��HClΪ0.16mol | D�� | ת�Ƶĵ�����Ϊ0.16�� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| ��� | �� | �� | �� | �� |
| ��Һ | NaCl | CH3COONH4 | NaHCO3 | 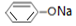 |
| pH | 7.0 | 7.0 | 8.4 | 9.9 |
| A�� | ���ԣ�H2CO3��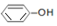 | |
| B�� | ˮ���������c��H+������=�� | |
| C�� | ��Һ���У�c��HCO3-��+c��CO32-��+c��H2CO3��=0.1mol•L-1 | |
| D�� | ��Һ���У�c��Na+����c��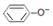 ����c��OH-����c��H+�� ����c��OH-����c��H+�� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
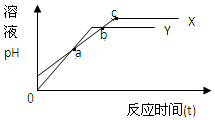 �ֱ�������1mol/L�����1mol/L������Һ�м��������þ������Ӧʱ������ҺpH�仯��ϵ��ͼ������˵���в���ȷ���ǣ�������
�ֱ�������1mol/L�����1mol/L������Һ�м��������þ������Ӧʱ������ҺpH�仯��ϵ��ͼ������˵���в���ȷ���ǣ�������| A�� | Y����������þ���ķ�Ӧ | B�� | a��ʱ��ӦY����þ�������� | ||
| C�� | b���ʾ��ʱ����ҺpH��� | D�� | c���ʾ��ʱ��Ӧ���� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
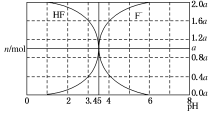 25��ʱ���� 2a mol•L-1 NaOH ��Һ�ζ� 1.0L 2a mol•L-1�������Һ���õ����Һ�� HF��F-�����ʵ�������Һ pH �ı仯��ͼ��ʾ������˵����ȷ���ǣ�������
25��ʱ���� 2a mol•L-1 NaOH ��Һ�ζ� 1.0L 2a mol•L-1�������Һ���õ����Һ�� HF��F-�����ʵ�������Һ pH �ı仯��ͼ��ʾ������˵����ȷ���ǣ�������| A�� | pH=3 ʱ����Һ�У�c��Na+����c��F-�� | |
| B�� | c��F-����c��HF��ʱ����Һһ���ʼ��� | |
| C�� | pH=4 ʱ����Һ�У�c��HF��+c��Na+��+c��H+��-c��OH-����2a mol?L-1 | |
| D�� | pH=3.45 ʱ��NaOH ��Һǡ���� HF ��ȫ��Ӧ |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
�鿴�𰸺ͽ���>>
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com