
| A. | 55 g•mol-1 | B. | 96 g•mol-1 | C. | 108 g•mol-1 | D. | 110 g•mol-1 |
 一诺书业暑假作业快乐假期云南美术出版社系列答案
一诺书业暑假作业快乐假期云南美术出版社系列答案科目:高中化学 来源: 题型:选择题
| A. | 常温常压下,17g甲基(-14CH3)所含中子数为8NA | |
| B. | 标准状况下,22.4L盐酸含有NA个HCl分子 | |
| C. | 常温常压下,0.3molCl2通入水中,充分反应后转移电子数目为0.3 NA | |
| D. | 1.0L1.0mo1•L1的NaAlO2水溶液中含有的氧原子数为2NA |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 2.3 g钠由原子变成离子时,失去的电子数为0.1NA | |
| B. | 0.2NA个HNO3分子与19.6 g H3PO4含有相同的氧原子数 | |
| C. | 28 g氮气所含的原子数为NA | |
| D. | NA个氧分子与NA个氢分子的质量比为8:1 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 蒸馏 | B. | 升华 | C. | 过滤 | D. | 蒸发 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 全部 | B. | ①和③ | C. | ②和③ | D. | ②③④ |
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
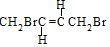 .
.查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 标准状况下11.2L氯气 | B. | 17g氨气(NH3) | ||
| C. | 0.8mol氧气 | D. | 1.204×1024个H2O分子 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | HX是弱酸 | B. | 离子浓度:c(Z-)>c(Y-)>c(X-) | ||
| C. | 电离常数:K(HZ)>K(HY) | D. | c(X-)=c(Y-)+c(HY)=c(Z-)+c(HZ) |
查看答案和解析>>
科目:高中化学 来源: 题型:实验题
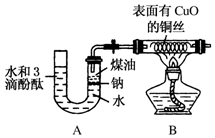 某课外活动小组为了检验钠与水反应的产物,设计如图装置(夹持装置省略).首先在U形管内加入少量煤油和几粒钠块,再从U形管高端加入水(含有酚酞),赶出空气,一会儿点燃酒精灯加热铜丝.
某课外活动小组为了检验钠与水反应的产物,设计如图装置(夹持装置省略).首先在U形管内加入少量煤油和几粒钠块,再从U形管高端加入水(含有酚酞),赶出空气,一会儿点燃酒精灯加热铜丝.查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com