
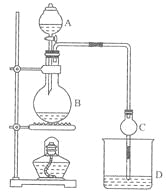
【题目】(11分)某课外小组设计的实验室制取乙酸乙酯的装置如图14-2所示,A中放有浓硫酸,B中放有乙醇、无水醋酸钠,D中放有饱和碳酸钠溶液。
已知①无水氯化钙可与乙醇形成难溶于水的CaCl2·6 C2H50H ②有关有机物的沸点:
试剂 | 乙醚 | 乙醇 | 乙酸 | 乙酸乙酯 |
沸点/℃ | 34.7 | 78.5 | 118 | 77.1 |
请回答:
(1)浓硫酸的作用是 ;若用同位素180示踪法确定反应产物水分子中氧原子的提供者,写出能表示180位置的化学方程式: 。
(2)球形干燥管C的作用是 。若反应前向D中加入几滴酚酞,溶液呈红色,产生此现象的原因是(用离子方程式表示) ;反应结束后D中的现象是 .
(3)从D中分离出的乙酸乙酯中常含有一定量的乙醇、乙醚和水,应先加入无水氯化钙,分离出 (填物质名称);再加入(此空从下列选项中选择,填编号) ,然后进行蒸馏,收集77℃左右的馏分,以得较纯净的乙酸乙酯。
A.五氧化二磷 | B.碱石灰 | C.无水硫酸钠 | D.生石灰 |
【答案】(1)制乙酸、催化剂、脱水剂;CH3COOH+CH3CH218OH![]() CH3CO18OC2H5+H2O;(2)防止倒吸、冷凝;CO32-+H2O
CH3CO18OC2H5+H2O;(2)防止倒吸、冷凝;CO32-+H2O![]() HCO3-+OH-;溶液分层,上层无色油体液体,下层溶液颜色变浅;(3)乙醇和水;C;
HCO3-+OH-;溶液分层,上层无色油体液体,下层溶液颜色变浅;(3)乙醇和水;C;
【解析】
试题(1) 硫酸与乙酸钠反应生成乙酸,乙酸与乙醇反应需浓硫酸作催化剂,该反应为可逆反应,浓硫酸吸水利于平衡向生成乙酸乙酯方向移动;乙醇、乙酸在浓硫酸的作用下发生酯化反应生成乙酸乙酯和水,反应中酸脱羟基醇脱氢。
(2) 圆底烧瓶受热不均,导管口伸入液面下可能发生倒吸。D溶液是饱和碳酸钠,碳酸根离子水解,溶液呈碱性;乙酸乙酯不溶于饱和碳酸钠溶液,密度比水小,溶液分层,上层无色油体液体,乙酸和碳酸钠反应。
(3)无水氯化钙吸收能吸收乙醇,硫酸钠除去水,然后进行蒸馏,得到较纯净的乙酸乙酯。
解析:(1) 硫酸与乙酸钠反应生成乙酸,乙酸与乙醇反应需浓硫酸作催化剂,该反应为可逆反应,浓硫酸吸水利于平衡向生成乙酸乙酯方向移动,浓硫酸的作用是制备乙酸、催化剂、吸水剂;乙醇、乙酸在浓硫酸的作用下发生酯化反应生成乙酸乙酯和水,反应中酸脱羟基醇脱氢,方程式为![]() 。
。
(2) 圆底烧瓶受热不均,球形干燥管体积大,可以防止倒吸,同时起冷凝作用。D溶液是饱和碳酸钠,碳酸根离子水解:CO32-+H2O ![]() HCO3-+OH-,溶液呈碱性,所以加入几滴酚酞,溶液呈红色;乙酸乙酯不溶于饱和碳酸钠溶液,密度比水小,溶液分层,上层无色油体液体,乙酸和碳酸钠反应而使溶液红色变浅。
HCO3-+OH-,溶液呈碱性,所以加入几滴酚酞,溶液呈红色;乙酸乙酯不溶于饱和碳酸钠溶液,密度比水小,溶液分层,上层无色油体液体,乙酸和碳酸钠反应而使溶液红色变浅。
(3)无水氯化钙吸收能吸收乙醇,所以先加入无水氯化钙,分离出乙醇;再加入无水硫酸钠除水,然后进行蒸馏,收集77℃左右的馏分,以得较纯净的乙酸乙酯。


 心算口算巧算一课一练系列答案
心算口算巧算一课一练系列答案科目:高中化学 来源: 题型:
【题目】用下列实验装置进行相应实验,设计正确且能达到实验目的的是
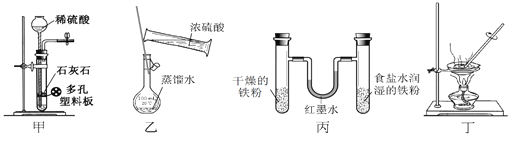
A. 甲用于实验室制取少量CO2 B. 乙用于配制一定物质的量浓度的硫酸
C. 丙用于模拟生铁的电化学腐蚀 D. 丁用于蒸干A1Cl3溶液制备无水AlC13
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】实验室有一未知浓度的盐酸,某同学在实验室中进行实验测定盐酸的浓度。请完成下列填空:
配制100mL0.10molL-1NaOH标准溶液。需用托盘天平称量___g的氢氧化钠固体。
取20.00mL待测盐酸放入锥形瓶中,并滴加 2~3滴酚酞作指示剂,用配制的标准 NaOH溶液进行滴定。重复上述滴定操作 2~3次,记录数据如下:
滴定次数 | 待测盐酸的体积/mL | 0.10 mol/L NaOH 溶液的体积/mL | |
滴定前刻度 | 滴定后刻度 | ||
第一次 | 20.00 | 2.00 | 28.15 |
第二次 | 20.00 | 1.50 | 29.50 |
第三次 | 20.00 | 0.20 | 26.55 |
①该实验滴定达到终点的标志是_________
②根据上述数据,可计算出该盐酸的浓度约为______。(保留两位有效数字)
③在上述实验中,下列操作(其他操作正确)会造成测定结果偏高的有_______。(双选)
A 滴定终点读数时俯视读数 B 酸式滴定管使用前,水洗后未用待测盐酸润洗
C 锥形瓶水洗后未干燥 D 碱式滴定管尖嘴部分有气泡,滴定后消失
E 称量NaOH 固体时,混入少量KOH杂质
④现用以上实验配制的0.10molL-1NaOH溶液滴定未知浓度的CHCOOH溶液,反应恰好完全时,下列叙述中正确的是_____
A 溶液呈中性,可选用甲基橙或酚酞作指示剂
B 溶液呈中性,只能选用石蕊作指示剂
C 溶液呈碱性,可选用甲基橙或酚酞作指示剂
D 溶液呈碱性,只能选用酚酞作指示剂
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】高能LiFePO4电池,多应用于公共交通。电池中间是聚合物的隔膜, 主要作用是在反应过程中只让Li+通过。结构如图所示。
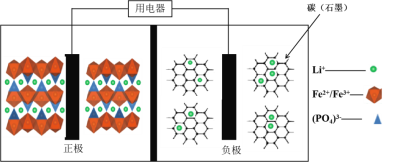
原理如下:(1-x)LiFePO4+xFePO4+LixCn![]() LiFePO4+nC。
LiFePO4+nC。
下列说法不正确的是( )
A. 放电时,正极电极反应式:xFePO4+xLi++xe-===xLiFePO4
B. 放电时,电子由负极经导线、用电器、导线到正极
C. 充电时,阴极电极反应式:xLi++xe-+nC===LixCn
D. 充电时,Li+向左移动
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】能表示H2(g)+ I2(g)![]() 2HI(g)已经达到平衡状态的标志是( )
2HI(g)已经达到平衡状态的标志是( )
①c(H2)=c(I2)=c(HI)时
②c(H2):c(I2):c(HI)=1:1:2时
③c(H2)、c(I2)、c(HI)不再随时间而改变
④单位时间内生成nmolH2的同时生成2nmolHI
⑤单位时间内生成nmolH2的同时生成nmolI2
⑥反应速v(H2)=v(I2)=1/2v(HI)
⑦一个H-H键断裂的同时有两个H-I键断裂
⑧温度和体积一定时,容器内压强不再变化
⑨温度和体积一定时,混合气体的颜色不再变化
⑩温度和压强一定时,混合气体的密度不再变化
条件一定,混合气体的平均相对分子质量不再变化
A.③④⑦⑨⑩B.③④⑦⑨C.②③④⑦⑨D.②③④⑥⑦⑨
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在一定温度下,改变反应物中n(SO2)对反应2SO2(g)+O2(g)2SO3(g) △H<0的影响如图所示,下列说法正确的是( )
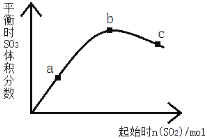
A. 反应b、c点均为平衡点,a点未达平衡且向正反应方向进行
B. a、b、c三点中,a点时SO2的转化率最高
C. 上述图象可以得出SO2的含量越高得到的混合气体中SO3的体积分数越高
D. a、b、c三点的平衡常数Kb>Kc>Ka
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列水解方程式的书写不正确的是( )
A.NH4++H2O![]() NH3·H2O+H+
NH3·H2O+H+
B.S2-+2H2O![]() H2S+2OH-
H2S+2OH-
C.CH3COONa+H2O![]() CH3COOH+NaOH
CH3COOH+NaOH
D.MgCO3 + H2O![]() Mg(OH)2 + CO2
Mg(OH)2 + CO2
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在一定温度下,向2 L恒容密闭容器中充入1 mol A,发生A(g)![]() B(g) + C(g)反应。反应过程中c(C) 随时间变化的曲线如下图所示,下列说法不正确的是
B(g) + C(g)反应。反应过程中c(C) 随时间变化的曲线如下图所示,下列说法不正确的是

A.反应在0 ~50 s的平均速率v(C) =1.6×10-3mol/(L·s)
B.该温度下,反应的平衡常数K = 0.025
C.保持其他条件不变,升高温度,平衡时c(B)=0.11mol/L,则该反应的ΔH<0
D.反应达平衡后,再向容器中充入1 mol A,该温度下再达到平衡时,0.1 mol/L<c(C)<0.2 mol/L
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】已知:2X(g)+Y(g)2Z(s) △H= -M kJ·mol-1。T℃,将2 mol X(g)和1 mol Y(g)加入体积为1L的恒容密闭容器中进行反应, 10 min后达到平衡,生成0.2 mol Z,共放出热量N kJ,下列说法不正确的是
A.其他条件不变,压缩容器,逆反应速率不变
B.在10 min内,X的反应速率为0.02 mol·L-1·min-l
C.在5 min末,X、Y的转化率不相等
D.在0~10 min内,Y的反应速率为![]() mol·L-1·min-l
mol·L-1·min-l
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com