
在其他条件不变时,改变某一条件对A2(g)+3B2(g) 2AB3(g)化学平衡状态的影响,得到如图所示的变化规律(图中T表示温度)。下列结论正确的是
2AB3(g)化学平衡状态的影响,得到如图所示的变化规律(图中T表示温度)。下列结论正确的是

A.a、c两点A2的转化率相等
B.正反应一定是吸热反应,且T2>T1
C.b点时,平衡体系中A、B原子数之比为1:3
D.向a点的平衡体系中加入A2,可达到b点的平衡状态
 快乐暑假暑假能力自测中西书局系列答案
快乐暑假暑假能力自测中西书局系列答案科目:高中化学 来源: 题型:
 工业上一般在密闭容器中采用下列反应合成甲醇:CO(g)+2H2(g)?CH30H(g)
工业上一般在密闭容器中采用下列反应合成甲醇:CO(g)+2H2(g)?CH30H(g)| 1 |
| 2 |
| n(H2) |
| n(CH3OH) |
查看答案和解析>>
科目:高中化学 来源: 题型:
(1)当上述系统达到平衡时,O2和NO2的物质的量分别为n(O2)=0.1 mol、n(NO2)=3.6 mol,则此时SO3气体的物质的量为______________。
(2)当上述系统达到平衡时,欲求其混合气体的平衡组成,则至少还需要知道两种气体的平衡浓度,但这两种气体不能同时是SO3和______________,或NO和______________(填它们的分子式)。
(3)在其他条件不变的情况下,若改为起始时在1 L容器中充入2 mol NO2和2 mol SO2,则上述两反应达到平衡时,c平(SO2)=______________mol·L-1。
查看答案和解析>>
科目:高中化学 来源: 题型:
(7分)一定条件下,在体积为3L的密闭容器中,一氧化碳与氢气反应生成甲醇(催化剂为Cu2O/ZnO):CO(g)+2H2(g)CH3OH(g) ΔH< 0
根据题意完成下列各题:
(1)反应达到平衡时,平衡常数表达式K = 。
(2)其它条件不变,仅把温度改为500℃,请在下图上画出此温度下甲醇的物质的量随反应时间变化的示意图。
(3)升高温度,K值 (填“增大”、“减小”或“不变”),增大压强,
K值 (填“增大”、“减小”或“不变”)。
(4)在300℃,从反应开始到平衡,氢气的平均反应速率v(H2)=
(5)在其他条件不变的情况下,对处于B点的体系体积压缩到原来的1/2,下列有关该体系的说法正确的是( )
a.氢气的浓度减少 b.正反应速率加快,逆反应速率减小
c.甲醇的物质的量增加 d.重新平衡时n(H2)/n(CH3OH)减小
查看答案和解析>>
科目:高中化学 来源:2010—2011学年江西省白鹭洲中学高二下学期期中考试化学试卷 题型:填空题
(7分)一定条件下,在体积为3L的密闭容器中,一氧化碳与氢气反应生成甲醇(催化剂为Cu2O/ZnO):CO(g)+2H2(g) CH3OH(g) ΔH< 0
CH3OH(g) ΔH< 0
根据题意完成下列各题:
(1)反应达到平衡时,平衡常数表达式K = 。
(2)其它条件不变,仅把温度改为500℃,请在下图上画出此温度下甲醇的物质的量随反应时间变化的示意图。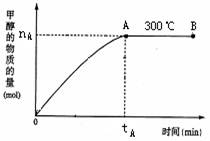
(3)升高温度,K值 (填“增大”、“减小”或“不变”),增大压强,
K值 (填“增大”、“减小”或“不变”)。
(4)在300℃,从反应开始到平衡,氢气的平均反应速率v(H2)=
(5)在其他条件不变的情况下,对处于B点的体系体积压缩到原来的1/2,下列有关该体系的说法正确的是( )
a.氢气的浓度减少 b.正反应速率加快,逆反应速率减小
c.甲醇的物质的量增加 d.重新平衡时n(H2)/n(CH3OH)减小
查看答案和解析>>
科目:高中化学 来源:2012-2013学年江苏省连云港市高三上学期摸底考试化学试卷(解析版) 题型:填空题
(14分)工业上一般在密闭容器中采用下列反应合成甲醇:CO(g)+2H2(g)
 CH30H(g)
CH30H(g)
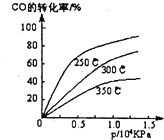
(1)不同温度下的平衡转化率与压强的关系如图所示。
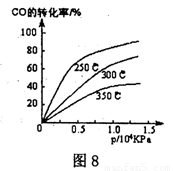
①该反应△H O,△S 0(填“>”或“<”),则该反 自发进行(填“一定能”、“一定不能”、“不一定”)
②实际生产条件控制在250℃、l,3×l04kPa左右,选择此压强的理由是 。
(2)某温度下,将2molCO和6mOlH2充入2L的密闭容器中,充分反应后,达到平衡时测得c(CO)=O.l mol·L -1。
①该反应的平衡常数K= :
②在其他条件不变的情况下,将容器体积压缩到原来的1/2,与原平衡相比,下列有
关说法正确的是 (填序号)。
a.氢气的浓度减少 b.正反应速率加快,逆反应速率也加快
c.甲醇的物质的量增加 d.重新平衡时n(H2)/n(CH30H)增大
③若保持同一反应温度将起始物质改为a mol CO、b mol H2、c mol CH30H,欲使平衡混合物中各组成与原平衡相同,则a、b应满足的关系为 ,且欲使开始时该反应向逆反应方向进行,c的取值范围是 。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com