
 ¶ž¼×ĆŃŹĒŅ»ÖÖÖŲŅŖµÄĒå½ąČ¼ĮĻ£¬Ņ²æÉĢę“ś·śĄū°ŗ×÷ÖĘĄä¼ĮµČ£¬¶Ō³ōŃõ²ćĪŽĘĘ»µ×÷ÓĆ£®¹¤ŅµÉĻæÉĄūÓĆĆŗµÄĘų»Æ²śĪļ£ØĖ®ĆŗĘų£©ŗĻ³É¶ž¼×ĆŃ£®
¶ž¼×ĆŃŹĒŅ»ÖÖÖŲŅŖµÄĒå½ąČ¼ĮĻ£¬Ņ²æÉĢę“ś·śĄū°ŗ×÷ÖĘĄä¼ĮµČ£¬¶Ō³ōŃõ²ćĪŽĘĘ»µ×÷ÓĆ£®¹¤ŅµÉĻæÉĄūÓĆĆŗµÄĘų»Æ²śĪļ£ØĖ®ĆŗĘų£©ŗĻ³É¶ž¼×ĆŃ£®·ÖĪö £Ø1£©ĆŗµÄĘų»ÆŹĒĄūÓĆĆŗÓėĖ®ÕōĘųøßĪĀĢõ¼žŠ”·“Ó¦£¬Éś³ÉCOŗĶH2µÄ¹ż³Ģ£»
£Ø2£©ĆŗµÄĘų»Æ¹ż³ĢÖŠ²śÉśµÄÓŠŗ¦ĘųĢåH2SÓĆNa2CO3ČÜŅŗĪüŹÕ£¬Éś³ÉĮ½ÖÖĖįŹ½ŃĪĪŖĮņĒāĖįÄĘŗĶĢ¼ĖįĒā£»
£Ø3£©¢Ł2H2£Øg£©+CO£Øg£©?CH3OH£Øg£©”÷H=-90.8kJ•mol-1
¢Ś2CH3OH£Øg£©?CH3OCH3£Øg£©+H2O£Øg£©”÷H=-23.5kJ•mol-1
¢ŪCO£Øg£©+H2O£Øg£©?CO2£Øg£©+H2£Øg£©”÷H=-41.3kJ•mol-1
ÓÉøĒĖ¹¶ØĀÉ¢Ś+¢Ū+¢Ł”Į2¼ĘĖć£»ŅŖĢįøßCOµÄ×Ŗ»ÆĀŹ£¬Ó¦Ź¹Ę½ŗāÕżĻņŅĘ¶Æ£»
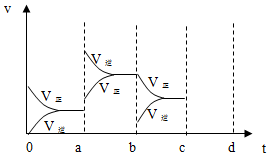
£Ø4£©ŌŚaŹ±æĢ£¬ÕżÄę·“Ó¦ĖŁĀŹ¶¼Ōö“ó£¬ĒŅÄę·“Ó¦ĖŁĀŹ“óÓŚÕż·“Ó¦ĖŁĀŹ£¬¼“Ę½ŗāÄęĻņŅĘ¶Æ£¬æÉĪŖÉżøßĪĀ¶Č£¬ŌŚbŹ±æĢ£¬Õż·“Ó¦ĖŁĀŹ ²»±ä£¬Äę·“Ó¦ĖŁĀŹ¼õŠ”£¬ĒŅÕż·“Ó¦ĖŁĀŹ“óÓŚÄę·“Ó¦ĖŁĀŹ£¬¼“Ę½ŗāÕżĻņŅĘ¶Æ£¬ŅņĪŖ½µµĶÉś³ÉĪļµÄÅØ¶Č£¬Ōö“óŃ¹Ēæ£¬Ę½ŗāÕżĻņŅĘ¶Æ£®
½ā“š ½ā£ŗ£Ø1£©ĆŗµÄĘų»ÆŹĒĄūÓĆĆŗÓėĖ®ÕōĘųøßĪĀĢõ¼žŠ”·“Ó¦£¬Éś³ÉCOŗĶH2µÄ¹ż³Ģ£ŗC+H2O$\frac{\underline{\;øßĪĀ\;}}{\;}$CO+H2£¬
¹Ź“š°øĪŖ£ŗC+H2O$\frac{\underline{\;øßĪĀ\;}}{\;}$CO+H2£»
£Ø2£©ĆŗµÄĘų»Æ¹ż³ĢÖŠ²śÉśµÄÓŠŗ¦ĘųĢåH2SÓĆNa2CO3ČÜŅŗĪüŹÕ£¬Éś³ÉĮ½ÖÖĖįŹ½ŃĪĪŖĮņĒāĖįÄĘŗĶĢ¼ĖįĒā£¬·“Ó¦µÄ»Æѧ·½³ĢŹ½ĪŖ£ŗNa2CO3+H2SØTNaHCO3+NaHS£¬
¹Ź“š°øĪŖ£ŗNa2CO3+H2SØTNaHCO3+NaHS£»
£Ø3£©¢Ł2H2£Øg£©+CO£Øg£©?CH3OH£Øg£©”÷H=-90.8kJ•mol-1
¢Ś2CH3OH£Øg£©?CH3OCH3£Øg£©+H2O£Øg£©”÷H=-23.5kJ•mol-1
¢ŪCO£Øg£©+H2O£Øg£©?CO2£Øg£©+H2£Øg£©”÷H=-41.3kJ•mol-1
ÓÉøĒĖ¹¶ØĀÉ¢Ś+¢Ū+¢Ł”Į2µĆµ½3H2£Øg£©+3CO£Øg£©?CH3OCH3£Øg£©+CO2£Øg£©µÄ”÷H=-246.4kJ•mol-1£¬
Ņ»¶ØĢõ¼žĻĀµÄĆܱÕČŻĘ÷ÖŠ£¬øĆ×Ü·“Ó¦“ļµ½Ę½ŗā£¬·“Ó¦ŹĒ·ÅČČ·“Ó¦£¬·“Ó¦Ē°ŗóĘųĢåĢå»ż¼õŠ”µÄ·“Ó¦£¬ŅŖĢįøßCOµÄ×Ŗ»ÆĀŹ£¬Ę½ŗāÕżĻņ½ųŠŠ£¬
a”¢Õż·“Ó¦ĪŖ·ÅČČ·“Ó¦£¬ÉżøßĪĀ¶Č£¬Ę½ŗāÄęĻņŅĘ¶Æ£¬×Ŗ»ÆĀŹ¼õŠ”£¬¹Źa“ķĪó£»
b”¢¼ÓČė“߻ƼĮ£¬øı䷓ӦĖŁĀŹ²»øıä»ÆŃ§Ę½ŗā£¬×Ŗ»ÆĀŹ²»±ä£¬¹Źb“ķĪó£»
c”¢¼õÉŁCO2µÄÅØ¶Č£¬¼õÉŁÉś³ÉĪļÅضČĘ½ŗāÕżĻņ½ųŠŠ£¬Ņ»Ńõ»ÆĢ¼×Ŗ»ÆĀŹŌö“󣬹ŹcÕżČ·£»
d”¢Ōö¼ÓCOµÄÅØ¶Č£¬ĢįøßĒāĘų×Ŗ»ÆĀŹ£¬Ņ»Ńõ»ÆĢ¼×Ŗ»ÆĀŹ¼õŠ”£¬¹Źd“ķĪó£»
e”¢·ÖĄė³ö¶ž¼×ĆŃ£ØCH3OCH3£©£¬Ę½ŗāÕżĻņ½ųŠŠ£¬Ņ»Ńõ»ÆĢ¼×Ŗ»ÆĀŹŌö“󣬹ŹeÕżČ·£»
¹Ź“š°øĪŖ£ŗ-246.4kJ•mol-1£»c”¢e£»
£Ø4£©øł¾ŻĶ¼¶žæÉÖŖ£¬ŌŚaŹ±æĢ£¬ÕżÄę·“Ó¦ĖŁĀŹ¶¼Ōö“ó£¬ĒŅÄę·“Ó¦ĖŁĀŹ“óÓŚÕż·“Ó¦ĖŁĀŹ£¬¼“Ę½ŗāÄęĻņŅĘ¶Æ£¬ŅņĪŖ·“Ó¦µÄ”÷H£¼0£¬øł¾ŻÓ°Ļģ»Æѧ·“Ó¦ĖŁĀŹŗĶ»ÆŃ§Ę½ŗāµÄĢõ¼žæÉÖŖ£¬a”«b¹ż³ĢÖŠøıäµÄĢõ¼žæÉÄÜŹĒÉżĪĀ£»ŌŚbŹ±æĢ£¬Õż·“Ó¦ĖŁĀŹ ²»±ä£¬Äę·“Ó¦ĖŁĀŹ¼õŠ”£¬ĒŅÕż·“Ó¦ĖŁĀŹ“óÓŚÄę·“Ó¦ĖŁĀŹ£¬¼“Ę½ŗāÕżĻņŅĘ¶Æ£¬øł¾ŻÓ°Ļģ»Æѧ·“Ó¦ĖŁĀŹŗĶ»ÆŃ§Ę½ŗāµÄĢõ¼žæÉÖŖ£¬b”«c¹ż³ĢÖŠøıäµÄĢõ¼žæÉÄÜŹĒ¼õŠ”SO3µÄÅØ¶Č£¬ŌŚb”«c¹ż³Ģŗó£¬ČōŌö“óŃ¹Ēæ£¬ÕżÄę·“Ó¦ĖŁĀŹ¶¼»įŌö“ó£¬ÓÉÓŚøĆ·“Ó¦ĪŖĢå»żĖõŠ”µÄ·“Ó¦£¬ĖłŅŌĘ½ŗāÕżĻņŅĘ¶Æ£¬øł¾ŻŃ¹Ēæ¶Ō»Æѧ·“Ó¦ĖŁĀŹµÄÓ°ĻģæÉ»³öĻą¹ŲµÄĶ¼ĪŖ£ŗ £¬
£¬
¹Ź“š°øĪŖ£ŗÉżĪĀ£»¼õŠ”SO3µÄÅØ¶Č£» £®
£®
µćĘĄ ±¾Ģāæ¼²é½ĻĪŖ×ŪŗĻ£¬Éę¼°ČČ»Æѧ·½³ĢŹ½µÄŹéŠ“·½·ØŗĶøĒĖ¹¶ØĀɵļĘĖć”¢»ÆŃ§Ę½ŗāµÄÓ°ĻģŅņĖŲµÄĻą¹ŲÖŖŹ¶£¬²ąÖŲæ¼²éѧɜµÄ·ÖĪöÄÜĮ¦£¬×¢Ņā°ŃĪÕøĒĖ¹¶ØĀɵÄŅżÓĆŅŌ¼°Ķ¼ĻóµÄ·ÖĪö£¬°ŃĪÕĶā½ēĢõ¼ž¶ŌĘ½ŗāŅĘ¶ÆµÄÓ°Ļģ£¬ÄѶČÖŠµČ£®


 ŌĶĮæģ³µĻµĮŠ“š°ø
ŌĶĮæģ³µĻµĮŠ“š°ø
| Äź¼¶ | øßÖŠæĪ³Ģ | Äź¼¶ | ³õÖŠæĪ³Ģ |
| øßŅ» | øßŅ»Ćā·ŃæĪ³ĢĶĘ¼ö£” | ³õŅ» | ³õŅ»Ćā·ŃæĪ³ĢĶĘ¼ö£” |
| ø߶ž | ø߶žĆā·ŃæĪ³ĢĶĘ¼ö£” | ³õ¶ž | ³õ¶žĆā·ŃæĪ³ĢĶĘ¼ö£” |
| øßČż | øßČżĆā·ŃæĪ³ĢĶĘ¼ö£” | ³õČż | ³õČżĆā·ŃæĪ³ĢĶĘ¼ö£” |
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ½ā“šĢā
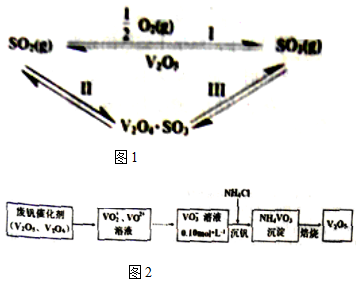
| »Æѧ¼ü | S=O£ØSO2£© | S=O£ØSO3£© | O=O£ØO2£© |
| ÄÜĮæ/kJ | 535 | 472 | 496 |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗŃ”ŌńĢā
| A£® | ³£ĪĀ³£Ń¹ĻĀ£¬23gNO2ŗĶN2O4»ģŗĻĘųĢåÖŠŗ¬OŌ×ÓŹżĪŖNA | |
| B£® | 1mol/L Al2£ØSO4£©3ČÜŅŗÖŠŗ¬SO42-øöŹżĪŖ3NA£¬ŗ¬Al3+øöŹżŠ”ÓŚ2NA | |
| C£® | ŌŚ±ź×¼×“æöĻĀ£¬½«22.4L SO3ČÜÓŚĖ®Åä³É1LČÜŅŗ£¬ĖłµĆČÜŅŗÖŠŗ¬SO42-øöŹżĪŖNA | |
| D£® | ½«1moL ĀČĘųĶØČėµ½×ćĮæĖ®ÖŠ£¬ŌņN£ØHClO£©+N£ØCl-£©+N£ØClO-£©ØT2NA |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ½ā“šĢā
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗŃ”ŌńĢā
| A£® | ¢Ś¢Ü¢Ž¢ß¢ą¢į | B£® | ¢Ł¢Ś¢Ü¢Ž¢ß¢ą¢į | C£® | ¢Ł¢Ū¢Ü¢Ż¢Ž¢ą¢ā | D£® | ¢Ł¢Ś¢Ü¢ą¢į |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗĢīæÕĢā
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗĢīæÕĢā
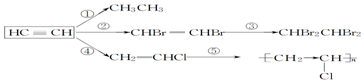
 £¬¼Ó¾Ū·“Ó¦£®
£¬¼Ó¾Ū·“Ó¦£®²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗŃ”ŌńĢā
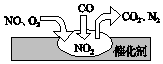 Ėę×ÅĪŅ¹śĘū³µÄźĻśĮæµÄ“ó·łŌö¼Ó£¬æÕĘų»·¾³ŹÜµ½ĮĖŗÜ“óµÄĪŪČ¾£®Ęū³µĪ²Ęų×°ÖĆĄļ£¬ĘųĢåŌŚ“߻ƼĮ±ķĆęĪüø½Óė½āĪü×÷ÓĆµÄ¹ż³ĢČēĶ¼ĖłŹ¾£¬ĻĀĮŠĖµ·ØÕżČ·µÄŹĒ£Ø””””£©
Ėę×ÅĪŅ¹śĘū³µÄźĻśĮæµÄ“ó·łŌö¼Ó£¬æÕĘų»·¾³ŹÜµ½ĮĖŗÜ“óµÄĪŪČ¾£®Ęū³µĪ²Ęų×°ÖĆĄļ£¬ĘųĢåŌŚ“߻ƼĮ±ķĆęĪüø½Óė½āĪü×÷ÓĆµÄ¹ż³ĢČēĶ¼ĖłŹ¾£¬ĻĀĮŠĖµ·ØÕżČ·µÄŹĒ£Ø””””£©| A£® | ·“Ó¦ÖŠNOĪŖŃõ»Æ¼Į£¬N2ĪŖŃõ»Æ²śĪļ | |
| B£® | Ęū³µĪ²ĘųµÄÖ÷ŅŖĪŪČ¾³É·Ö°üĄØCO”¢NOŗĶN2 | |
| C£® | NOŗĶO2±ŲŠėŌŚ“߻ƼĮ±ķĆę²ÅÄÜ·“Ó¦ | |
| D£® | “ß»Æ×Ŗ»Æ×Ü»Æѧ·½³ĢŹ½ĪŖ2NO+O2+4CO=4CO2+N2 |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ½ā“šĢā
| Źµ Ńé ¢ń | ²Ł×÷ | ĻÖĻó |
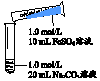 | 1”¢»ģŗĻŗó³öĻÖ°×É«Šõד³Įµķ£¬Õńµ“£¬²æ·Ö³Įµķ³Ź»ŅĀĢÉ«£¬ĪŽĘųÅŻ²śÉś 2”¢·ÅÖĆ5-8·ÖÖÓ£¬»ŅĀĢÉ«³ĮµķÖš½„Ōö¶ą£¬×īÖÕ±ä³ÉŗģŗÖÉ« |
| ŹµŃé¢ņ | ²Ł×÷ | ĻÖĻó |
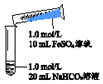 | 1”¢»ģŗĻŗó£¬ŹŌ¹ÜÖŠ³öĻÖ°×É«æÅĮ£×“»ė×Ē£¬Ę¬æĢŗóÓŠ“óĮæĘųÅŻ²śÉś 2”¢Õńµ“£¬Õ³ø½ŌŚŹŌ¹ÜÄŚ±ŚµÄ°×É«æÅĮ£×“»ė×Ē±äŗģ×ŲÉ«£¬ĒŅŌ½Ą“Ō½¶ą£»20·ÖÖÓŗ󣬰×É«»ė×ĒĆ÷ĻŌ³Į½µ |
| ŹµŃé¢ņ | ²Ł×÷ | ĻÖĻó |
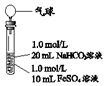 | 1”¢»ģŗĻŗó£¬ŹŌ¹ÜÖŠ³öĻÖ°×É«æÅĮ£×“»ė×Ē£¬Ę¬æĢŗóÓŠ“óĮæĘųÅŻ²śÉś 2”¢Ņ»¶ĪŹ±¼äŗ󽫓ųÓŠĘųĒņ£ØÅž”æÕĘų£©µÄ½ŗČūČū½ōŹŌ¹Ü£¬Õńµ“ŗó·ÅÖĆ5Š”Ź±£¬ĘųĒņÅņÕĶ£¬ŹŌ¹ÜÖŠ³ĮµķĪļŹ¼ÖÕ±£³Ö°×É« |
²éæ““š°øŗĶ½āĪö>>
°Ł¶ČÖĀŠÅ - Į·Ļ°²įĮŠ±ķ - ŹŌĢāĮŠ±ķ
ŗž±±Ź”»„ĮŖĶųĪ„·ØŗĶ²»Į¼ŠÅĻ¢¾Ł±ØĘ½ĢØ | ĶųÉĻÓŠŗ¦ŠÅĻ¢¾Ł±Ø×ØĒų | µēŠÅÕ©Ę¾Ł±Ø×ØĒų | É꥜Ź·ŠéĪŽÖ÷ŅåÓŠŗ¦ŠÅĻ¢¾Ł±Ø×ØĒų | ÉęĘóĒÖČؾŁ±Ø×ØĒų
Ī„·ØŗĶ²»Į¼ŠÅĻ¢¾Ł±Øµē»°£ŗ027-86699610 ¾Ł±ØÓŹĻä£ŗ58377363@163.com