

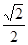 a(2分)
a(2分) 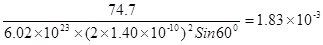 (2分,列式1分)
(2分,列式1分)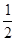 (5+3-4×2)=4,且没有孤电子对,所以其空间构型是正四面体;
(5+3-4×2)=4,且没有孤电子对,所以其空间构型是正四面体;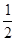 a,距离最近的两个阳离子核间的距离是距离最近的氧离子和镍离子距离的
a,距离最近的两个阳离子核间的距离是距离最近的氧离子和镍离子距离的 倍,所以其距离是
倍,所以其距离是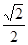 acm;
acm;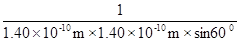 ,每个氧化镍的质量=
,每个氧化镍的质量=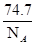 g,所以每平方米含有的氧化镍质量=
g,所以每平方米含有的氧化镍质量=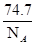 ×
×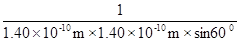 =
=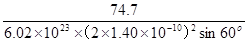 =1.83×10-3
=1.83×10-3

 期末集结号系列答案
期末集结号系列答案科目:高中化学 来源:不详 题型:填空题

查看答案和解析>>
科目:高中化学 来源:不详 题型:填空题

查看答案和解析>>
科目:高中化学 来源:不详 题型:填空题

查看答案和解析>>
科目:高中化学 来源:不详 题型:填空题

查看答案和解析>>
科目:高中化学 来源:不详 题型:填空题
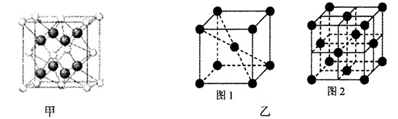
| 元素 | 结构或性质信息 |
| A | 原子核外有一个未成对电子,其氢化物与水分子间能形成氢键 |
| B | 原子核外M层电子数是N层电子数的4倍 |
| C | 是使用最为广泛的合金的主要成分 |
| D | 原子各内层电子均已饱和,最外层电子数为1 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:填空题
| 元素 | 相关信息 |
| X | X元素形成的一种同素异形体是天然晶体中硬度最大的单质 |
| Y | 常温常压下,Y单质是淡黄色固体,用于制造黑火药 |
| Z | Z的基态原子核外有3个能级上有电子,且有3个单电子 |
| W | W元素形成的双原子分子,常温下为黄绿色气体,一种常见工业原料 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:填空题
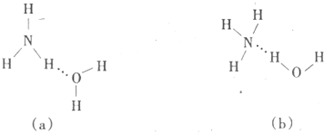
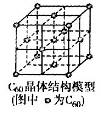
查看答案和解析>>
科目:高中化学 来源:不详 题型:填空题
 )。
)。查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com