
����Ŀ��̼���̣�MnCO3��������ĸ�����ǿ���Բ��ϣ�Ҳ���Ʊ�Mn2O3��MnO2���̵����������Ҫԭ�ϣ��㷺���ڵ��ӡ�������ҽҩ����ҵ��
��1����ҵ���Ʊ�����ʽΪ��MnSO4+2NH4HCO3=MnCO3��+��NH4��2SO4+CO2��+H2O����Ӧ��ͨ��������Թ�����NH4HCO3���ҿ�����Һ��pHΪ6.8��7.4�������Թ�����NH4HCO3��Ŀ���� ��
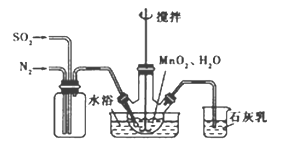
��2��ʵ����ģ�ҵ���������Ʊ�������װ����ͼ
��ʯ������뷴Ӧ�Ļ�ѧ����ʽΪ ��
����Ӧ�����У�ΪʹSO2������ת����ȫ����ͨ��SO2��N2����һ�������ı��ҺͶ�ϵ������£��ɲ�ȡ�ĺ�����ʩ�� ��
��3��MnCO3�ڿ����м�����ת��Ϊ��ͬ��̬���̵�������������������¶ȵı仯��ͼ��ʾ����300��ʱ��ʣ�������n(Mn����n(O��Ϊ ��ͼ�е�D��Ӧ����ijɷ�Ϊ ���ѧʽ����
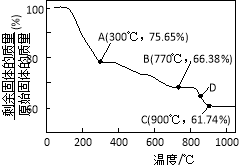
���𰸡���1�������Թ�����NH4HCO3�����MnSO4��ת������ʹMnCO3������ȫ
��2����Ca(OH��2ʮSO2=CaSO3+H2O��
�������ʵ����¶ȡ�����ͨ�˻������
��1��2 (3���� Mn3O4��MnO(����������������
��������
�����������1��MnSO4+2NH4HCO3=MnCO3��+��NH4��2SO4+CO2��+H2O����Ӧ��ͨ��������Թ�����NH4HCO3���ҿ�����Һ��pHΪ6.8��7.4�������Թ�����NH4HCO3��Ŀ�������MnSO4��ת���ʣ�ʹMnCO3������ȫ��
��2�������Ʊ�������װ��ͼ��
��ʯ�����Ƿ�ֹ����������Ⱦ���������뷴Ӧ�Ļ�ѧ����ʽΪCa(OH��2ʮSO2=CaSO3+H2O��
����Ӧ�����У�ΪʹSO2������ת����ȫ����ͨ��SO2��N2����һ�������ı��ҺͶ�ϵ������£��ɲ�ȡ�ĺ�����ʩ�п����ʵ����¶ȡ�����ͨ�˻��������
��3������MnCO3�����ʵ���Ϊ1 mol��������Ϊ115 g
��A��ʣ���������Ϊ115 g��75.65%��87 g
���ٵ�����Ϊ115 g��87 g��28 g
��֪MnCO3ʧȥ�����ΪCO
��ʣ�����ijɷ�ΪMnO2
��C��ʣ���������Ϊ115 g��61.74%��71 g
����Ԫ���غ�֪m(Mn����55 g����m(O ��1��71 g��55 g��16 g
��n(Mn����n(O����![]() ��
��![]() ��1��1
��1��1
��ʣ�����ijɷ�ΪMnO
ͬ����B��ʣ���������Ϊ115 g��66.38%��76.337 g
��m(Mn����55 g����m(O ��2��76.337 g��55 g��21.337 g
��n(Mn����n(O����![]() ��
��![]() ��3��4
��3��4
��ʣ�����ijɷ�ΪMn3O4
��D�����B��C֮�䣬��D���Ӧ����ijɷ�ΪMn3O4��MnO�Ļ������



| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ������˵����������
A. �������Ʒ��ڿ����б��
B. ȡ��ʣ��Ľ����Ʋ��ܷŻ�ԭ�Լ�ƿ��
C. ����������Һ����ʢװ�������IJ����Լ�ƿ�б���
D. ʢ��FeSO4��Һ���Լ�ƿ��Ҫ����м
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��100mL 4mol/L ϡ������2gп����Ӧ����һ���¶���Ϊ�˼�����Ӧ�����ʣ����ֲ�Ӱ����������������������Ӧ���м��루 ��
A. �����ƹ��� B. ����ͭ���� C. �������Һ D. �Ȼ�����Һ
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����50mL Na2SO4��Na2CO3�Ļ����Һ�м��������BaCl2��Һ���õ�14.51g��ɫ���������ɫ�����м��������ϡHNO3����ַ�Ӧ�������ٵ�4.66g���������������
��1��ԭ�����Һ��Na2SO4�����ʵ���Ũ���Ƕ��٣�
��2�������������ڱ�״���µ�����Ƕ��٣�
��3��ԭ��Һ��Na+���ʵ���Ũ���Ƕ��٣�
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��Ϊ�˼���ij����NaHCO3���ʵ�Na2CO3��Ʒ�Ĵ��ȣ��ֽ�w1 g��Ʒ���ȣ���������Ϊw2 g�������Ʒ��Na2CO3�Ĵ���(��������)��
A. ![]() B.
B. ![]() C.
C. ![]() D.
D. ![]()
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ������˵����ȷ����
A. 1molO2��������32g/mol B. H2��Ħ��������2g
C. 1molH+��������1g D. ��ԭ�Ӷ��ԣ�Ħ�������������ԭ������
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����1����������CO��SO2�ֱ�װ��ͬ��ͬ���������������������֮�� ��������ԭ��֮�� ���ܶ�֮�� ��ѹǿ֮�� ��
��2������״����224L��HCl����1000gˮ����ܶ�Ϊ1.23g/cm3��Һ��������Һ�����ʵ���Ũ��Ϊ________��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����֪Ư��Һ�Ǻ���NaClO��NaCl�����Һ(pH>7��,���й��ڸ���Һ˵����ȷ����
A������Һ�У�Ag+��K+��NO3��Mg2+���Դ�������
B������Һ�У�H+��NH4+��SO42��I ���Դ�������
C�������Һ�м���Ũ���ᣬÿ����1molCl2��ת�Ƶ���ԼΪ6.02��1023
D�������Һ�е�������Na2SO3��Һ����Ӧ�����ӷ���ʽΪ��SO32+ClO == Cl+ SO42
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ������ģ�ͷֱ��ʾC2H2��S8��SF6�Ľṹ������˵���������ǣ� ��
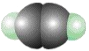

A��32 g S8�������0.125 mol ����
B��SF6���ɼ��Լ����ɵķǼ��Է���
C��1 mol C2H2��������3 mol ������2 mol ����
D��1 mol S8���8 mol S��S��
�鿴�𰸺ͽ���>>
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com