
| C | ||
| A | R | B |
| D |
| A. | 4Z | B. | 4Z+10 | C. | 4Z+14 | D. | 4Z+5 |
分析 如果R第三周期Mg元素,D和R原子序数相差8,C和R原子序数相差8;
如果R是第三周期第IIIA族到第VIIA族元素,D和R原子序数相差18,C和R原子序数相差8;
如果R是第四周期Ca元素,C和R原子序数相差8,D和R原子序数相差18;
如果R是第四周期第IIIA族到第VIIA族元素,C和R原子序数相差18、R和D原子序数相差18;
如果这几种元素都是副族元素,且R是第五周期第IVB族到第VIII族、第IB族时,C和R原子序数相差18、R和D原子序数相差32.
解答 解:如果R第三周期Mg元素,D和R原子序数相差8,C和R原子序数相差8,则A、B、C、D四种元素的原子序数之和为4Z;
如果R是第三周期第IIIA族到第VIIA族元素,D和R原子序数相差18,C和R原子序数相差8,则A、B、C、D四种元素的原子序数之和为4Z+10;
如果R是第四周期Ca元素,C和R原子序数相差8,D和R原子序数相差18,则A、B、C、D四种元素的原子序数之和为4Z+10;
如果R是第四周期第IIIA族到第VIIA族元素,C和R原子序数相差18、R和D原子序数相差18,A、B、C、D四种元素的原子序数之和为4Z;
如果这几种元素都是副族元素,且R是第五周期第IVB族到第VIII族、第IB族时,C和R原子序数相差18、R和D原子序数相差32,则A、B、C、D四种元素的原子序数之和为4Z+14,
通过以上分析知,A、B、C、D四种元素原子序数之和不可能为4Z+5,
故选D.
点评 本题考查元素周期表结构及元素在周期表中的位置,侧重考查学生分析问题能力、发散思维能力,采用假设方法对元素进行分析,注意:同一主族相邻元素原子序数之差,难度较大.


科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
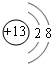 、
、 .
.查看答案和解析>>
科目:高中化学 来源: 题型:选择题

| A. | X、Y、Z元素分别为N、P、O | |
| B. | 白格中都是主族元素,灰格中都是副族元素 | |
| C. | 原子半径:Z>X>Y | |
| D. | X、Y、Z的气态氢化物中最稳定的是:X的氢化物 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:解答题

查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | CH2=CH2+Br2→BrCH2CH2Br | |
| B. | 2CH3CH2OH+O2$→_{△}^{催化剂}$2CH3CHO+2H2O | |
| C. | 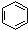 +HNO3$\stackrel{浓硫酸△}{→}$ +HNO3$\stackrel{浓硫酸△}{→}$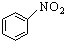 +H2O +H2O | |
| D. | C6H12O6$→_{△}^{催化剂}$2C2H5OH+2CO2↑ |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com