
| 实验步骤 | 实验操作 | 实验现象 |
| Ⅰ | 将反应后的黑色粉末X(假定成分分布均匀)取出少量,放入另一试管中,加入少量盐酸,微热 | 黑色粉末逐渐溶解,溶液呈浅绿色;有少量气泡产生 |
| Ⅱ | 向实验Ⅰ中得到的溶液滴加几滴KSCN溶液,振荡 | 溶液没有出现红色 |
分析 (1)Fe粉与水蒸气在高温下反应生成Fe3O4和氢气;
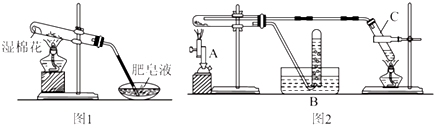
(2)装置C用于制备水蒸气;
(3)应先提供水蒸气,排除装置内的空气;
(4)氢气易燃烧,应避免爆炸;
(5)如铁粉过量,则不能生成Fe3+;
(6)铁和水蒸气反应生成四氧化三铁和氢气,结合固体质量分析判断生成物成分.
解答 解:(1)酒精灯的加热温度400~500℃,适用于温度不需太高的实验,所以本实验中产物为FeO和氢气,方程式为Fe+H2O(g)$\frac{\underline{\;高温\;}}{\;}$FeO+H2,
故答案为:Fe+H2O(g)$\frac{\underline{\;高温\;}}{\;}$FeO+H2;
(2)反应物为铁和水蒸气,则装置C用于制备水蒸气,故答案为:制取水蒸气;
(3)反应时,应先点燃酒精灯,为反应体系提供稳定的水蒸气气流,故答案为:酒精灯;
(4)水蒸气与铁粉在酒精喷灯加强热下生成四氧化三铁和氢气;因为氢气在空气中比重达到一定程度,遇明火就会发生爆炸,所以用装置B收集氢气,
故答案为:氢气遇明火可能发生爆炸;
(5)有气泡冒出,说明铁有剩余,故可能是剩余的铁将三价铁离子还原为亚铁离子,所以不能证明产物为氧化亚铁,反应的离子方程式为Fe+2H+═2Fe2++H2↑,2Fe3++Fe═3Fe2+,
故答案为:Fe+2H+═2Fe2++H2↑,2Fe3++Fe═3Fe2+;
(6)由冷却后的固体消耗FeCl30.08 mol可知剩余Fe为0.04 mol,故氧化物中n(Fe)=$\frac{5.60g}{56g/mol}$-0.04 mol=0.06 mol,n(O)=$\frac{6.88g-5.60g}{16g/mol}$=0.08 mol,即n(Fe):n(O)=3:4,所得固体产物为Fe3O4.
故答案为:Fe3O4.
点评 本题考查性质实验方案的设计,为高频考点,侧重于学生的分析能力、实验能力和计算能力的考查,把握高温下铁与水反应及实验中装置的作用为解答的关键,题目难度中等.


 孟建平小学滚动测试系列答案
孟建平小学滚动测试系列答案科目:高中化学 来源: 题型:推断题
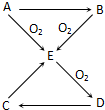 已知A、B、C、D、E五种物质有如图所示的转化关系(部分反应物及反应条件未列出,若解题时需要,可作合理假设),
已知A、B、C、D、E五种物质有如图所示的转化关系(部分反应物及反应条件未列出,若解题时需要,可作合理假设),查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 为控制水浴温度为85~90℃,把温度计插入反应液中 | |
| B. | 为除去阿司匹林中混有的杂质,可在粗产品中加足量NaHCO3溶液、搅拌、过滤、洗涤沉淀,干燥即得精品 | |
| C. | 一定条件下,1mol阿司匹林最多可与2mol的NaOH反应 | |
| D. | 可用FeCl3溶液检验阿司匹林中是否含有未反应完的水杨酸 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
 | ⅠA | ⅡA | ⅢA | ⅣA | ⅤA | ⅥA | ⅦA | 0 |
| 1 | A | |||||||
| 2 | D | E | F | G | I | |||
| 3 | B | C | H |
 .
. →
→ .
.查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 46g C2H6O中含有的C-H键数一定为5NA | |
| B. | 常温常压下,17g 甲基(-14CH3)所含电子总数为9NA | |
| C. | 制粗硅时12g C能还原含2NASi-O键的SiO2 | |
| D. | CO2气体与足量的Na2O2反应,固体增重28g时转移了NA个电子 |
查看答案和解析>>
科目:高中化学 来源: 题型:实验题
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 16a mol-1 | B. | $\frac{16}{a}$ | C. | ($\frac{16}{a}$) mol-1 | D. | 16 a |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 取KMnO4样品时不慎在表面沾了点蒸馏水 | |
| B. | 容量瓶洗涤后残留蒸馏水 | |
| C. | 定容时俯视容量瓶刻度线 | |
| D. | 摇匀后见液面下降,再加水至刻度线 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com