
| A. | 一定条件下,将1molN2和3molH2H混合,充分反应后转移电子数为6NA | |
| B. | 常温下,5.6gFe与足量浓硝酸作用转移电子数一定为0.3NA | |
| C. | 65gZn与一定量的浓硫酸反应至完全溶解,转移电子数一定为2NA | |
| D. | 6.4g由S2、S4、S8组成的混合物中含有硫原子的数目为0.1NA |
分析 A.氮气与氢气反应生成氨气为可逆反应,可逆反应不能进行到底;
B.常温下铁与浓硝酸发生钝化现象,阻止了反应的继续进行;
C.锌为+2价金属,65g锌的物质的量为1mol,完全反应失去2mol电子;
D.S2、S4、S8都是与S原子构成的,6.4g混合物中含有6.4gS原子,含有0.2mol硫原子.
解答 解:A.合成氨是可逆反应,1mol N2和3mol H2充分混合,反应生成的氨气小于2mol,转移的电子数小于6NA,故A错误;
B.常温下铁、铝与浓硫酸、浓硝酸发生钝化,阻止了反应的进行,故B错误;
C.65g锌的物质的量为1mol,1mol锌完全反应生成1mol锌离子,转移了2mol电子,转移电子数一定为2NA,故C正确;
D.6.4gS2、S4、S8的混合物中含有6.4gS原子,含有0.2mol硫原子,所含S原子数为0.2NA,故D错误;
故选C.
点评 本题考查阿伏加德罗常数的有关计算和判断,题目难度中等,注意明确可逆反应特点,掌握好以物质的量为中心的各化学量与阿伏加德罗常数的关系,注意质量守恒定律在化学计算中的应用方法.


 灵星计算小达人系列答案
灵星计算小达人系列答案 孟建平错题本系列答案
孟建平错题本系列答案科目:高中化学 来源: 题型:多选题
| 反应时间/s | 0 | 3 | 6 | 12 | 24 |
| n(CO2)/mol | 0 | 0.6 | 0.96 | 1.5 | 1.5 |
| A. | 反应在0~3s内的平均速率v(H2O)=0.12mol•L-1•s-1 | |
| B. | 24s后,若保持其他条件不变,降低温度,达到新平衡时测得c(CO2)=0.76mol•L-1,则反应的△H<0 | |
| C. | 在T温度下,若起始时向容器中充入4.0molH2O和2.0molCO2、2.0molH2,与原平衡相比,达到平衡时,容器内压强增大 | |
| D. | 在T温度下,起始时向容器中充入2.0molH2O、1.0molCO2和1.0molH2,达到平衡时,CO2的转化率等于25% |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
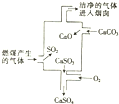
| A. | 使用此废气处理工艺不能减少SO2的排放 | |
| B. | 该过程发生的反应有化合、分解、置换和氧化还原反应 | |
| C. | 整个过程的反应可表示为2SO2+2CaCO3+O2═2CaSO4+2CO2 | |
| D. | 可用NaOH溶液检验废气处理是否达标 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
 A、B、C、D、E、F六种短周期元素的简单离子都含有10个电子,且对应元素化合价与原子序数的关系如图所示.
A、B、C、D、E、F六种短周期元素的简单离子都含有10个电子,且对应元素化合价与原子序数的关系如图所示.| ⅠA | ⅡA | ⅢA | ⅣA | ⅤA | ⅥA | ⅦA | 0 | |
| 一 | ----------------- | |||||||
| 二 | ||||||||
| 三 | ||||||||
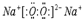 ,AB、两元素对应的气态氢化物的稳定性强弱关系是H2O>NH3(用化学式表示).
,AB、两元素对应的气态氢化物的稳定性强弱关系是H2O>NH3(用化学式表示).查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | ①②③⑤ | B. | ①③④ | C. | ①③⑤ | D. | ①②③④⑤ |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
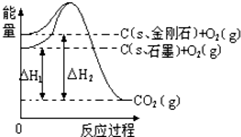
| A. | 石墨和金刚石的转化是物理变化 | |
| B. | 金刚石的稳定性强于石墨 | |
| C. | 1 mol石墨的总键能比1 mol金刚石的总键能大 1.9 kJ | |
| D. | C(s,石墨)=C(s,金刚石),该反应的焓变(△H)为负值 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | ②③④⑤ | B. | ①③④⑤ | C. | ①②③④ | D. | ①②④⑤ |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
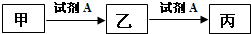
| A. | 若A为硝酸,X为金属元素,则甲与丙反应可生成乙 | |
| B. | 若乙为NaHCO3,则丙一定是CO2 | |
| C. | 若A为金属单质,乙的水溶液遇KSCN溶液变红,则甲可能为非金属单质 | |
| D. | 若A为NaOH溶液,X为短周期的金属元素,则乙一定为白色沉淀 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 加入适量稀盐酸 | B. | 加入适量稀硫酸 | ||
| C. | 加入适量烧碱固体 | D. | 加水稀释 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com