
【题目】(1)指出配合物K3[Co(CN)6]中的中心离子、配位体及其配位数:_____、_______、________。
(2)下列分子中若有手性原子,请用“*”标出其手性碳原子。____________
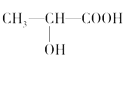
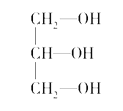
(3)在下列物质①CO2、②NH3、③CCl4、④BF3、⑤H2O、⑥SO2、⑦SO3、⑧、PCl3中,属于非极性分子的是(填序号)________________。
(4)试比较下列含氧酸的酸性强弱(填“>”、“<”或“=”):HClO3________HClO4;
(5)I3+属于多卤素阳离子,根据VSEPR模型推测I3+的立体构型为_______________。
【答案】 Co3+ CN- 6 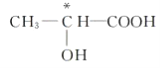 ①③④⑦ < V形
①③④⑦ < V形
【解析】(1)根据配合物的结构简式可知,在配合物K3[Co(CN)6]中的中心离子是Co3+,配位体是CN-,配位数是6;(2)如果饱和碳原子连接的4个原子或基团各不相同,则该碳原子就是手性碳原子,所以含有手性碳原子的是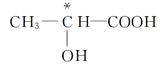 ;
;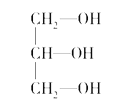 不含有手性碳原子;(3)①CO2中C元素化合价为+4,C原子最外层4个电子全部成键,为非极性分子;②NH3中C元素化合价为-3,N原子最外层5个电子未全部成键,为极性分子;③CCl4中C元素化合价为+4,C原子最外层4个电子全部成键,为非极性分子;④BF3中B元素化合价为+3,B原子最外层3个电子全部成键,为非极性分子;⑤H2O中O元素化合价为-2,O原子最外层6个电子未全部成键,为极性分子;⑥SO2中S元素化合价为+4,S原子最外层6个电子未全部成键,为极性分子;⑦SO3中S元素化合价为+6,S原子最外层6个电子全部成键,为非极性分子;⑧PCl3中P元素化合价为+3,P原子最外层5个电子未全部成键,为极性分子;答案选①③④⑦;(4)含氧酸分子的结构中含非羟基(羟基为-OH)氧原子数越多,该含氧酸的酸性越强,所以含氧酸的通式可写成(HO)mROn,如果成酸元素R相同,则n值越大,酸性越强,则酸性:HClO3<HClO4;(5)因为I3+可看成II2+,所以根据价层电子对互斥理论可知,I3+中中心原子含有的孤对电子对数=
不含有手性碳原子;(3)①CO2中C元素化合价为+4,C原子最外层4个电子全部成键,为非极性分子;②NH3中C元素化合价为-3,N原子最外层5个电子未全部成键,为极性分子;③CCl4中C元素化合价为+4,C原子最外层4个电子全部成键,为非极性分子;④BF3中B元素化合价为+3,B原子最外层3个电子全部成键,为非极性分子;⑤H2O中O元素化合价为-2,O原子最外层6个电子未全部成键,为极性分子;⑥SO2中S元素化合价为+4,S原子最外层6个电子未全部成键,为极性分子;⑦SO3中S元素化合价为+6,S原子最外层6个电子全部成键,为非极性分子;⑧PCl3中P元素化合价为+3,P原子最外层5个电子未全部成键,为极性分子;答案选①③④⑦;(4)含氧酸分子的结构中含非羟基(羟基为-OH)氧原子数越多,该含氧酸的酸性越强,所以含氧酸的通式可写成(HO)mROn,如果成酸元素R相同,则n值越大,酸性越强,则酸性:HClO3<HClO4;(5)因为I3+可看成II2+,所以根据价层电子对互斥理论可知,I3+中中心原子含有的孤对电子对数=![]() =2,所以其空间构型为V形。
=2,所以其空间构型为V形。


 开心快乐假期作业暑假作业西安出版社系列答案
开心快乐假期作业暑假作业西安出版社系列答案 名题训练系列答案
名题训练系列答案科目:高中化学 来源: 题型:
【题目】有关煤、石油和天然气的综合利用,下列说法正确的是
A.水煤气主要成分是CH4
B.煤的气化和液化、石油的分馏都是物理变化
C.裂解的目的是提高汽油的产量和质量
D.鉴别直馏汽油和裂化汽油,可用溴水鉴别
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】有六种短周期元素,已知A的单质是最清洁的能源物质,其他元素的原子半径及主要化合价如下表:
元素代号 | B | C | D | E | F |
原子半径/nm | 0.186 | 0.143 | 0.102 | 0.099 | 0.074 |
主要化合价 | +1 | +3 | +6、-2 | +7、-1 | -2 |
根据上述信息回答以下问题。
(1)D在元素周期表中的位置______________;E的离子结构示意图______________。
(2)关于A元素在周期表中的位置,一直存在纷争,有人主张把它放在第ⅦA族,试分析其理由________________________________。
(3)用电子式表示B的单质与D的单质形成化合物的过程________________________。
(4)下列各项比较,正确的是________________________。
①氢化物的沸点:D低于F ②A~F元素的简单离子半径:C的最大
③气态氢化物稳定性:D比E稳定 ④最高价氧化物对应的水化物碱性:B小于C
(5)E单质常用于自来水消毒。用必要的文字和离子方程式解释原因______________________________________________________________。
(6)写出C的单质与B的最高价氧化物的水化物反应的离子方程式________________。
(7)C的单质与元素M的红棕色氧化物N反应可用于焊接钢轨,该反应的化学方程式为________________________________。
(8)已知单质M的燃烧热为375kJ/mol,写出表示其燃烧热的热化学方程式___________________________。
(9)已知NH3结合质子的能力强于F的氢化物,请用最恰当的离子方程式证明这个结论________________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】I.某学习小组做Na2O2与H2O反应的实验,发现一些有趣的现象:
①取适量Na2O2固体用脱脂棉包好放在石棉网上,然后向脱脂棉上滴加3-4滴水,结果脱脂棉剧烈燃烧。
②取适量Na2O2固体置于试管中,加水使其充分反应至不再产生气体为止,滴入几滴酚酞试液,溶液先变红后褪色。回答有关问题。
(1)写出Na2O2的电子式_______________________。
(2)已知Na2O2可看作二元弱酸H2O2对应的盐,其第一步水解完全进行。写出其第一步水解的离子方程式为___________________________________。
(3)由①实验现象所得出的有关结论是:a.有氧气生成;b.___________________。
(4)Na2O2与H2O反应的离子方程式____________________________________。
II.为探究Na2O2与H2O反应的机理,他们在老师的指导下设计了下图所示装置。连接好装置,打开K1、K2,通过注射器注入适量蒸馏水,充分反应后用气球鼓气,Na2S溶液变浑浊,酸性KMnO4溶液褪色。分别取A、C中溶液滴入几滴酚酞,开始都变红,以后A中溶液很快褪色,C中溶液缓慢褪色。另取A、C中溶液分别加入少量二氧化锰,充分振荡,发现均反应剧烈、产生大量气泡,把带火星的木条伸入试管,木条复燃,向反应后的溶液中滴入几滴酚酞试液,溶液变红不褪色。
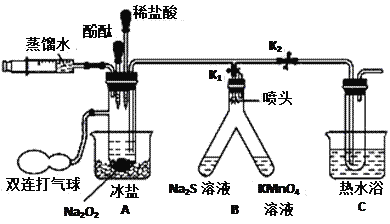
(5)A中冰盐和C中热水的作用分别是__________________,___________________。
(6)用化学方程式表示Na2S变浑浊的原因___________________________________。
(7)用离子方程式表示KMnO4溶液褪色的原因(MnO4-在酸性条件下被还原成Mn2+)__________________________________________。
(8)Na2O2与H2O反应的机理是(用化学方程式表示)第一步_____________________,第二步_______________________________。
(9)若向Na2O2中滴加适量的稀盐酸,也能产生同样的气体,请写出该反应的化学方程式___________________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列有关金属晶体的说法中,正确的是( )
A. 简单立方堆积的晶胞中原子配位数是8
B. 晶胞中配位数为12的金属,一定是面心立方最密堆积
C. Zn的晶胞类型与铜相同
D. 铁的晶胞中空间利用率为68%
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】合成气的主要成分是 一氧化碳和氢气,是重要的化工原料。
I.已知下列反应:
①CH4(g) + H2O(g)![]() CO(g) + 3H2(g) ΔH = +206 kJ/mol
CO(g) + 3H2(g) ΔH = +206 kJ/mol
②C(s) + H2O(g) = CO(g) + H2(g) ΔH = +131 kJ/mol
(1)工业制取炭黑的方法之一是将甲烷隔绝空气加热到1300℃进行裂解。填写空白。
CH4(g)= C(s)+ 2H2(g) ΔH =______________kJ/mol。
(2)若800℃时,反应①的平衡常数K1=1.0,某时刻测得该温度下,密闭容器中各物质的物质的量浓度分别为:c(CH4)=4.0 mol·L-1;c(H2O)=5.0 mol·L-1;c(CO)=1.5 mol·L-1;c(H2)=2 mol·L-1,则此时该可逆反应的状态是_____________________(填“达到平衡”、“向正反应方向移动”或“向逆反应方向移动”)。
Ⅱ.甲醇是一种可再生能源,工业上用合成气来合成甲醇:CO(g)+2H2(g)![]() CH3OH(g),分析该反应并回答下列问题:
CH3OH(g),分析该反应并回答下列问题:
(3)一定条件下,将CO与H2以物质的量之比1:1置于恒容密闭容器中发生以上反应,能说明该反应已达到平衡的是_____________________________。
A.体系的压强不发生变化 B.混合气的密度保持不变
C.体系中碳元素的质量分数不变 D.CO与H2的物质的量之比保持不变
(4)如图是该反应在不同温度下CO的转化率随时间变化的曲线。T1和T2温度下的平衡常数大小关系是K1______K2 (填“>”、“<”或“=”)。理由是__________________________________________________。
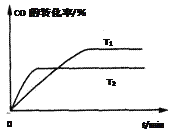
(5)已知甲醇燃料电池的工作原理如图所示。该电池工作时,电池左边的电极发生的电极反应式为______________________________。
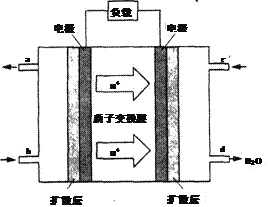
(6)用甲醇燃料电池作为直流电源,设计如图装置制取Cu2O,电解总反应为:2Cu+H2O=Cu2O+H2↑。写出铜电极的电极反应式_______________________。

查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】(一) A、B、C、D为中学常见物质且均含有同一种元素,相互转化关系如图(反应条件及其他物质已经略去):
![]()
(1)若A、B、C、D均为化合物,而且它们的水溶液均能使湿润的蓝色石蕊试纸变红,则D的化学式为________,写出B→C的化学反应方程式:____________。
(2)若A的水溶液能使湿润的红色石蕊试纸变蓝,D的稀溶液能使湿润的蓝色石蕊试纸变红。则D的化学式为__________________。写出A→B的化学反应方程式:_______。
(3)若A为单质,组成元素的原子所含质子的数目小于18,D为强碱,则B的化学式:________________。
(二)(1)肼(N2H4)和NO2是一种双组分火箭推进剂。两种物质混合发生反应生成N2和H2O(g),已知8g气体肼在上述反应中放出142kJ热量,其热化学方程式为______________ 。
(2)0.3mol的气态高能燃料乙硼烷(B2H6)在氧气中燃烧,生成固态三氧化二硼和液态水,放出649.5kJ热量,其热化学反应方程式为__________________;
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】电炉加热时用纯O2氧化管内样品,根据产物的质量确定有机物的组成.下列装置是用燃烧法确定有机物分子式常用的装置.
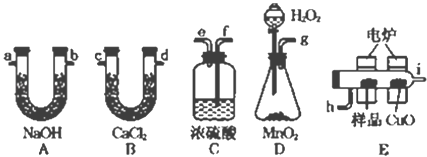
(1)产生的O2按从左到右的流向,所选装置各导管的正确连接顺序是g→ → →h→i→ → → → ._______________
(2)燃烧管中CuO的作用是______.
(3)若实验中所取样品只含C、H、O三种元素中的两种或三种,准确称取3.24g样品,经充分反应后,A管质量增加9.24g,B管质量增加2.16g,则该样品的实验式为______.
(4)要确定该物质的分子式,还要知道该物质的______.经测定其蒸气密度为4.82g/L(已换算为标准状况下),则其分子式为______.
(5)经红外光谱分析知该化合物的分子中存在1个苯环,苯环上只有1个支链,且支链中有1个甲基.试写出该有机物的结构简式______.
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com