
 ,故错。故选AD。
,故错。故选AD。

科目:高中化学 来源:不详 题型:单选题
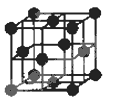
| A.金刚石的正四面体网状结构中最小的环上有6个碳原子 |
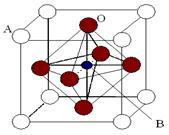
| B.如图在面心立方密堆积的金属晶体中,每个金属原子周围紧邻的有12个金属原子 |
| C.在氯化钠晶体中,每个氯离子周围都紧邻8个钠离子 |
| D.分子晶体干冰也是面心立方晶胞,每个晶胞平均含有4个CO2分子 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
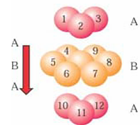
| A.①②③④⑤⑥ | B.③②①⑤④⑥ | C.③②①④⑤⑥ | D.⑥⑤④③②① |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| A.石英和生石灰的熔化 | B.冰的熔化和氯化钠的熔化 |
| C.晶体硅和晶体硫的熔化 | D.钠和铁的熔化 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| A.熔点从高到低的顺序是:金刚石>碳化硅>晶体硅 |
| B.熔点从高到低的顺序是:金刚石>晶体硅>碳化硅 |
| C.三种晶体中的结构单元都是三角锥结构 |
| D.三种晶体都是原子晶体且均为电的良导体 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:填空题
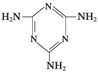 俗称“蛋白精”。动物摄入三聚氰胺和三聚氰酸
俗称“蛋白精”。动物摄入三聚氰胺和三聚氰酸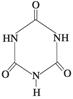 后,
后,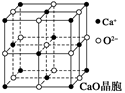
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| A.晶格能是气态离子形成1摩离子晶体释放的能量 |
| B.晶格能通常取正值,但是有时也取负值 |
| C.晶格能越大,形成的离子晶体越不稳定 |
| D.晶格能越大,物质的硬度反而越小 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| A.在NaCl晶体中,距Na+最近的Cl-形成正八面体 |
| B.在NaCl晶体中,每个晶胞平均占有4个Na+ |
| C.在CsCl晶体中,每个晶胞平均占有8个Cs+ |
| D.铜晶体为面心立方堆积,铜原子的配位数(距离一个铜原子最近的其它铜原子的个数)为12 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com