
| A. | ①② | B. | ②③ | C. | ③④ | D. | ①④ |
分析 ①氯气和水反应生成HCl、HClO,这两种酸都能和NaOH溶液发生中和反应;
②除杂时要除去杂质且不能引进新的杂质;
③碘和浓盐酸不反应,易溶于有机溶剂,且能和热的强碱溶液反应;
④制Cl2后的黑褐色污迹是二氧化锰,二氧化锰和浓盐酸在加热条件下能反应生成可溶性的氯化锰.
解答 解:①氯气和水反应生成HCl、HClO,这两种酸都能和NaOH溶液发生中和反应,所以可用倒扣在NaOH溶液上面的漏斗装置吸收残余的Cl2,故正确;
②除杂时要除去杂质且不能引进新的杂质,加入HCl,虽然能除去碳酸氢钾,但引进新的杂质KCl,应该用HI溶液,故错误;
③碘和浓盐酸不反应,易溶于有机溶剂,且能和热的强碱溶液反应,可以用乙醇或热的NaOH溶液除去碘,故错误;
④制Cl2后的黑褐色污迹是二氧化锰,二氧化锰和浓盐酸在加热条件下能反应生成可溶性的氯化锰,所以制Cl2后的黑褐色污迹可用热的浓盐酸洗去,故正确;
故选D.
点评 本题考查化学实验方案评价,为高频考点,涉及除杂、尾气处理等知识点,明确实验原理、物质性质是解本题关键,注意:除杂时不能引进新的杂质且操作简单易行,题目难度不大.


科目:高中化学 来源: 题型:选择题
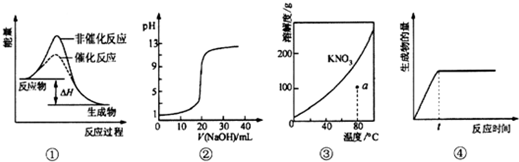
| A. | ①表示某吸热反应分别在有、无催化剂的情况下反应过程中的能量变化 | |
| B. | ②表示0.1 mo1•L-1NaOH溶液滴定20 mL 0.1 mo1•L-1HCl溶液所得到的滴定曲线 | |
| C. | ③表示KNO3的溶解度曲线,图中a点所示的溶液是80℃时KNO3的不饱和溶液 | |
| D. | 某可逆反应生成物的量随反应时间关系如图④所示,在t时反应物转化率达到最大 |
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
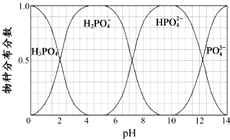 磷的重要化合物NaH2PO4、Na2HPO4和Na3PO4可通过H3PO4与NaOH溶液反应获得,含磷各物种的分布分数(平衡时某物种的浓度占各物种浓度之和的分数)与pH 的关系如图所示.
磷的重要化合物NaH2PO4、Na2HPO4和Na3PO4可通过H3PO4与NaOH溶液反应获得,含磷各物种的分布分数(平衡时某物种的浓度占各物种浓度之和的分数)与pH 的关系如图所示.查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | ①③④⑥ | B. | ②⑤ | C. | ①③⑤⑥ | D. | ①②③④⑤ |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 95℃纯水的pH<7,说明加热可导致水呈酸性 | |
| B. | 用pH试纸测溶液的pH时,需先用蒸馏水润湿试纸 | |
| C. | 0.2 mol/L的盐酸与等体积水混合后pH约为1 | |
| D. | 25℃时,pH=12的氨水溶液与pH=2的盐酸等体积混合后pH=7 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
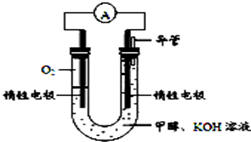 “低碳循环”引起各国的高度重视,而如何降低大气中CO2的含量及有效地开发利用CO2,引起了全世界的普遍重视.所以“低碳经济”正成为科学家研究的主要课题
“低碳循环”引起各国的高度重视,而如何降低大气中CO2的含量及有效地开发利用CO2,引起了全世界的普遍重视.所以“低碳经济”正成为科学家研究的主要课题| 实验组 | 温度℃ | 起始量/mol | 平衡量/mol | 达到平衡所需时间/min | ||
| CO | H2O | H2 | CO | |||
| 1 | 650 | 4 | 2 | 1.6 | 2.4 | 6 |
| 2 | 900 | 2 | 1 | 0.4 | 1.6 | 3 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 原子半径依次增大 | B. | 单质的熔沸点逐渐升高 | ||
| C. | 卤离子的还原性逐渐减弱 | D. | 氢化物的热稳定性依次减弱 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com