


 名校课堂系列答案
名校课堂系列答案科目:高中化学 来源: 题型:

| 气体 | 氮气 | 氢气 | 氨 |
| 熔点(℃) | -210.01 | -252.77 | -77.74 |
| 沸点(℃) | -195.79 | -259.23 | -33.42 |
| [NH3]2 |
| [N2][H2]3 |
| [NH3]2 |
| [N2][H2]3 |
查看答案和解析>>
科目:高中化学 来源: 题型:
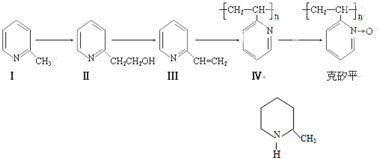
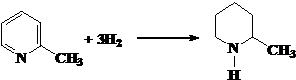
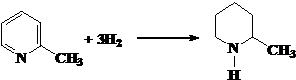
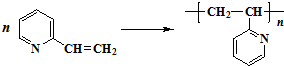
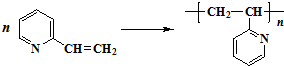
查看答案和解析>>
科目:高中化学 来源: 题型:
工业上合成氨是在一定条件下进行如下反应:
N2(g)+3H2(g)![]() 2NH3(g),△H=-92.2kJ/mol;其部分工艺流程如下:
2NH3(g),△H=-92.2kJ/mol;其部分工艺流程如下:

反应体系中各组分的部分性质见下表:
| 气体 | 氮气 | 氢气 | 氨 |
| 熔点(℃) | -210.01 | -252.77 | -77.74 |
| 沸点(℃) | -195.79 | -259.23 | -33.42 |
回答下列问题:
(1)写出该反应的化学平衡常数表达式:K= 。随着温度升高,
K值 (填增大、减小、不变)。
(2)平衡常数K值越大,表明 (填序号)。
A.N2的转化率越高 B.NH3的产率越大
C.原料中N2的含量越高 D.化学反应速率越快
(3)合成氨反应的平衡常数很小,所以在工业上采取气体循环的流程。即反应后通过把混合气体的温度降低到 使 分离出来;继续循环的气体是 。
查看答案和解析>>
科目:高中化学 来源: 题型:
工业上合成氨是在一定条件下进行如下反应:
N2(g)+3H2(g)2NH3(g),△H=-92.2kJ/mol;其部分工艺流程如下:
反应体系中各组分的部分性质见下表:
| 气体 | 氮气 | 氢气 | 氨 |
| 熔点(℃) | -210.01 | -252.77 | -77.74 |
| 沸点(℃) | -195.79 | -259.23 | -33.42 |
回答下列问题:
(1)写出该反应的化学平衡常数表达式:K= 。随着温度升高,
K值 (填增大、减小、不变)。
(2)平衡常数K值越大,表明 (填序号)。
A.N2的转化率越高 B.NH3的产率越大
C.原料中N2的含量越高 D.化学反应速率越快
(3)合成氨反应的平衡常数很小,所以在工业上采取气体循环的流程。即反应后通过把混合气体的温度降低到 使 分离出来;继续循环的气体是 。
查看答案和解析>>
科目:高中化学 来源:2014届湖北省高二秋季期中联考化学试卷(解析版) 题型:填空题
(14分)工业上利用CO和水蒸气在一定条件下发生反应制取氢气:
CO(g)+H2O(g)  CO2(g)+H2(g)
CO2(g)+H2(g)
某研究小组分别在体积均为2 L的恒容密闭容器中加入一定量的反应物,使其发生反应,相关数据如下:
|
容器 编号 |
温度 /℃ |
起始量/mol |
平衡量/mol |
达到平衡的时间/min |
达平衡时体系能量的变化/kJ |
||
|
CO |
H2O |
CO2 |
H2 |
||||
|
① |
650 |
1 |
2 |
0.4 |
0.4 |
5 |
16.4kJ |
|
② |
650 |
2 |
4 |
|
|
t1 |
Q1 kJ |
|
③ |
900 |
2 |
4 |
1.6 |
1.6 |
t2 |
Q2 kJ |
(1)计算容器②中反应的平衡常数K= (计算结果保留两位小数)。
(2)容器③中反应达平衡时,CO的转化率为 。
(3)容器①中反应达平衡这段时间,化学反应速率v (H2) = 。
(4)该反应的正反应为 (填“吸热”或“放热”)反应,理由是 。
(5)下列叙述正确的是 (填字母序号)。
a.平衡时,容器①和容器②中CO2的体积分数相等
b.反应达平衡状态时,Q2 > Q1 > 32.8 kJ
c.达到平衡的时间:t2 > t1>2.5 min
d.该反应的热化学方程式可表示为:CO(g)+H2O(g)  CO2(g)+H2(g) △H=-41 kJ/mol
CO2(g)+H2(g) △H=-41 kJ/mol
(6)容器②中反应进行到t min时,测得混合气体中CO2的物质的量为0.6 mol。若用200 mL 5 mol/L的NaOH溶液将其完全吸收,得到的溶液中所有离子的物质的量浓度由大到小的顺序为 。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com