
分析 (1)反应中Cu元素的化合价升高,N元素的化合价降低;
(2)根据铜和二氧化氮之间的关系式计算;
(3)根据转移电子守恒计算被还原的硝酸.
解答 解:(1)反应中Cu元素的化合价升高,被氧化,铜为还原剂,N元素的化合价降低,被还原,硝酸为氧化剂,答:氧化剂为硝酸,还原剂为铜
(2)铜和二氧化氮的关系式为:Cu----2NO2,铜的物质的量=$\frac{6.4}{64}mol=0.1mol$,根据关系式知,0.1mol铜与硝酸反应可以得到0.2mol二氧化氮,二氧化氮在标况下的体积=0.2mol×22.4L/mol=4.48L,
答:二氧化氮的体积是4.48L;
(3)6.4g铜全部被氧化,提供电子的物质的量=$\frac{6.4}{64}mol×2=0.2mol$,而硝酸中+5价的N被还原成二氧化氮中+4价的N,需要得到1mol电子,所以要得到0.2mol得电子,只能还原0.2mol硝酸,
答:有0.2mol硝酸被还原.
点评 本题考查氧化还原反应,为高考常见题型,侧重氧化还原反应中基本概念的考查,明确含元素化合价降低的物质为氧化剂、还原剂被氧化等即可解答,题目较简单.


 学期复习一本通学习总动员期末加暑假延边人民出版社系列答案
学期复习一本通学习总动员期末加暑假延边人民出版社系列答案 芒果教辅暑假天地重庆出版社系列答案
芒果教辅暑假天地重庆出版社系列答案科目:高中化学 来源: 题型:填空题
查看答案和解析>>
科目:高中化学 来源: 题型:多选题
| A. | 油脂在人体内的水解、氧化可释放能量,所以油脂可在人体内提供能量 | |
| B. | 为人体合成其他化合物提供原料 | |
| C. | 保持体温,保护内脏器官 | |
| D. | 促进脂溶性维生素A、D、E、K等物质的吸收 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | v(B2)=0.8 mol•L-1•s-1 | B. | v(A2)=0.4 mol•L-1•s-1 | ||
| C. | v(C)=0.6 mol•L-1•s-1 | D. | v(B2)=4.2 mol•L-1•min-1 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | a>b>c>d | B. | c>a>b>d | C. | a>c>d>b | D. | b>d>c>a |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
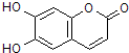
| A. | M的相对分子质量是180 | |
| B. | M与足量的NaOH溶液发生反应时,所得的有机产物的化学式C9H4O5Na4 | |
| C. | 1molM最多能与2molBr2发生反应 | |
| D. | 1molM与足量NaHCO3反应能生成2molCO2 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com