
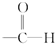
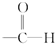 中C、O共用2对电子,C、H共用1对电子,有一个为成键的电子;
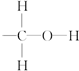
中C、O共用2对电子,C、H共用1对电子,有一个为成键的电子; 中,C与2个氢原子、1个氧原子分别共用1对电子,O与H之间共用1对电子,C有1个未成对电子;
中,C与2个氢原子、1个氧原子分别共用1对电子,O与H之间共用1对电子,C有1个未成对电子;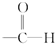 中C、O共用2对电子,C、H共用1对电子,电子式为
中C、O共用2对电子,C、H共用1对电子,电子式为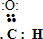 ;
;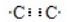 ;
; 中,C与2个氢原子、1个氧原子分别共用1对电子,O与H之间共用1对电子,C有1个未成对电子,电子式为
中,C与2个氢原子、1个氧原子分别共用1对电子,O与H之间共用1对电子,C有1个未成对电子,电子式为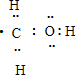 ;
;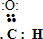 ;
;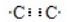 ;
;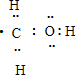 ;
;

科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
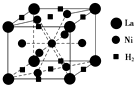 目前,利用金属或合金储氢的研究已取得很大进展,如图是一种镍基合金储氢后的晶胞结构图.
目前,利用金属或合金储氢的研究已取得很大进展,如图是一种镍基合金储氢后的晶胞结构图.查看答案和解析>>
科目:高中化学 来源: 题型:
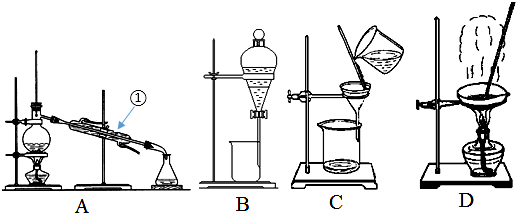
查看答案和解析>>
科目:高中化学 来源: 题型:
| 温度/℃ | 400 | 500 | 800 |
| 平衡常数K | 9.94 | 9 | 1 |
查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、KMnO4酸性溶液既可鉴别乙烷与乙烯,又可除去乙烷中的乙烯而得到纯净的乙烷 |
| B、在混有乙酸的乙酸乙酯中加入NaOH溶液可以达到除杂的目的 |
| C、丙烯的结构简式可以表示为CH3CHCH2 |
| D、CH2Cl2是纯净物说明甲烷是四面体结构而不是正方形 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com