

 ��������ϵ�д�
��������ϵ�д�
| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�

| ||
| ||

t��min�� Ũ�ȣ�mol/L�� |
0 | 1 | 2 | 3 | 4 | 5 | 6 |
| c��C�� | 0.054 | 0.034 | 0.018 | 0.012 | 0.008 | 0.006 | 0.006 |
| c��O2�� | 0.032 | 0.022 | 0.014 | 0.011 | 0.009 | 0.008 | 0.008 |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�

�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
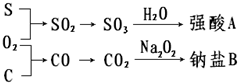 �������ʼ�����ͼ��ʾת����ϵ���ش��������⣺
�������ʼ�����ͼ��ʾת����ϵ���ش��������⣺�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ����׳��Ƥ�顤����ͬ��ϵ�С������ɽ��������߶���ѧ���ϣ� ���ͣ�022
��ɫ��������A����ͼ��ʾת����ϵ��ÿ�������ʾ��һ�ַ�Ӧ���������(��Ӧ���������ɵ�ˮ����ȥ)������C��F������Ϊ��ɫ���壬D��E�й�ͬ�������ӣ�
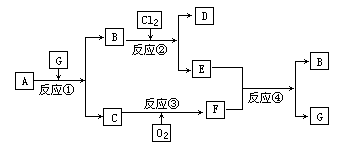
(1)д��B��C�Ļ�ѧʽ��B________��
����������������������C________��
(2)д����Ӧ�ܵ����ӷ���ʽ________��
(3)д����Ӧ�۵Ļ�ѧ����ʽ������������ת�Ƶ����________��
�鿴�𰸺ͽ���>>
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com