
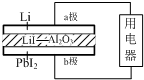
 某锂碘电池以LiI-Al2O3固体为电解质传递离子,其基本结构示意图如下,电池总反应可表示为:2Li+PbI2=2LiI+Pb.下列说法正确的是( )
某锂碘电池以LiI-Al2O3固体为电解质传递离子,其基本结构示意图如下,电池总反应可表示为:2Li+PbI2=2LiI+Pb.下列说法正确的是( )| A. | 电子由b极经用电器流向a极 | |
| B. | I-由a极通过固体电解质传递到b极 | |
| C. | b极上的电极反应式为:PbI2-2e-=Pb+2I- | |
| D. | b极质量减少1.27 g 时,a极转移的电子数约为6.02×1021 |
分析 根据电池总反应:2Li+PbI2=2LiI+Pb可知:通入锂的一极为电池的负极,发生氧化反应,通入PbI2的一极为电池的正极,发生还原反应,PbI2+2e-=Pb+2I-电池工作时,电子通过外电路从负极流向正极,即从a极流向b极,电解质溶液中阴离子向负极移动,即由b极通过固体酸电解质传递到a极;根据反应PbI2+2e-=Pb+2I-,b极质量减少1.27g时,转移0.01mol电子.
解答 解:A、通入锂的一极为电池的负极,通入PbI2的一极为电池的正极,这样电子应该是通过外电路由a极流向b,故A错误;
B、电解质溶液中阴离子向负极移动,即由b极通过固体酸电解质传递到a极,故B错误;
C、通入PbI2的一极为电池的正极,发生还原反应,PbI2+2e-=Pb+2I-,故C错误;
D、根据反应PbI2+2e-=Pb+2I-,b极质量减少1.27g时,转移0.01mol电子,a极转移的电子数约为6.02×1021,故D正确.
故选D.
点评 本题考查原电池的工作原理,学习中要明确电子以及离子的定向移动问题,要能正确判断原电池的正负极,以及电极反应式的书写问题,题目难度不大.


 优百分课时互动系列答案
优百分课时互动系列答案科目:高中化学 来源: 题型:选择题
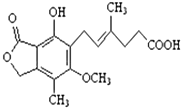 麦考酚酸是一种有效的免疫抑制剂,能有效地防止肾移植排斥,其结构简式如图所示.下列有关麦考酚酸说法不正确的是( )
麦考酚酸是一种有效的免疫抑制剂,能有效地防止肾移植排斥,其结构简式如图所示.下列有关麦考酚酸说法不正确的是( )| A. | 分子式为C17H22O6 | |
| B. | 能与FeCl3溶液发生显色反应 | |
| C. | 1mol麦考酚酸最多能与3mol NaOH反应 | |
| D. | 1mol麦考酚酸最多能与4mol H2发生加成反应 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 在FeO•FeyCrxO3中3x=y | |
| B. | 消耗硫酸亚铁铵的物质量为n(2-x)mol | |
| C. | 反应中发生转移的电子数为3nx mol | |
| D. | 处理废水中Cr2O72- 的物质量为$\frac{nx}{2}$mol |
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
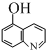 )是白色或淡黄色粉末,可通过如下实验步骤制得:
)是白色或淡黄色粉末,可通过如下实验步骤制得: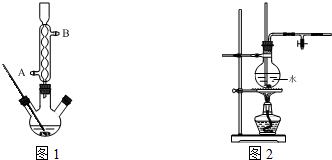
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
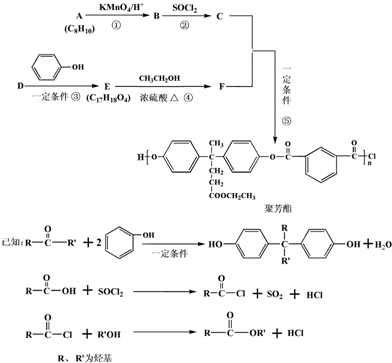
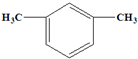 .
. .
.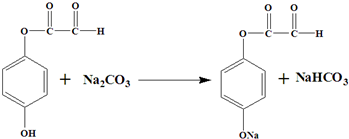 或
或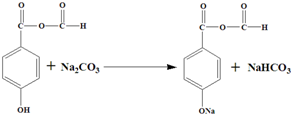 .
.查看答案和解析>>
科目:高中化学 来源: 题型:填空题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
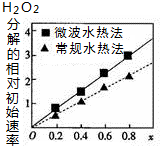 已知CoxNi(1-x)Fe2O4(其中Co、Ni均为+2价)可用作H2O2分解的催化剂,具有较高的活性,通常由两种不同方法制得.如图为二种方法制得的催化剂,在10℃时催化分解6%的H2O2溶液的相对初始速率随x变化的曲线图.下列说法错误的是( )
已知CoxNi(1-x)Fe2O4(其中Co、Ni均为+2价)可用作H2O2分解的催化剂,具有较高的活性,通常由两种不同方法制得.如图为二种方法制得的催化剂,在10℃时催化分解6%的H2O2溶液的相对初始速率随x变化的曲线图.下列说法错误的是( )| A. | 该催化剂中铁元素的化合价为+3价 | |
| B. | Co、Ni、Fe均为ⅧB族元素 | |
| C. | 由图中信息可知,Co2+、Ni2+两种离子中催化效果较好的是Co2+ | |
| D. | 由图中信息可知,微波水热法制取的催化剂活性更高 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com