
.如图中A、B、H都属于盐类,A和B的水溶液都能使酚酞变红,H是人们日常生活中最常用的食品添加剂之一,E是淡黄色固体
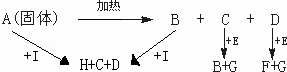
(1)写出下列物质的化学式FNaOH,IHCl
(2)写出下列反应的化学方程式:A→B+C+D
;C+E→B+G2;D+E→F+G
(3)写出下列反应的离子方程式:A+I→H+C+D;B+I→H+C+D.
| 无机物的推断. | |
| 专题: | 推断题. |
| 分析: | A、B、H都属于盐类,H是人们日常生活中最常用的食品添加剂之一,则H为NaCl,A和B的水溶液都能使酚酞变红,A分解得到B、C、D,考虑A为NaHCO3,B为Na2CO3,C、D分别为H2O、CO2中的一种,二者都能与淡黄色固体E反应生成G,则E为Na2O2,G为O2,由转化关系,可推知F为NaOH,D为H2O,C为CO2,I为 HCl,据此解答. |
| 解答: | 解:A、B、H都属于盐类,H是人们日常生活中最常用的食品添加剂之一,则H为NaCl,A和B的水溶液都能使酚酞变红,A分解得到B、C、D,考虑A为NaHCO3,B为Na2CO3,C、D分别为H2O、CO2中的一种,二者都能与淡黄色固体E反应生成G,则E为Na2O2,G为O2,由转化关系,可推知F为NaOH,D为H2O,C为CO2,I为 HCl, (1)由上述分析可知,F为NaOH,I为HCl,故答案为:NaOH;HCl; (2)A→B+C+D 的化学方程式:2NaHCO3 C+E→B+G的化学方程式:2Na2O2+2CO2=2Na2CO3+O2; D+E→F+G的化学方程式:2Na2O2+2H2O=4NaOH+O2↑, 故答案为:2NaHCO3 (3)A+I→H+C+D 的离子方程式:HCO3﹣+H+=CO2↑+H2O;B+I→H+C+D的离子方程式:CO32﹣+2H+=CO2↑+H2O, 故答案为:HCO3﹣+H+=CO2↑+H2O;CO32﹣+2H+=CO2↑+H2O. |
| 点评: | 本题考查无机物的推断,涉及钠元素化合物的转化,需要学生熟练掌握元素化合物知识,侧重对化学用语的考查,题目难度不大 |


 阅读快车系列答案
阅读快车系列答案科目:高中化学 来源: 题型:
用实验确定某酸HA是弱电解质。两同学的方案是:
甲:①称取一定质量的HA配制0.1 mol·L-1的溶液100 mL;
②用pH试纸测出该溶液的pH,即可证明HA是弱电解质。
乙:①用已知物质的量浓度的HA溶液、盐酸,分别配制pH=1的两种酸溶液各100 mL;
②分别取这两种溶液各10 mL,加水稀释为100 mL;
③各取相同体积的两种稀释液装入两个试管,同时加入纯度相同的锌粒,观察现象,即可证明HA是弱电解质。
(1)在两个方案的第①步中,都要用到的定量仪器是________________。
(2)甲方案中,说明HA是弱电解质的理由是测得溶液的pH______1(填“>”、“<”或“=”)。
乙方案中,说明HA是弱电解质的现象是____________(多选扣分)。
①装HCl溶液的试管中放出H2的速率快;
②装HA溶液的试管中放出H2的速率快;
③两个试管中产生气体的速率一样快。
(3)请你评价:乙方案中难以实现之处和不妥之处:
________________________________________________________________________、
________________________________________________________________________。
(4)请你再提出一个合理而比较容易进行的方案(药品可任取),作简明扼要表述:________________________________________________________________________
________________________________________________________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
对于合成氨反应,达到平衡后,以下分析正确的是( )
A.升高温度,对正反应的反应速率影响更大
B.增大压强,对正反应的反应速率影响更大
C.减小反应物浓度,对逆反应的反应速率影响更大
D.加入催化剂,对逆反应的反应速率影响更大
查看答案和解析>>
科目:高中化学 来源: 题型:
下列关于碱金属的叙述中 ,正确的是
,正确的是 ()
()
| A. | 碱金属都可以保存在煤油中 | |
| B. | 碱金属与水 | |
| C. | 碱金属在空气中加热均可生成多种氧化物 | |
| D. | 碱金属的硬度小、密度小、熔点低 |
查看答案和解析>>
科目:高中化学 来源: 题型:
分析图中的能量变化情况,下列正确的是( )
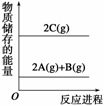
A.2A+B===2C ΔH<0 B.2C===2A+B ΔH<0
C.2A(g)+B(g)===2C(g) ΔH<0 D.2A(g)+B(g)===2C(g) ΔH>0
查看答案和解析>>
科目:高中化学 来源: 题型:
已知:
(1)H2(g)+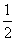 O2(g)===H2O(g) ΔH1=a kJ·mol-1
O2(g)===H2O(g) ΔH1=a kJ·mol-1
(2)2H2(g)+O2(g)===2H2O(g) ΔH2=b kJ·mol-1
(3)H2(g)+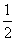 O2(g)===H2O(l) ΔH3=c kJ·mol-1
O2(g)===H2O(l) ΔH3=c kJ·mol-1
(4)2H2(g)+O2(g)===2H2O(l) ΔH4=d kJ·mol-1
下列关系式中正确的是( )
A.a<c<0 B.b>d>0 C.2a=b<0 D.2c=d>0
查看答案和解析>>
科目:高中化学 来源: 题型:
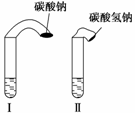
(1) 高中教材中有这样一个实验:在两支试管中分别加入3 mL稀盐酸(均足量)(只有浓度
小于1 mol·L-1的稀盐酸跟Na2CO3和NaHCO3反应才能根据反应的剧烈程度区分开来,浓度较高则反应现象都是同样的剧烈),将两个各装有0.3 g NaHCO3和Na2CO3粉末的小气球分别套在两支试管口上。将气球内的NaHCO3或Na2CO3同时倒入试管中,观察到现象如下:
①试管中(填产生沉淀或气体及反应速率等相关现象)_____________________________ ________________________________________________________________________
________________________________________________________________________;
②试管中气球大小(包含试管)体积之比约为(填最简单整数比)Ⅰ∶Ⅱ=________;
③甲同学用手触摸试管,发现盛NaHCO3粉末的试管变凉,而盛Na2CO3粉末的试管温度有升高。由此他得出:不管其状态如何,NaHCO3和HCl反应为吸热反应,而Na2CO3和HCl反应为放热反应。
甲得出的结论是否正确________(填“正确”或“不正确”)。
(2)为研究是吸热反应还是放热反应,继续进行了下列实验(每次实验各做3次平行实验,取平均值):(注:每组固体全溶解且完全反应)
| 序号 | 试剂1 | 试剂2 | 混合前 温度 | 混合后最高或 最低温度 |
| A | 50 mL水 | 2.5 g NaHCO3固体 | 20℃ | 18.5℃ |
| B | 50 mL水 | 3.2 g Na2CO3固体 | 20℃ | 23.3℃ |
| C | 50 mL稀盐酸 | 2.5 g NaHCO3固体 | 20℃ | 17.4℃ |
| D | 50 mL稀盐酸 | 3.2 g Na2CO3固体 | 20℃ | 24.4℃ |
请你帮助填写相关内容:
① 该研究报告的题目是_________________________________________________
________________________________________________________________________;
②该实验中所用的仪器除试管、药匙(或V形纸槽)、气球、下端带环状玻璃棒、烧杯、量筒、保温瓶外,还需要的仪器名称为______________和________________;
③通过上述实验可得出两条结论:
a.Na2CO3溶液和盐酸的反应是______(吸热或放热)反应;
b.NaHCO3溶液和盐酸的反应是______(吸热或放热)反应。
答案 (1)①两支试管中都产生大量气泡,但盛NaHCO3的试管中反应速率要快得多
②42∶53
③不正确
(2)①《NaHCO3、Na2CO3和盐酸反应过程中热效应的研究》
②托盘天平 温度计
③a.放热 b.吸热
查看答案和解析>>
科目:高中化学 来源: 题型:
将有机物完全燃烧,生成CO2和H2O。将12 g该有机物完全燃烧后的产物通过浓H2SO4,浓H2SO4增重14.4 g,再通过碱石灰,碱石灰增重26.4 g。该有机物分子式为( )
A.C4H10 B.C2H6O
C.C3H8O D.C2H4O2
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com