
| 名称 | 性状 | 熔点(℃) | 沸点(℃) | 密度(g/mL) | 溶解性 | |
| 水 | 乙醇 | |||||
| 甲苯 | 无色液体易燃易挥发 | -95 | 110.6 | 0.8669 | 不溶 | 互溶 |
| 苯甲酸 | 白色片状或针状晶体 | 112.4 (100℃左右升华) | 248 | 1.2659 | 微溶 | 易溶 |
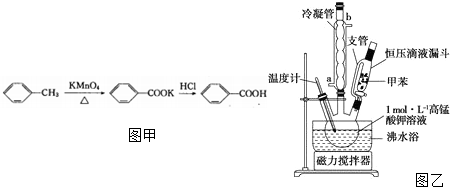
分析 I.(1)甲苯不溶于水会分层,反应生成的苯甲酸钾易溶于水;装置a能冷凝回流蒸汽;支管连接了恒压滴液漏斗中的液体上、下方,使恒压滴液漏斗中的液体上、下方的压强相等;
II.(2)亚硫酸氢钠均有还原性,能还原高锰酸钾;
(3)由表中数据可知,苯甲酸在冷水中的溶解度较小,用冷水洗涤可以减少产品的损失;苯甲酸中的杂质为氯化钾,由表中数据可知苯甲酸易升华,KCl的熔沸点很高,不升华;
III.(4)苯甲酸与氢氧化钾反应生成苯甲酸钾,苯甲酸钾水解显碱性,应该用酚酞作指示剂;溶液颜色由无色变为浅红色说明滴定到达终点;根据氢氧化钾的物质的量求出苯甲酸的物质的量,再求出质量和质量分数.
解答 解:I.(1)甲苯不溶于水会分层,反应生成的苯甲酸钾易溶于水,所以反应后的混合溶液不再分层,说明甲苯完全反应;装置a能冷凝回流水蒸汽、甲苯蒸汽,防止甲苯的挥发而降低产品产率;支管连接了恒压滴液漏斗中的液体上、下方,使恒压滴液漏斗中的液体上、下方的压强相等,便于甲苯顺利滴入三颈烧瓶,
故答案为:分层;将甲苯和水冷凝回流,防止甲苯的挥发而降低产品产率;平衡压强,便于甲苯顺利滴入三颈烧瓶;
II.(2)亚硫酸氢钠均有还原性,能还原高锰酸钾生成二氧化锰、硫酸钾和水,其反应的离子方程式为:2MnO4-+3HSO3-+OH-=2MnO2↓+3SO42-+2 H2O;
故答案为:2MnO4-+3HSO3-+OH-=2MnO2↓+3SO42-+2H2O;
(3)由表中数据可知,苯甲酸在冷水中的溶解度较小,用冷水洗涤可以减少产品的损失,苯甲酸中的杂质为氯化钾,由表中数据可知苯甲酸易升华,KCl的熔沸点很高,不升华,所以提纯含有氯化钾的苯甲酸可以采用升华的方法,故选D,
故答案为:苯甲酸在冷水中的溶解度较小,用冷水洗涤可以减少产品的损失;D;
III.(4)苯甲酸与氢氧化钾反应生成苯甲酸钾,苯甲酸钾水解显碱性,应该用在碱性条件下变色的指示剂,所以选用酚酞作指示剂,溶液颜色由无色变为浅红色,且30S内不褪色,说明滴定到达终点;
n(KOH)=cV=0.1000mol•L-1 ×0.024L=0.0024mol,苯甲酸与氢氧化钾等物质的量恰好反应,则n(苯甲酸)=0.0024mol,
则其总质量为0.0024mol×122g/mol×$\frac{100ml}{25ml}$=1.1712g,所以产品中苯甲酸质量分数为$\frac{1.1712g}{1.22g}$×100%=96.00%,
故答案为:酚酞;溶液颜色由无色变为浅红色,且30S内不褪色;96.00%.
点评 本题考查了苯甲酸的制备实验方案设计,涉及实验现象的判断、装置分析评价、物质的分离提纯、氧化还原反应配平、滴定原理的应用等,清楚制备的原理是解答的关键,题目难度中等.


 活力课时同步练习册系列答案
活力课时同步练习册系列答案科目:高中化学 来源: 题型:选择题
| 元素代号 | X | Y | Z | W |
| 原子半径/pm | 160 | 143 | 70 | 66 |
| 主要化合价 | +2 | +3 | +5、+3、-3 | -2 |
| A. | X、Y元素的金属性 X<Y | |
| B. | W的氢化物比同族其它元素的氢化物稳定,是因为W的氢化物中存在氢键 | |
| C. | Y的最高价氧化物对应的水化物能溶于稀氨水 | |
| D. | 一定条件下,W单质可以将Z单质从其氢化物中置换出来 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
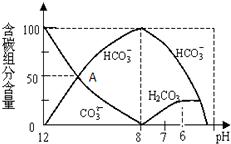 在含有弱电解质的溶液中,往往有多个化学平衡共存.
在含有弱电解质的溶液中,往往有多个化学平衡共存.查看答案和解析>>
科目:高中化学 来源: 题型:填空题
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
| 滴定序号 | 待测液体积 | 所消耗盐酸标准的体积(mL) | |
| 滴定前 | 滴定后 | ||
| 1 | 25.00 | 0.50 | 20.60 |
| 2 | 25.00 | 6.00 | 26.00 |
| 3 | 25.00 | 1.10 | 21.00 |
| 难溶物 | AgCl | AgBr | AgCN | Ag2CrO4 | AgSCN |
| 颜色 | 白 | 浅黄 | 白 | 砖红 | 白 |
| Ksp | 1.77×10-10 | 5.35×10-13 | 1.21×10-16 | 1.12×10-12 | 1.0×10-12 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
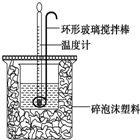 利用如图所示装置测定中和热的实验步骤如下:
利用如图所示装置测定中和热的实验步骤如下:| 实验 序号 | 起始温度t1/℃ | 终止温度t2/℃ | |
| 盐酸 | 氢氧化钠溶液 | 混合溶液 | |
| 1 | 20.0 | 20.1 | 23.2 |
| 2 | 20.2 | 20.4 | 23.4 |
| 3 | 20.5 | 20.6 | 23.6 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com