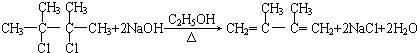��2012?�ӱ���ģ�⣩���ǵ����Ϻ����ḻ��һ��Ԫ�أ���Ԫ�صĵ��ʼ��仯�����ڹ�ũҵ������������������Ҫ���ã�
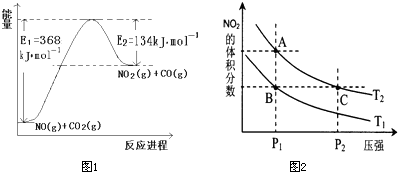
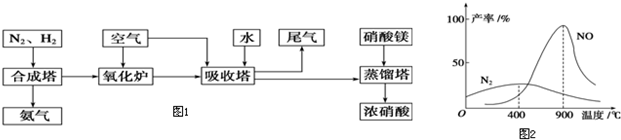
��1��������ͼ1��ʾ�����仯ʾ��ͼ����д��NO��CO
2��Ӧ���Ȼ�ѧ����ʽ
CO2��g��+NO��g��=NO2��g��+CO��g����H=+234kJ?mol-1
CO2��g��+NO��g��=NO2��g��+CO��g����H=+234kJ?mol-1
��
��2���ڹ̶�������ܱ������У��������»�ѧ��Ӧ��
2NH
3��g��?N
2��g��+3H
2��g����H��0��
��ƽ�ⳣ��K���¶�T�Ĺ�ϵ���±���
| T/K |
298 |
398 |
498 |
| ƽ�ⳣ��K |
2.44��10-6 |
K1 |
K2 |
�����ж�K
1��
��
K
2�������������������=������
�ڸ÷�Ӧ���ر��S
��
��
0 �����������������=������
�����и�����˵���÷�Ӧ�Ѵﵽƽ��״̬����
c
c
������ĸ����
a��������N
2��H
2��NH
3�����ʵ���֮��Ϊ1��3��2
b��2v��NH
3��
��=3v��H
2��
��c�������ڻ������ƽ����Է����������ֲ���
d�����������ܶȱ��ֲ���
��һ���¶��£���1L�ܱ������г���1molN
2��3molH
2��������Ӧ���������ݻ��㶨��10min�ﵽƽ��ʱ������������ʵ���Ϊԭ����
����N2��ת���ʦ���N
2��=
20%
20%
��
��3��������ͬ�¶�����ͬŨ�ȵ���������Һ��A��NH
4HCO
3��B��NH
4 HSO
4��C��NH
4Cl����pH�ɴ�С��˳������
ACB
ACB
������ĸ����
���ڳ��³�ѹ��pH������5��NH
4Cl��HCl��Һ��������Һ����ˮ���������c��H
+��֮��Ϊ
104��1
104��1
��
��4���Է�ӦN
2O
4��g��?2NO
2��g����H��0�����¶ȷֱ�ΪT
1��T
2ʱ��ƽ����ϵ��NO
2�����������ѹǿ�仯������ͼ2��ʾ������˵����ȷ����
cd
cd
��
a��A��C����ķ�Ӧ���ʣ�A��C
b��A��C����Ļ�ѧƽ�ⳣ����A��C
c��A��C����N
2O
4��ת���ʣ�A��C
d����״̬B��״̬A�������ü��ȵķ�����