
����Ŀ���ҹ������涨��2006��7��1�պ���ͭ�������ӡ��������������Ȳ��ϵĵ��Ӳ�Ʒ��ֹͶ���г��������йص���������˵���в���ȷ����(����)
A.��������Ӧ������Ⱦ�������»��գ�ʹ֮��Ϊ���õ���Դ
B.�����������ڻ��Ϸ��գ��������еĽ����ٻ�������
C.��������������������������Ⱦ����ˮԴ
D.�����ĵ�������Ӧ�ڱ������ڴ������Ͻ��������������
 ������������ϵ�д�
������������ϵ�д�
| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ���嵥�ʾ��й㷺�Ĺ�ҵ��ֵ����������֪��Br2�ķе�Ϊ59�棬����ˮ���ж��ԣ�ij��ѧС��ģ�ҵ���̴�Ũ���ĺ�ˮ����ȡҺ�壬��Ҫʵ��װ�ã��г�װ����ȥ���������������£� 
������A��B���رջ���b��d������a��c����A�л���ͨ��Cl2����Ӧ������
�ڹر�a��c����b��d����A�й��������ȿ�����
�۽��в���ڵ�ͬʱ����B��ͨ������SO2��
�ܹر�b����a����ͨ��A��B�л���ͨ������Cl2��
�ݽ�B������Һ����������ռ�Һ�壮
��ش�
��1���жϲ�����з�Ӧ�Ѿ������������Ϊ ��
��2��������й����ȿ���������Ϊ�� �����B�з�������Ҫ��Ӧ�����ӷ���ʽΪ ��
��3���ۺϷ�������١��ڡ��ۺ͢ܣ����IJ�����������Ŀ��Ϊ ��
��4����ʵ����β����������ѡ����ĸ�����մ����� a��ˮ b��Ũ���� c��NaOH��Һ d������NaCl��Һ
��5��������У������õ��IJ����������ƾ��ơ��¶ȼơ�β�ӹܡ���ƿ�⣬��������Ҫ�ﵽ�ᴿ���Ŀ�ģ�������Ӧ���ƵĹؼ�����Ϊ ��
��6����ֱ������A��C�����в���ٺ͢ڣ���ַ�Ӧ������ƿ�еμ�ϡ���ᣬ�پ�����ݣ�Ҳ���Ƶ�Һ�壮�μ�ϡ����֮ǰ��C�з�Ӧ������NaBr��NaBrO3�ȣ��÷�Ӧ�Ļ�ѧ����ʽΪ ��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ�����������У����ǻ�Ϊͬ���칹����� ( )
A. ���ۺ������� B. ���Ǻ���ѿ��
C. ������춡�� D. ���Ǻ�������
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ�������л������������ԭ������������ȷ���ǣ� ��
A.![]() 3������1��3������ϩ
3������1��3������ϩ
B.![]() 2���ǻ�����
2���ǻ�����
C.CH3CH��C2H5��CH2CH2CH3 2���һ�����
D.CH3CH��CH3��CH2COOH 3��������
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����ⷨ�Ƽ��ԭ���DZ���ʳ��ˮ�����ڴ����к�����ɳ��Ca2+��Mg2+��Fe3+��SO42�����ʣ������ϵ��Ҫ����˱��뾭�����ƣ�ijУʵ��С�龫�ƴ���ˮ��ʵ��������£�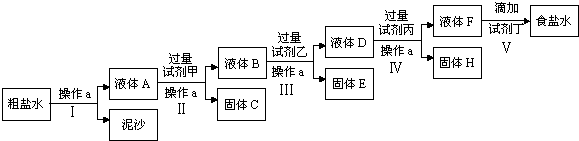
��ش��������⣺
��1������a�������� �� ������������
��2���ڢ��У���������Լ������������ִ��������ܳ��������Լ���Ϊ���ѧʽ����Һ��
��3��д������H�������ʵĻ�ѧʽ��
��4���ڢ����У���μ����Լ���ֱ����Һ�����Ա仯ʱ��д���˹����з�����Ӧ�����ӷ���ʽ�� ��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��14C��C��һ�ַ����Ժ��أ��ڸ߲���������������߲��������ӻ�˱�ը���������Ӻ��14N��ʹ��ת��Ϊ14C.����˵����ȷ����
A. 14Cԭ���������6������B. 14C���ص�������Ϊ8
C. 14C��14N��Ϊͬλ��D. 14C16O2��������Ϊ46
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��ij��ȤС��̽��SO2���廹ԭFe3+ �� ����ʹ�õ�ҩƷ��װ����ͼ��ʾ����������˵�����������ǣ� �� 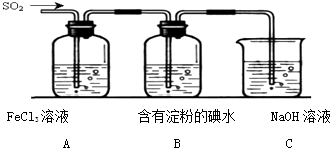
A.�ܱ���I���Ļ�ԭ������SO2��������B����ɫ��Һ��ɫ
B.װ��C������������SO2β������ֹ��Ⱦ����
C.Ϊ����֤A�з�����������ԭ��Ӧ��������ϡ�����ữ��BaCl2 �� ������ɫ����
D.Ϊ����֤A�з�����������ԭ��Ӧ������KMnO4��Һ���Ϻ�ɫ��ȥ
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����Cl2����ijЩ�����л���ʱ�����������HCl�����÷�ӦA����ʵ���ȵ�ѭ�����ã���ӦA��
4HCl+O2  2Cl2+2H2O
2Cl2+2H2O
��֪��������ӦA�У�4mol HCl���������ų�115.6kJ��������
���� 
��1����ӦA���Ȼ�ѧ����ʽ�� ��
��2���Ͽ�1mol H��O����Ͽ�1mol H��Cl�������������ԼΪ kJ��H2O��H��O����HCl��H��Cl�����ǿ���������� ��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ���ƽ���һ�ֹ��صĽ�������������������ʷ�ϣ��ƽ�����������������ģ�������ɳ���Խ�����������»�����֮˵����˵���ƽ�����Ȼ������Ҫ��________��ʽ���ڣ�Ҳ˵���ƽ�Ļ�ѧ��������Ȼ�����·dz�________ ��
�鿴�𰸺ͽ���>>
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com