
| n |
| V |
| ||
| ||
| 10.7g |
| 53.5g/mol |
| 0.2mol��44.8L |
| 2mol |
| 0.2mol |
| 0.5L |
| 3e- |
| 1 |
| 2 |
| 2e- |
| 1 |
| 2 |



| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
| A��1 mol N2�����е�ԭ����ΪNA |
| B����״���£�22.4 Lˮ�к��е�ˮ������ΪNA |
| C�������ʵ�����N2��CO������������ΪNA |
| D�����³�ѹ��32g SO2���״����11.2L N2������ͬ�ķ����� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
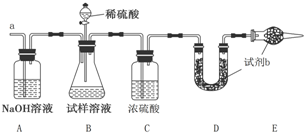 ��ѧ��һ����ʵ��Ϊ��������Ȼ��ѧ����������ʵ��֪ʶ�ش��������⣮
��ѧ��һ����ʵ��Ϊ��������Ȼ��ѧ����������ʵ��֪ʶ�ش��������⣮�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
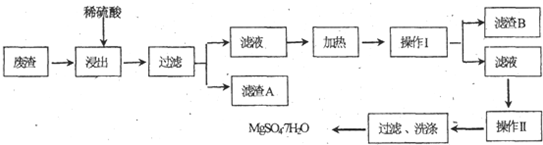
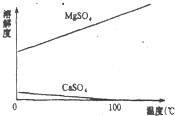
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
| �� ���� |
IA | 0 | ||||||
| l | �� | ��A | ��A | ��A | VA | ��A | ��A | |
| 2 | �� | �� | �� | |||||
| 3 | �� | �� | �� | �� |
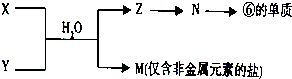
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�

| ������ | Fe��OH��3 | Al��OH��3 | Cu��OH��2 | Mn��OH��2 | CuS | MnS | MnCO3 |
| ������ȫʱ��pH | 3.7 | 5.2 | 6.4 | 9.8 | ��0 | ��7 | ��7 |
| ||
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
| �����Լ� | �����Ը��������Һ������ˮ �۱���̼������Һ�� ������������Һ |
| �ᴿ���� | A����B��ȡ��C��Һ��Dϴ�� |
| �� | �����Լ� | �ᴿ���� |
| ���飨��ϩ�� | ||
| �������������ᣩ |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
| A��K+��Na+��OH-��MnO4- |
| B��Ba2+��Cu2+��NO3-��SO42- |
| C��Mg2+��Na+��OH-��SO42- |
| D��Cl-��Ba2+��NO3-��OH- |
�鿴�𰸺ͽ���>>
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com