
【题目】下列物质的转化在给定条件下能实现的是( )
A. NH3![]() NO2
NO2![]() HNO3B. Al
HNO3B. Al![]() NaAlO2(aq)
NaAlO2(aq)![]() NaAlO2(s)
NaAlO2(s)
C. Fe![]() Fe2O3
Fe2O3![]() FeD. AgNO3(aq)
FeD. AgNO3(aq)![]() [Ag(NH3)2OH(aq)]
[Ag(NH3)2OH(aq)]![]() Ag
Ag
 阅读快车系列答案
阅读快车系列答案科目:高中化学 来源: 题型:
【题目】水合肼(N2H4·H2O)又名水合联氨,是无色透明、具有腐蚀性和强还原性的碱性液体,它是一种重要的化工试剂,利用尿素法生产水合肼的原理为CO(NH2)2+2NaOH+NaClO=Na2CO3+N2H4·H2O+NaCl。
实验一:制备NaClO溶液。(实验装置如图1所示)

(1)下列仪器在配制100 mL7.5mol/L的NaOH溶液时,可能用到的有_______(填字母)。
A.容量瓶 B.烧瓶 C.胶头滴管 D.玻璃棒
(2)锥形瓶中发生反应的离子方程式为____。
实验二:制取水合肼。(实验装置如图2所示)
(3)①装置A的名称为____,反应过程中需控制反应温度,同时将分液漏斗中溶液缓慢滴入A中,如果滴速过快则会导致产品产率降低,同时产生大量氮气,写出该过程的化学反应方程式:____________,故分液漏斗中的溶液是_____(填字母)。
A. CO(NH2)2溶液 B. NaOH和NaClO
②充分反应后,加热A内的溶液,收集108~114℃的馏分,即可得到水合肼的粗产品。
实验三:测定馏分中肼含量。
(4)称取馏分5.0 g,加入适量NaHCO3固体,加水配成250 mL溶液,移岀25.00 mL置于锥形瓶中,并滴加23滴淀粉溶液,用0.10 mol/L的标准I2溶液滴定。滴定过程中,溶液的pH保持在6.5左右。(已知:N2H4·H2O + 2I2=N2↑+ H2O+4HI)
滴定时,碘的标准溶液盛放在____(填“酸式”或“碱式”)滴定管中;本实验滴定终点的现象为____。实验测得消耗I2溶液的平均值为18.00 mL,馏分中水合肼(N2H4·H2O)的质量分数为________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】有Al、CuO、Fe2O3组成的混合物共10.0 g,放入500 mL某浓度的盐酸溶液中,混合物完全溶解,当再加入250 mL 2.0 mol/L的NaOH溶液时,得到的沉淀最多。上述盐酸溶液的浓度为( )
A.0.5 mol/LB.1.0 mol/LC.2.0 mol/LD.3.0 mol/L
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】CsF是离子晶体,其晶格能可通过下图的循环计算得到,以下说法错误的是
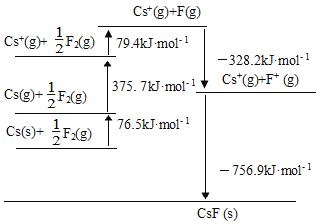
A. Cs原子的第一电离能为452.2 kJ·mol1
B. F-F键的键能为158.8 kJ·mol1
C. CsF的晶格能756.9kJ·mol1
D. 1molCs(s)转变成Cs(g)所要吸收的能量为76.5kJ
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】碱金属元素和卤族元素广泛存在,用化学用语回答下列问题。
(1)氢氟酸可以用来雕刻玻璃。用电子式表示氟化氢的形成过程__________。
(2)过氧化钠可以用于潜水艇中氧气的来源,其与二氧化碳反应的化学方程式是_____。
(3)次氯酸钠溶液(pH>7)和溴化钠溶液混合,可以作为角膜塑形镜的除蛋白液。二者混合后,溶液变成淡黄色,该反应的离子方程式是_____________________。
(4)Li-SOCl2电池可用于心脏起搏器。该电池的电极材料分别为锂和碳,电解液是LiAlCl4-SOCl2。电池的总反应可表示为:4Li+2SOCl2 = 4LiCl +S +SO2。组装该电池必须在无水条件下进行,原因是_____________(用化学方程式表示)。
(5)关于碱金属和卤族元素,下列说法一定正确的是____________。
A.从上到下,单质密度依次增大 B.从上到下,单质熔沸点依次升高
C.从上到下,原子半径依次增大 D.单质都可以与水反应
(6)常温下,KMnO4固体和浓盐酸反应产生氯气。为验证卤素单质氧化性的相对强弱,某小组用下图所示装置进行实验(夹持仪器已略去,气密性已检验)。
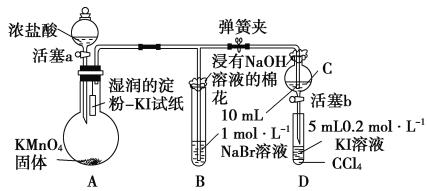
实验过程:
Ⅰ.打开弹簧夹,打开活塞a,滴加浓盐酸。
Ⅱ.当B和C中的溶液都变为黄色时,夹紧弹簧夹。
Ⅲ.当B中溶液由黄色变为红棕色时,关闭活塞a。
Ⅳ.……
①验证氯气的氧化性强于碘的实验现象是____________________。
②B中溶液发生反应的离子方程式是__________________________。
③为验证溴的氧化性强于碘,过程Ⅳ的操作和现象是______________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列叙述中正确的是( )
A. 1 molN2与4molH2混合充分反应,则转移的电子数目为6mol
B. 向0.1mol·L-1CH3COONa溶液中加入少量水,溶液中![]() 减小
减小
C. 常温下,C(s)+H2O(g)![]() CO(g)+H2(g)不能自发进行,则该反应的ΔH>0
CO(g)+H2(g)不能自发进行,则该反应的ΔH>0
D. HCl和NaOH反应的中和热为-57.3kJ·mol-1,则H2SO4和Ba(OH)2反应的中和热为-114.6 kJ·mol-1
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】有Ⅰ~Ⅳ四个体积均为0.5 L的恒容密闭容器,在Ⅰ、Ⅱ、Ⅲ中按不同投料比(Z)充入HCl和O2(如下表),加入催化剂发生反应4HCl(g)+O2(g)![]() 2Cl2(g)+2H2O(g);ΔH,HCl的平衡转化率(α)与Z和温度(t)的关系如图所示。下列说法正确的是( )
2Cl2(g)+2H2O(g);ΔH,HCl的平衡转化率(α)与Z和温度(t)的关系如图所示。下列说法正确的是( )
容器 | 起始时 | ||
t/℃ | n(HCl)/mol | Z | |
Ⅰ | 300 | 0.25 | a |
Ⅱ | 300 | 0.25 | b |
Ⅲ | 300 | 0.25 | 4 |
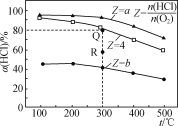
A. ΔH<0,a<4<b
B. 300℃该反应的平衡常数的值为64
C. 容器Ⅲ某时刻处在R点,则R点的υ正>υ逆,压强:p(R)>p(Q)
D. 若起始时,在容器Ⅳ中充入0.25molCl2和0.25molH2O(g),300℃达平衡时容器中c(HCl)=0.1mol·L-1
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】大气中氮氧化物和碳氢化合物受紫外线作用可产生一次污染物——光化学烟雾,其中部分物质的反应过程如图所示。下列说法正确的是( )

A.该过程中![]() 作催化剂B.反应过程中没有电子转移
作催化剂B.反应过程中没有电子转移
C.反应过程中氮氧化物不断被消耗D.丙烯转化为甲醛和乙醛
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】电化学在生产生活中都具有重要的作用和意义:
(1)图为绿色电源“二甲醚(CH3OCH3)燃料电池”的工作原理示意图:该电池的负极反应式为:_________,若串联该燃料电池来电解硫酸钠溶液,消耗4.6g二甲醚后总共可在电解池两极收集到13.44L(标况)气体,该套装置的能量利用率为___________.(保留三位有效数字)

(2)制备Na2S2O5也可采用三室膜电解技术,装置如图所示,其中SO2碱吸收液中含有NaHSO3和Na2SO3。阳极的电极反应式为_______。电解后,____室的NaHSO3浓度增加。将该室溶液进行结晶脱水,可得到Na2S2O5。

(3)二氧化氯(ClO2,黄绿色易溶于水的气体)是高效、低毒的消毒剂,答下列问题:
实验室用NH4Cl、盐酸、NaClO2(亚氯酸钠)为原料,通过以下过程制备ClO2:电解时发生反应的化学方程式为______。溶液X中大量存在的阴离子有___。

(4)测定混合气中ClO2的含量:
Ⅰ.在锥形瓶中加入足量的碘化钾,用50 mL水溶解后,再加入 3 mL稀硫酸. 将一定量的混合气体通入混合溶液中充分吸收, 发生反应: 2ClO2+10I-+8H+=2Cl-+5I2+4H2O.
Ⅱ.用0.1000 mol·L-1硫代硫酸钠标准溶液滴定锥形瓶中的溶液(I2+2S2O32-=2I-+S4O62-),以淀粉溶液为指示剂显示终点时共用去20.00 mL硫代硫酸钠溶液。
①滴定至终点的现象是______, 测得混合气中ClO2的质量为______ g。
②测定混合气中ClO2的含量的操作中可能使测定结果偏低的是____(填字母)。
A.滴定管未润洗就直接注入硫代硫酸钠标准液
B.锥形瓶用蒸馏水洗净后没有干燥
C.滴定管读取标准液体积时,开始仰视读数,滴定结束时俯视读数
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com