
A、B、C、D、E、F、G是前四周期(除稀有气体)原子序数依次增大的七种元素,A的原子核外电子只有一种运动状态;B、C的价电子层中未成对电子数都是2;B、C、D同周期;E核外的s、p能级的电子总数相筹;F与E同周期且第一电离能比E小;G的+1价离子(G+)的各层电子全充满。回答下列问题: (相关问题用元素符号表示)
(1)写出E的基态原子的电子排布式________________________。
(2)B与C可形成化合物BC和BC2,BC2属于__________(填“极性”、“非极性”)分子,1 mol BC含有π键为____________________mol。
(3)由元素A、C、G组成的离子[G(A2C)4]2+在水溶液中显天蓝色,不考虑空间结构,[G(A2C)4]2+的结构可用示意图表示为__________(配位键用→标出)。
(4)测定A、D形成的化合物的相对分子质量时,实验测定值一般高于理论值的原因是_______。
(5)由元素A、B、F组成的原子个数比9 : 3 : 1的一种物质,分子中含三个相同的原子团,其结构简式为________________,分子中F原子的杂化方式为__________,该物质遇水爆炸,生成白色沉淀和无色气体,反应的化学方程式为____________________。
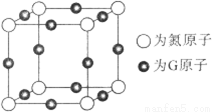
(6)G与氮元素形成的某种化合物的晶胞结构如图,则该化合物的化学式为__________,若晶体密度为a g·cm-3,列式计算G原子与氮原子最近的距离为__________pm(不必计算出数值,阿伏加德罗常数的值用NA表示)。
科目:高中化学 来源:2017届江苏省高三上学期摸底考试化学试卷(解析版) 题型:填空题
尿素(H2NCONH2)是一种农业生产中常用的氮肥。在工业上,尿素还用于制造有机铁肥,如[Fe(H2NCONH2)6](NO3)3[三硝酸六尿素合铁(III)]。回答下列问题:
(1)基态Fe3+的核外价电子排布式为 。
(2)C、N、O三种元素的第一电离能由大到小的顺序是 。
(3)在一定条件下,NH3与CO2能合成尿素,1mol尿素分子中,σ键的数目为 ;尿素分子中C原子的杂化方式为 。
(4)NO3-的空间构型为 ;写出NO3-互为等电子体的一种分子的化学式 。
查看答案和解析>>
科目:高中化学 来源:2016-2017学年河北省高二上学期摸底化学试卷(解析版) 题型:选择题
将4molA气体和2molB气体在2L的容器中混合并在一定条件下发生如下反应:2A(g)+B(g)?2C(g) 若经2s(秒)后测得C的浓度为0.6mol/L,现有下列几种说法:
①用物质A表示的反应的平均速率为0.3mol/(L•s)
②用物质B表示的反应的平均速率为0.6mol/(L•s)
③2S(秒)时物质A和B的转化率一样
④2S(秒)时物质B的浓度为0.3mol/L
其中正确的是( )
A.①③ B.③④ C.②③ D.①④
查看答案和解析>>
科目:高中化学 来源:2016-2017学年广东省汕头市高二上学期入学考试化学试卷(解析版) 题型:选择题
燃料电池是利用燃料(如H2、CO、CH4等)跟氧气反应从而将化学能转化成电能的装置。下列关于甲烷燃料电池(NaOH溶液作电解质溶液)的说法中正确的是
A.负极反应为O2+2H2O+4e-= 4OH-
B.放电时正极发生氧化反应,外电路中电子从正极流向负极
C.负极反应为CH4+10OH--8e-= CO32-+7H2O
D.随着放电的进行,溶液的pH增大
查看答案和解析>>
科目:高中化学 来源:2016-2017学年广东省汕头市高二上学期入学考试化学试卷(解析版) 题型:选择题
下列离子方程式书写正确的是:
A.将Ba(OH)2溶液不断加入KAl(SO4)2溶液中反应至沉淀物质的量最大:3Ba2+ + 6OH– + 2Al3+ + 3SO42–== 3BaSO4↓+ 2Al(OH)3↓
B.Cl2通入冷水中:Cl2 + H2O == Cl– + ClO– + 2H+
C.CuSO4溶液跟Ba(OH)2溶液混合:Ba2+ + SO42– == BaSO4↓
D.漂白粉溶液中通入SO2气体:Ca2++2ClO-+SO2+H2O=CaSO3↓+2HClO
查看答案和解析>>
科目:高中化学 来源:2017届新疆生产建设兵团二中高三上第一次月考化学试卷(解析版) 题型:选择题
已知酸性K2Cr2O7溶液可与FeSO4反应生成Fe3+和Cr3+。现将硫酸酸化的K2Cr2O7溶液与FeSO4溶液混合,充分反应后再向所得溶液中加入KI溶液,混合溶液中Fe3+的物质的量随加入的KI的物质的量的变化关系如图所示,下列说法中不正确的是( )
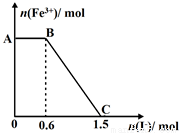
A.图中AB段的氧化剂为K2Cr2O7
B.图中BC段发生的反应为2Fe3++2I-=2Fe2++I2
C.开始加入的K2Cr2O7为0.25 mol
D.K2Cr2O7可与FeSO4反应的物质的量为1:3
查看答案和解析>>
科目:高中化学 来源:2017届新疆生产建设兵团二中高三上第一次月考化学试卷(解析版) 题型:选择题
下列反应中,属于加成反应的是( )
A.苯和液溴在FeBr3催化作用下生成溴苯
B.丙烯和氯气在一定条件卜反应生成ClCH2CH=CH2的反应
C.乙烯使酸性高锰酸钾溶液褪色
D.乙烯与HCl气体反应生成一氯乙烷
查看答案和解析>>
科目:高中化学 来源:2017届湖南省高三上学期第二次月考化学试卷(解析版) 题型:实验题
我国化工专家侯德榜,改进氨碱法设计了“联合制碱法”,为世界制碱工业作出了突出贡献.生产流程如图1:

(1)完成有关反应的化学方程式
①沉淀池:NH3+CO2+H2O+NaCl=NaHCO3↓+NH4Cl
②煅烧炉:
(2)联合制碱法的优点表述中,不正确的是
A.生产原料为:食盐、NH3、CO2
B.副产物氯化铵可做氮肥
C.生产过程中可循环利用的物质只有CO2
D.原料利用率高
某实验小组,利用下列装置图2模拟“联合制碱法”的第一步反应.

(3)上述装置中接口连接顺序为 ;
A.a接c;b接f、e接d B.a接d;b接f、e接c
C.b接d;a接e、f接c D.b接c;a接f、e接d
(4)D中应选用的液体为 .
为测定产品纯碱的成分和含量,做如下实验.假设产品纯碱中只含NaCl、NaHCO3杂质.
(5)检验产品纯碱中是否含有NaCl,可取少量试样溶于水后,再滴加 试剂.
(6)滴定法测定纯碱产品中NaHCO3含量的方法是:准确称取纯碱样品W g,放入锥形瓶中加蒸馏水溶解,加1~2滴酚酞指示剂,用c mol/L的HCl溶液滴定至溶液由红色变为无色(指示CO32﹣+H+=HCO3﹣反应的终点),所用HCl溶液体积为V1mL,再加1~2滴甲基橙指示剂,继续用HCl溶液滴定至溶液由黄色变为橙色,所用HCl溶液总体积为V2 mL.则纯碱样品中NaHCO3质量分数为 .
查看答案和解析>>
科目:高中化学 来源:2016-2017学年山东省淄博市高二上学期开学测化学试卷(解析版) 题型:选择题
合金在生产及生活中具有广泛的应用,下列物质属于合金的是
A.石墨 B.水晶 C.不锈钢 D.陶瓷
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com