
| 1000�Ѧ�% |
| M |
| n |
| V |
| 1000�Ѧ�% |
| M |
| 1000��1.84��98% |
| 98 |


 ��������һ���þ�ϵ�д�
��������һ���þ�ϵ�д� Сѧ��10����Ӧ����ϵ�д�
Сѧ��10����Ӧ����ϵ�д�
| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
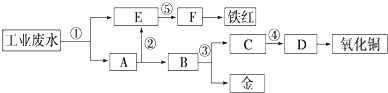
| A���μӷ�Ӧ��������0.4mol |
| B���������������Ϊ1.68 L |
| C���˷�Ӧ������ת�Ƶĵ���Ϊ0.3 mol |
| D����������к�NO21.12 L |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
| A����ù�صȿ����ضԲ�ԭ�������ƺ�ɱ�����ã�����ʹ��֮ǰҪ���й�����ʵ�� |
| B����ȡ����������Ȼ��������ֹʹ�������ã�����������к��������������ڶ�Ʒ |
| C����Ƽ��ǹ��ʰ�ί���ϸ��ֹʹ�õ��˷ܼ� |
| D��R��ʾ�Ǵ���ҩ��OTC��ʾ����ҩ |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
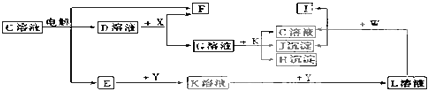
| A������ |
| B������CaSO4 |
| C������BaCl2 |
| D����ˮ |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
| A��Na2SO4 |
| B��CH3COOH |
| C��NaOH |
| D��CH3COOK |
�鿴�𰸺ͽ���>>
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com