
 ijĪĀ¶ČŹ±£¬ŌŚ2LµÄĆܱÕČŻĘ÷ÖŠ£¬X”¢Y”¢Z£Ø¾łĪŖĘųĢå£©ČżÖÖĪļÖŹµÄĮæĖꏱ¼äµÄ±ä»ÆĒśĻßČēĶ¼ĖłŹ¾£®
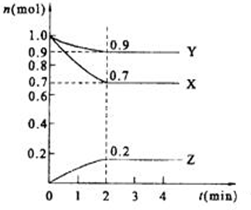
ijĪĀ¶ČŹ±£¬ŌŚ2LµÄĆܱÕČŻĘ÷ÖŠ£¬X”¢Y”¢Z£Ø¾łĪŖĘųĢå£©ČżÖÖĪļÖŹµÄĮæĖꏱ¼äµÄ±ä»ÆĒśĻßČēĶ¼ĖłŹ¾£®·ÖĪö £Ø1£©øł¾ŻĒśĻߵıä»ÆĒ÷ŹĘÅŠ¶Ļ·“Ó¦ĪļŗĶÉś³ÉĪļ£¬øł¾ŻĪļÖŹµÄĮæ±ä»ÆÖ®±ČµČÓŚ»Æѧ¼ĘĮæŹżÖ®±ČŹéŠ“·½³ĢŹ½£»
£Ø2£©øł¾Żv=$\frac{”÷c}{”÷t}$¼ĘĖć£»
£Ø3£©·“Ó¦µ½Ä³Ź±æĢø÷ĪļÖŹµÄĮæĒ”ŗĆĀś×ć£ŗn £ØX£©=n £ØY£©=n £ØZ£©£¬øł¾Ż·½³ĢŹ½ÖŖ£¬²Ī¼Ó·“Ó¦µÄn£ØX£©=1.5n£ØZ£©£¬²Ī¼Ó·“Ó¦µÄn£ØY£©=0.5n£ØZ£©£¬ĖłŅŌ·“Ó¦³õŹ¼a=n£ØZ£©+1.5n£ØZ£©=2.5n£ØZ£©£¬b=n£ØY£©+0.5n£ØZ£©£»
£Ø4£©øł¾ŻÓ°Ļģ»Æѧ·“Ó¦ĖŁĀŹµÄŅņĖŲÅŠ¶Ļ£»
£Ø5£©øł¾ŻÓ°Ļģ»ÆŃ§Ę½ŗāדĢ¬µÄĢŲÕ÷ŗĶÓ°ĻģŅņĖŲ£¬»Æѧ·“Ó¦ĻŽ¶ČŹĒŌŚŅ»¶ØĢõ¼žĻĀµÄĻŽ¶Č£®
½ā“š ½ā£ŗ£Ø1£©ÓÉĶ¼ĻóæÉŅŌ擳ö£¬·“Ó¦ÖŠX”¢YµÄĪļÖŹµÄĮæ¼õŠ”£¬ZµÄĪļÖŹµÄĮæŌö¶ą£¬ŌņX”¢YĪŖ·“Ó¦Īļ£¬ZĪŖÉś³ÉĪļ£¬ĒŅ”÷n£ØX£©£ŗ”÷n£ØY£©£ŗ”÷n£ØZ£©=0.1mol£ŗ0.3mol£ŗ0.2mol=1£ŗ3£ŗ2£¬Ōņ·“Ó¦µÄ»Æѧ·½³ĢŹ½ĪŖ£ŗX+3Y?2Z£¬
¹Ź“š°øĪŖ£ŗ3X+Y?2Z£»
£Ø2£©v£ØZ£©=$\frac{”÷c}{”÷t}$=$\frac{0.2mol”Ā2L}{2min}$=0.05mol/£ØL£®min£©£»
¹Ź“š°øĪŖ£ŗ0.05mol/£ØL£®min£©£»
£Ø3£©·“Ó¦µ½Ä³Ź±æĢø÷ĪļÖŹµÄĮæĒ”ŗĆĀś×ć£ŗn £ØX£©=n £ØY£©=n £ØZ£©£¬øł¾Ż·½³ĢŹ½ÖŖ£¬²Ī¼Ó·“Ó¦µÄn£ØX£©=1.5n£ØZ£©£¬²Ī¼Ó·“Ó¦µÄn£ØY£©=0.5n£ØZ£©£¬ĖłŅŌ·“Ó¦³õŹ¼a=n£ØZ£©+1.5n£ØZ£©=2.5n£ØZ£©£¬b=n£ØY£©+0.5n£ØZ£©=1.5n£ØZ£©£¬ĖłŅŌa£ŗb=2.5n£ØZ£©£ŗ1.5n£ØZ£©=5£ŗ3£»
¹Ź“š°øĪŖ£ŗ5£ŗ3£»
£Ø4£©A£®ŗćŃ¹Ź±³äČėHe£¬Ļąµ±ÓŚ¶Ō·“Ó¦¼õŃ¹£¬ĖŁĀŹ¼õĀż£¬A“ķĪó£»
B£®ŗćČŻŹ±³äČėHe£¬ĪļÖŹµÄÅضČĪ“±ä£¬·“Ó¦ĖŁĀŹ²»øı䣬B“ķĪó£»
C£®ŗćČŻŹ±³äČėX£¬Ōö¼Ó·“Ó¦ĪļµÄÅØ¶Č£¬·“Ó¦ĖŁĀŹ¼Óæģ£¬CÕżČ·£»
D£®¼°Ź±·ÖĄė³öZ£¬¼õÉŁĪļÖŹÅØ¶Č£¬·“Ó¦ĖŁĀŹ¼õĀż£¬D“ķĪó£»
E£®ÉżøßĪĀ¶Č£¬·“Ó¦ĖŁĀŹ¼Óæģ£¬EÕżČ·£»
F£®Ń”Ōńøߊ§µÄ“߻ƼĮ£¬·“Ó¦ĖŁĀŹ¼Óæģ£¬FÕżČ·£»
¹Ź“š°øĪŖ£ŗCEF£»
£Ø5£©A£®ÉżøßĪĀ¶Č£¬»ÆŃ§Ę½ŗā·¢ÉśŅĘ¶Æ£¬¼“»Æѧ·“Ó¦µÄĻŽ¶Čøı䣬AÕżČ·£»
B£®ÉżøßĪĀ¶ČÕż·“Ó¦ĖŁĀŹÄę·“Ó¦ĖŁĀŹ¾ł¼Óæģ£¬B“ķĪó£»
C£®øıäĶā½ēĢõ¼ž£¬»Æѧ·“Ó¦µÄĻŽ¶ČŹĒæÉŅŌøıäµÄ£¬C“ķĪó£»
D£®Ōö“óYµÄÅØ¶Č£¬Õż·“Ó¦ĖŁĀŹ¼Óæģ£¬Äę·“Ó¦ĖŁĀŹŅ²¼Óæģ£¬D“ķĪó£»
¹Ź“š°øŃ”£ŗA£®
µćĘĄ ±¾Ģāæ¼²é»ÆŃ§Ę½ŗāĶ¼Ļó·ÖĪö£¬»ÆŃ§Ę½ŗāµÄÓŠ¹Ų¼ĘĖć£¬Ó°Ļģ»Æѧ·“Ó¦ĖŁĀŹµÄŅņĖŲ£¬ĢāÄæÄŃ¶Č²»“ó£¬×¢Ņā·ÖĪöø÷ĪļÖŹµÄĮæµÄ±ä»ÆĒśĻߣ¬Ąķ½ā»Æѧ·“Ó¦ĻŽ¶ČµÄĢŲÕ÷£¬°ŃĪÕ»Æѧ·½³ĢŹ½µÄÅŠ¶Ļ·½·Ø£®


 ĒįĖÉæĪĢƵ„ŌŖĘŚÖŠĘŚÄ©×ØĢā³å“Ģ100·ÖĻµĮŠ“š°ø
ĒįĖÉæĪĢƵ„ŌŖĘŚÖŠĘŚÄ©×ØĢā³å“Ģ100·ÖĻµĮŠ“š°ø
| Äź¼¶ | øßÖŠæĪ³Ģ | Äź¼¶ | ³õÖŠæĪ³Ģ |
| øßŅ» | øßŅ»Ćā·ŃæĪ³ĢĶĘ¼ö£” | ³õŅ» | ³õŅ»Ćā·ŃæĪ³ĢĶĘ¼ö£” |
| ø߶ž | ø߶žĆā·ŃæĪ³ĢĶĘ¼ö£” | ³õ¶ž | ³õ¶žĆā·ŃæĪ³ĢĶĘ¼ö£” |
| øßČż | øßČżĆā·ŃæĪ³ĢĶĘ¼ö£” | ³õČż | ³õČżĆā·ŃæĪ³ĢĶĘ¼ö£” |
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗŃ”ŌńĢā
| A£® | K+”¢Cl-”¢NO3-”¢CO32- | B£® | Ag+”¢K+”¢Cl-”¢NO3- | ||
| C£® | Cu2+”¢SO42-”¢Na+”¢CO32- | D£® | Ba2+”¢OH-”¢Mg2+”¢NO3- |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ½ā“šĢā
| ĪĀ¶Č£Ø¾ų¶ŌĪĀ¶Č£© | K1 | K2 |
| 973 | 1.47 | 2.38 |
| 1173 | 2.15 | 1.67 |
| Ź±¼ä/min | CO2 | H2O | CO | H2 |
| 0 | 0.2000 | 0.3000 | 0 | 0 |
| 2 | 0.1740 | 0.2740 | 0.0260 | 0.0260 |
| 3 | c1 | c2 | c3 | c3 |
| 4 | c1 | c2 | c3 | |
| 5 | 0.0727 | 0.1727 | 0.1273 | 0.1273 |
| 6 | 0.0350 | 0.1350 | 0.1650 |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ½ā“šĢā

²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗŃ”ŌńĢā
| A£® | ČÜŅŗÖŠI-ÅØ¶Č¼õŠ” | B£® | ČܶȻż³£ŹżKspŌö“ó | ||
| C£® | ³ĮµķČܽāĘ½ŗāĻņ×óŅĘ¶Æ | D£® | ČÜŅŗÖŠPb2+ÅضČŌö“ó |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ½ā“šĢā
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗŃ”ŌńĢā
| A£® | ¢Ł¢Ś¢Ü | B£® | ¢Ł¢Ü¢Ž | C£® | ¢Ś¢Ū¢Ž | D£® | ¢Ū¢Ż¢Ž |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ½ā“šĢā
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗĢīæÕĢā
²éæ““š°øŗĶ½āĪö>>
°Ł¶ČÖĀŠÅ - Į·Ļ°²įĮŠ±ķ - ŹŌĢāĮŠ±ķ
ŗž±±Ź”»„ĮŖĶųĪ„·ØŗĶ²»Į¼ŠÅĻ¢¾Ł±ØĘ½ĢØ | ĶųÉĻÓŠŗ¦ŠÅĻ¢¾Ł±Ø×ØĒų | µēŠÅÕ©Ę¾Ł±Ø×ØĒų | É꥜Ź·ŠéĪŽÖ÷ŅåÓŠŗ¦ŠÅĻ¢¾Ł±Ø×ØĒų | ÉęĘóĒÖČؾŁ±Ø×ØĒų
Ī„·ØŗĶ²»Į¼ŠÅĻ¢¾Ł±Øµē»°£ŗ027-86699610 ¾Ł±ØÓŹĻä£ŗ58377363@163.com